Содержание
- 2. Химические реакции – это превращение одних веществ в другие
- 3. Унылая пора! Очей очарованье! Приятна мне твоя прощальная краса – Люблю я пышное природы увяданье, В
- 4. Трещат сухие сучья, Разгораясь жарко, Освещая тьму ночную Далеко и ярко! И.З. Суриков
- 5. В декабре, в декабре Все деревья в серебре, Нашу речку, словно в сказке, За ночь вымостил
- 6. А если медь в печи нагреть, То станет тяжелее медь С окалиною вместе. Не верите –
- 7. На рукомойнике моем Позеленела медь. Но так играет луч на нем, Что весело глядеть. А. Ахматова
- 8. Когда металл в крутые формы льем, Мне верится, что оживут в металле Горячие полдневные поля. Кипит
- 9. Признаки химических реакций: изменение цвета, выпадение осадка, выделение газа, выделение тепла и света
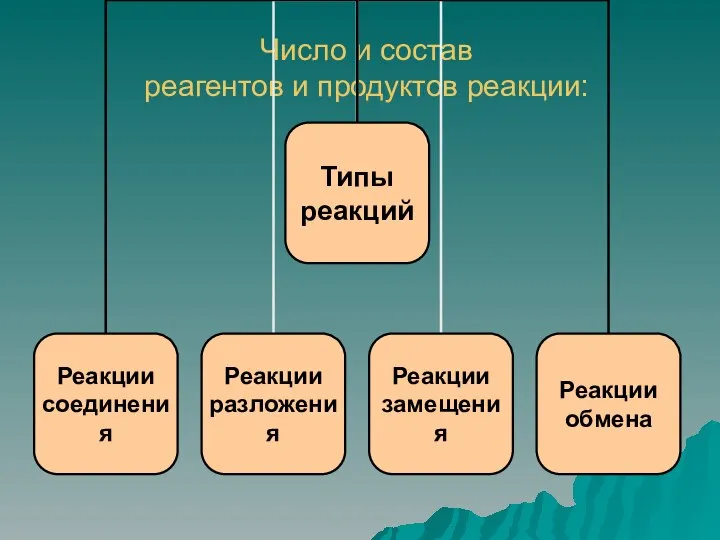
- 10. Число и состав реагентов и продуктов реакции:
- 11. «Доводы, до которых человек додумывается сам, обычно убеждают его больше, нежели те, которые пришли в голову
- 12. Реакции соединения - это реакции, при которых из двух или более веществ образуется одно сложное вещество
- 13. Реакции разложения - это реакции, при которых из одного сложного вещества образуются два или более веществ
- 14. Реакции замещения - это реакции, при которых атомы простого вещества замещают атомы в сложном веществе AB
- 15. Реакции обмена - это реакции между двумя сложными веществами, при которых они обмениваются своими составными частями
- 16. Определите тип каждой реакции: 2HgO → 2Hg + O2 Р. разложения CaO + H2O → Ca(OH)2
- 17. Даны вещества: Zn, O2, HCl, Zn(OH)2 Напишите по одной реакции каждого типа, возможные между этими веществами
- 18. Даны вещества: Zn, O2, HCl, Zn(OH)2. Напишите по одной реакции каждого типа, возможные между этими веществами
- 20. Скачать презентацию
















 Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Презентация на тему Полисахариды. Крахмал и целюлоза
Презентация на тему Полисахариды. Крахмал и целюлоза  Получение металлов в промышленности. Чёрная металлургия
Получение металлов в промышленности. Чёрная металлургия Строение атома. Строение электронных оболочек атомов
Строение атома. Строение электронных оболочек атомов Презентация на тему Металлы тоже воевали
Презентация на тему Металлы тоже воевали  8-11 2 валентность
8-11 2 валентность Химическая связь и строение вещества
Химическая связь и строение вещества Решение задач на смеси, растворы и сплавы
Решение задач на смеси, растворы и сплавы Теория электролитической диссоциации
Теория электролитической диссоциации Пространственная изомерия органических соединений
Пространственная изомерия органических соединений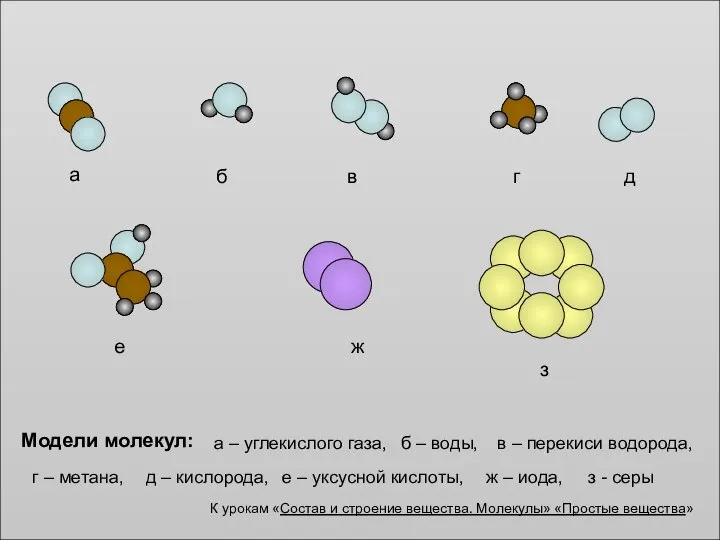 Модели молекул
Модели молекул Вода
Вода Применение обратимых и необратимых реакций в быту
Применение обратимых и необратимых реакций в быту Спирты. Классификация спиртов
Спирты. Классификация спиртов Коррозия металлов
Коррозия металлов Химический тренажер
Химический тренажер Кислород и сера
Кислород и сера Презентация на тему Зеленая химия и проблемы устойчивого развития
Презентация на тему Зеленая химия и проблемы устойчивого развития  Химическое вещество золото
Химическое вещество золото Фосфор туралы
Фосфор туралы Кислородные соединения углерода
Кислородные соединения углерода Химическая термодинамика. Термодинамические потенциалы
Химическая термодинамика. Термодинамические потенциалы Классификация реакций. Теория-кинетика
Классификация реакций. Теория-кинетика Алканы
Алканы Неметаллы. 8 класс
Неметаллы. 8 класс Изготовление слайма в домашних условиях
Изготовление слайма в домашних условиях Кислота
Кислота Тест по химии
Тест по химии