Содержание
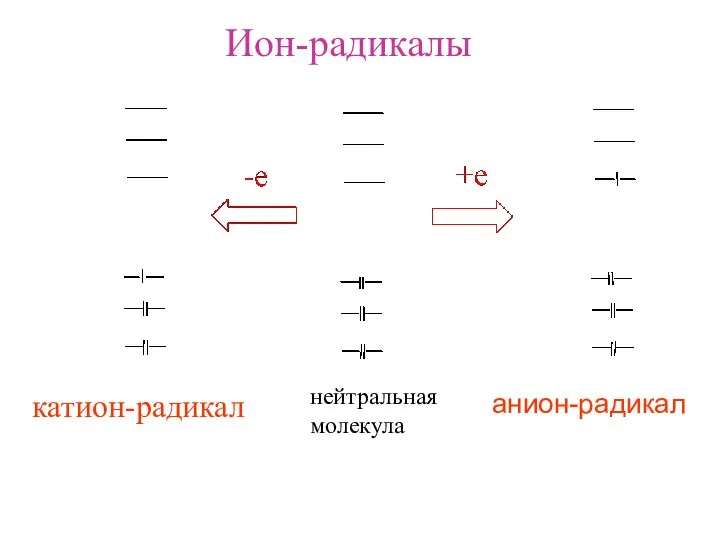
- 2. Ион-радикалы нейтральная молекула катион-радикал анион-радикал
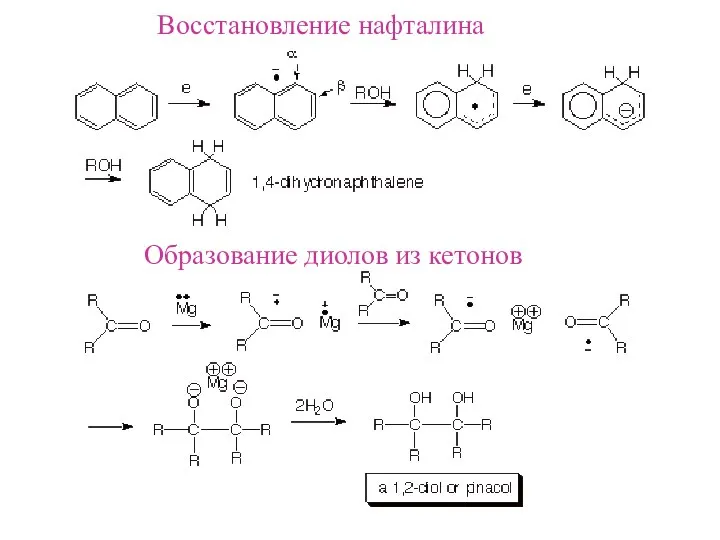
- 3. Восстановление нафталина Образование диолов из кетонов
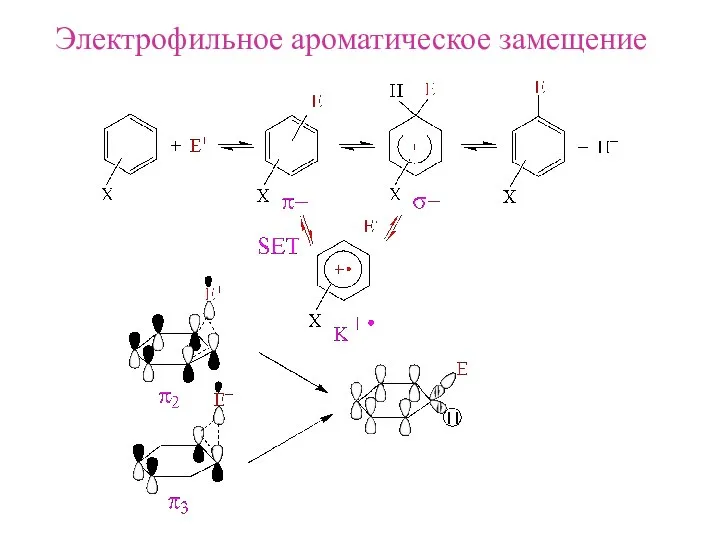
- 4. Электрофильное ароматическое замещение
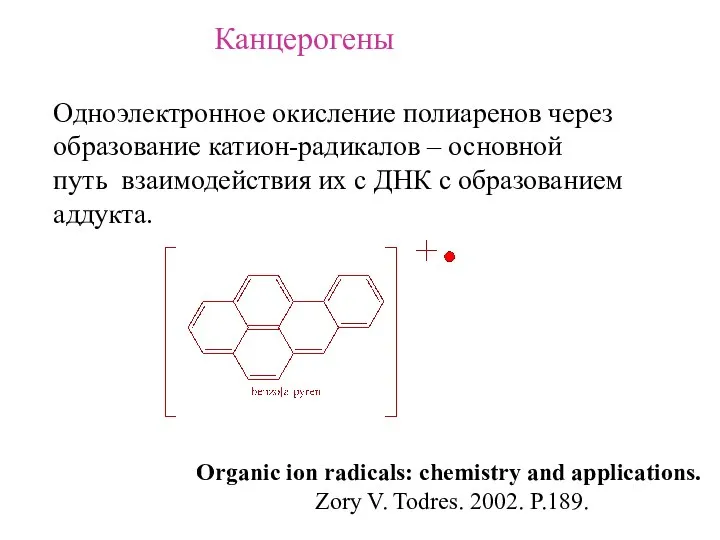
- 5. Канцерогены Одноэлектронное окисление полиаренов через образование катион-радикалов – основной путь взаимодействия их с ДНК с образованием
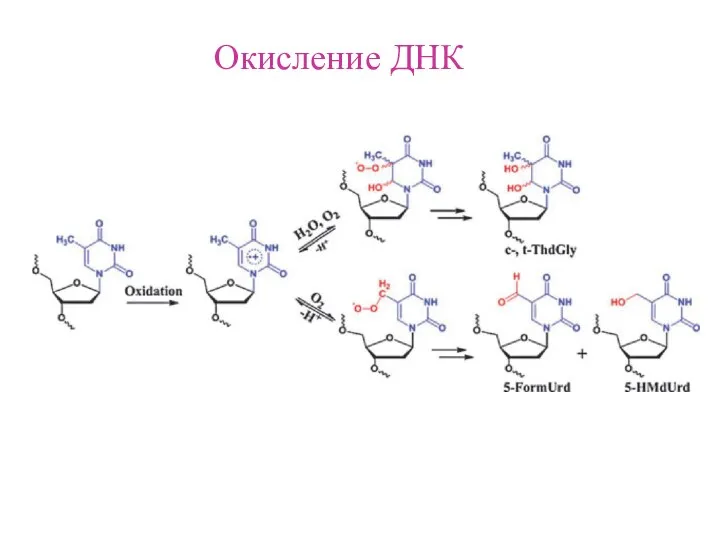
- 6. Окисление ДНК
- 7. Методы изучения ион-радикалов ЭПР (τ > 10−3 сек., струевая методика до 10−4) Переходы удовлетворяют резонансу: hν
- 8. 2. Метод измерения магнитной восприимчивости Позволяет определить концентрацию ион-радикалов 3. ЯМР Позволяет определить концентрацию ион-радикалов по
- 9. 5. ЭСП характеризует разницу энергий занятых (или SOMO) и незанятых МО] 6. ИКС (сведения о строении
- 10. 8. Фотоэлектронная спектроскопия В газе: облучение фотонами с определенной энергией (He(I)α 21.21ev). Измеряется кинетическая энергия поглощаемых
- 11. Ион-радикалы σ-доноров Алканы плохие акцепторы и доноры электронов Ip, э.в. СН4 12.61 Ip, э.в. С10 Н22
- 12. AlkH ионизируются в газе (Heα), но трудно окисляются в растворе Техника матричной изоляции С2v, D2d Обнаружен
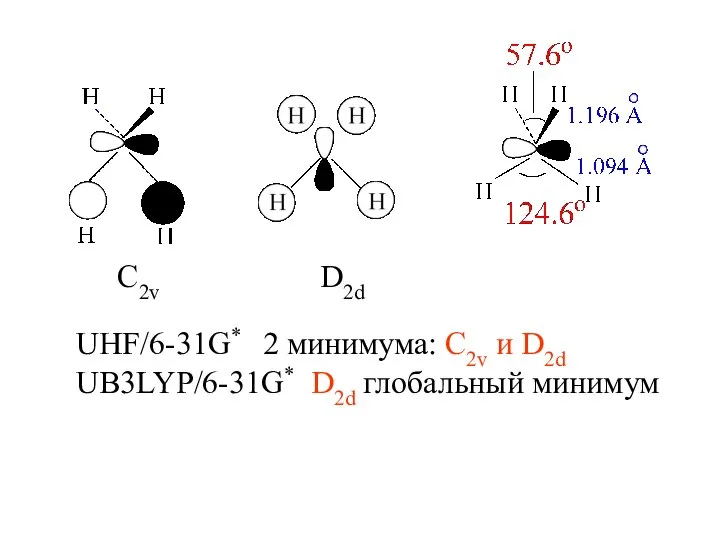
- 13. С2v D2d UHF/6-31G* 2 минимума: C2v и D2d UB3LYP/6-31G* D2d глобальный минимум
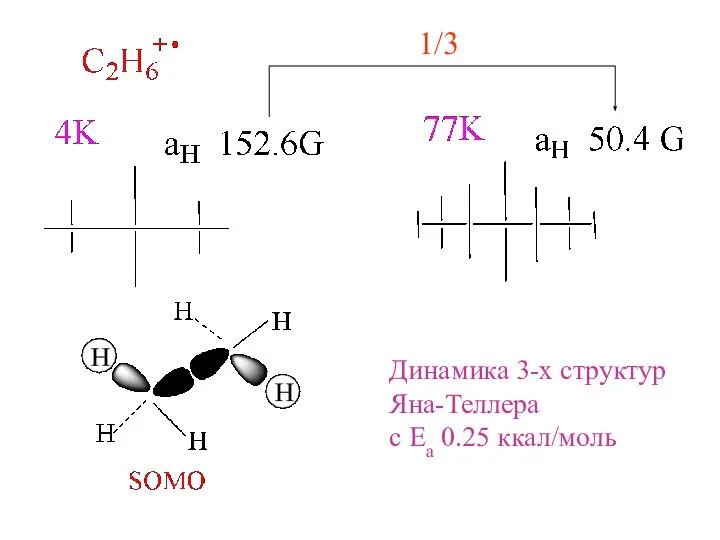
- 14. Динамика 3-х структур Яна-Теллера с Еа 0.25 ккал/моль 1/3
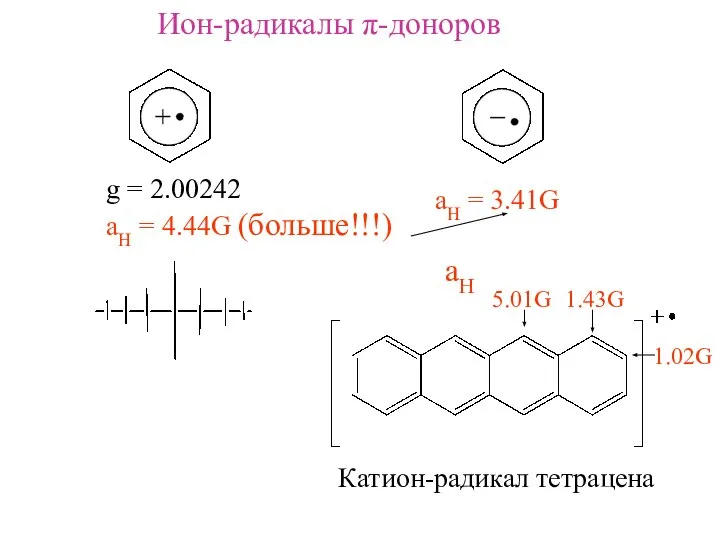
- 15. Ион-радикалы π-доноров g = 2.00242 aH = 4.44G (больше!!!) aH = 3.41G 1.43G 1.02G 5.01G aH
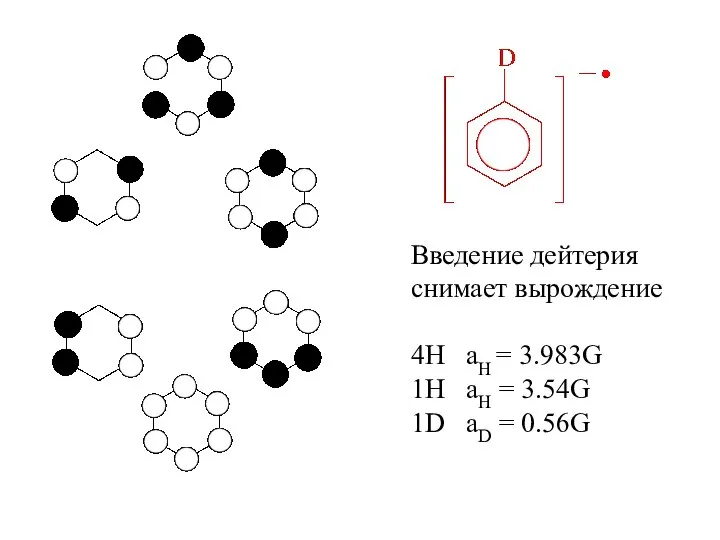
- 16. Введение дейтерия снимает вырождение 4H aH = 3.983G 1H aH = 3.54G 1D aD = 0.56G
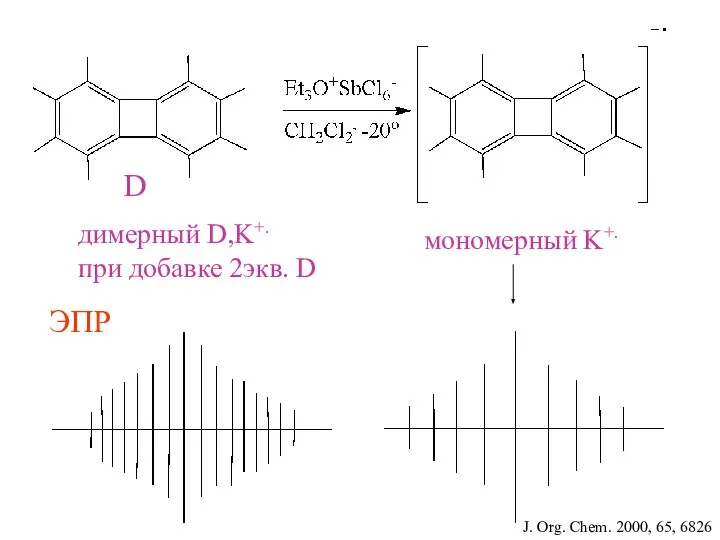
- 17. мономерный K+. димерный D,K+. при добавке 2экв. D D ЭПР J. Org. Chem. 2000, 65, 6826
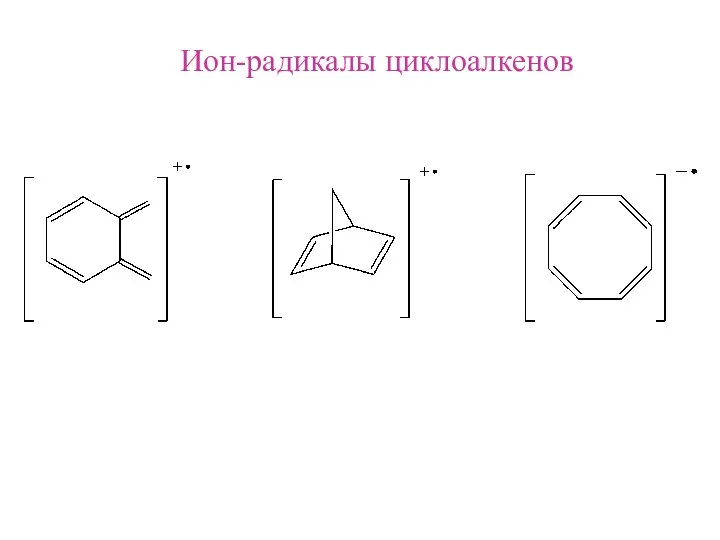
- 19. Ион-радикалы циклоалкенов
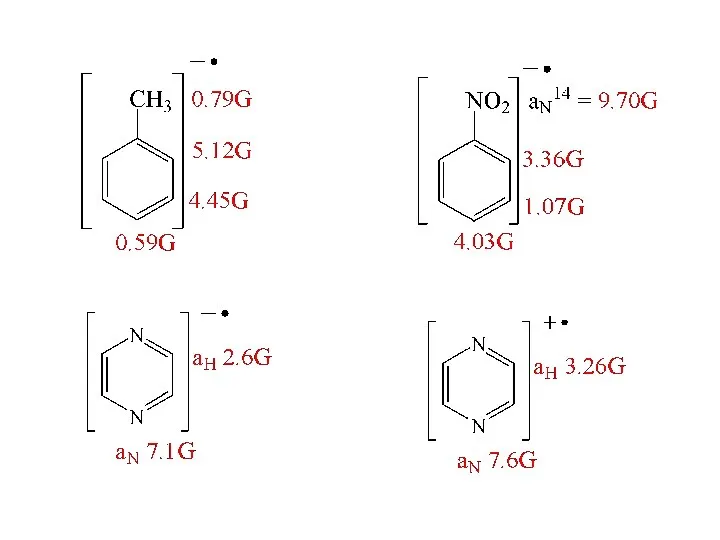
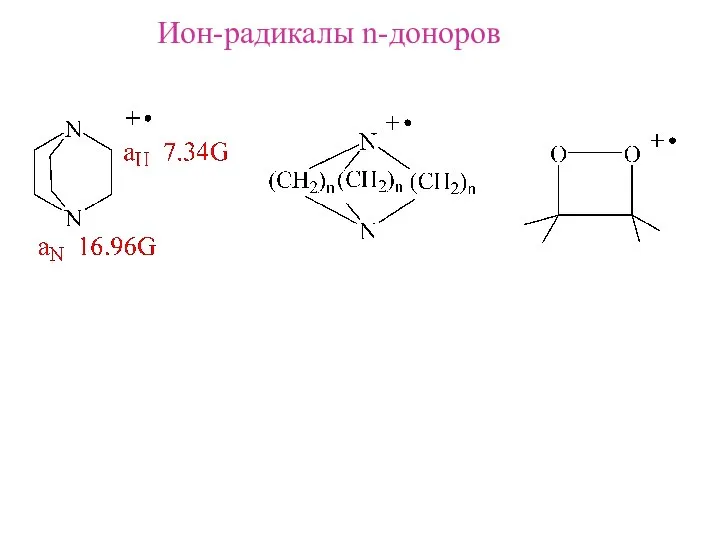
- 20. Ион-радикалы n-доноров
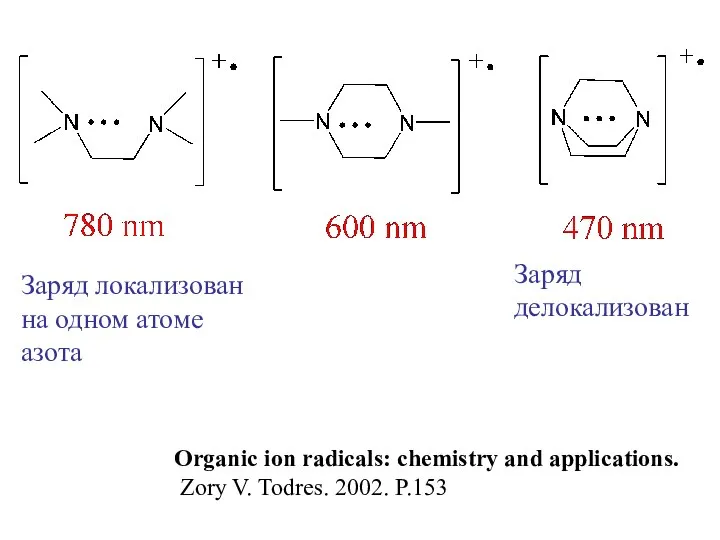
- 21. Заряд локализован на одном атоме азота Заряд делокализован Organic ion radicals: chemistry and applications. Zory V.
- 23. Скачать презентацию


![5. ЭСП характеризует разницу энергий занятых (или SOMO) и незанятых МО] 6.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/982242/slide-8.jpg)



 Алканы. Способы получения алканов. Химические свойства алканов
Алканы. Способы получения алканов. Химические свойства алканов Первый закон термодинамики. Термохимия
Первый закон термодинамики. Термохимия Оптические свойства ювелирных камней. Цвет плеохроизм. Часть 1
Оптические свойства ювелирных камней. Цвет плеохроизм. Часть 1 Интеллектуальная игра по химии Металлы
Интеллектуальная игра по химии Металлы Новое в ЕГЭ. Химия
Новое в ЕГЭ. Химия Аминобензой қышқылы және оның туындыларының синтезі, өндіру әдісі және физика-химиялық қасиеттері
Аминобензой қышқылы және оның туындыларының синтезі, өндіру әдісі және физика-химиялық қасиеттері Планетарная модель атома и его строение
Планетарная модель атома и его строение Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Профессии, связанне с химией
Профессии, связанне с химией История чернил
История чернил Презентация на тему Применение солей в быту
Презентация на тему Применение солей в быту  Структура и функции нуклеиновых кислот
Структура и функции нуклеиновых кислот Косметические средства. Виды, состав и влияние на организм
Косметические средства. Виды, состав и влияние на организм Классификация и номенклатура ОС
Классификация и номенклатура ОС О некоторых удивительных удивительных свойствах свойствах веществ
О некоторых удивительных удивительных свойствах свойствах веществ Вторичная переработка нефти. Риформинг
Вторичная переработка нефти. Риформинг Реакции соединения и разложения
Реакции соединения и разложения Природа и типы химических связей
Природа и типы химических связей Химико-аналитический контроль
Химико-аналитический контроль Презентация на тему Менделеев Дмитрий Иванович
Презентация на тему Менделеев Дмитрий Иванович  Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Классификация спиртов
Классификация спиртов Производственно-торговая компания ООО СОЖ Синтез-Набережные Челны
Производственно-торговая компания ООО СОЖ Синтез-Набережные Челны Процессы растворения твёрдых веществ
Процессы растворения твёрдых веществ Классификация химических реакций
Классификация химических реакций Многогранность- моё второе имя. Задача
Многогранность- моё второе имя. Задача Решение задач «Биохимия клетки»
Решение задач «Биохимия клетки» Соединения галогенов
Соединения галогенов