Содержание
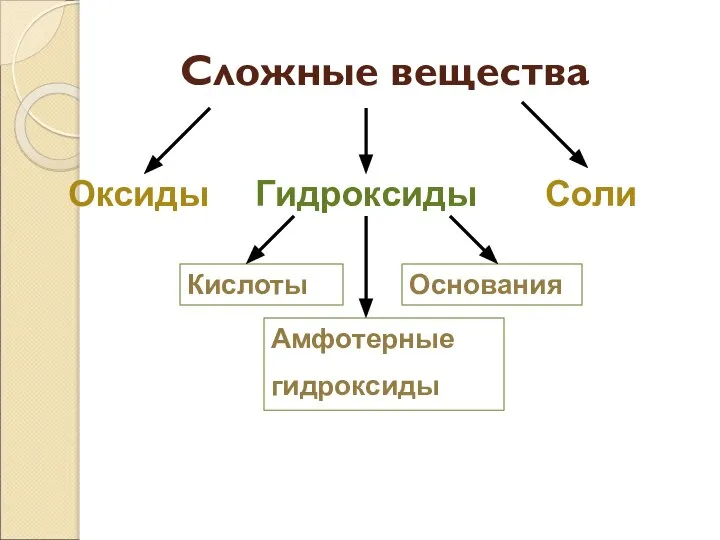
- 2. Сложные вещества Оксиды Гидроксиды Соли Кислоты Основания Амфотерные гидроксиды
- 3. Свойства оксидов и гидроксидов в периоде изменяются от основных через амфотерные к кислотным, т.к. увеличивается положительная
- 4. Гидроксиды Гидроксиды – это неорганические соединения, содержащие в составе гидроксильную группу (-ОН ) Общая формула: Э(ОН)n
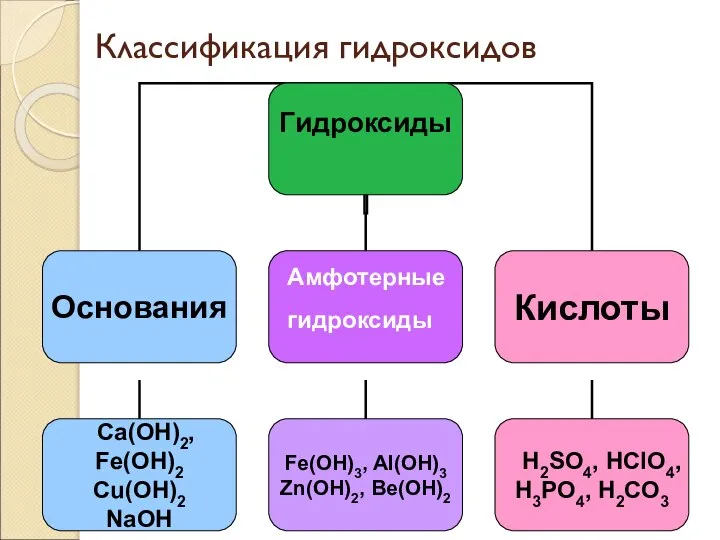
- 5. Амфотерные гидроксиды Классификация гидроксидов
- 6. Основания Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними одного или
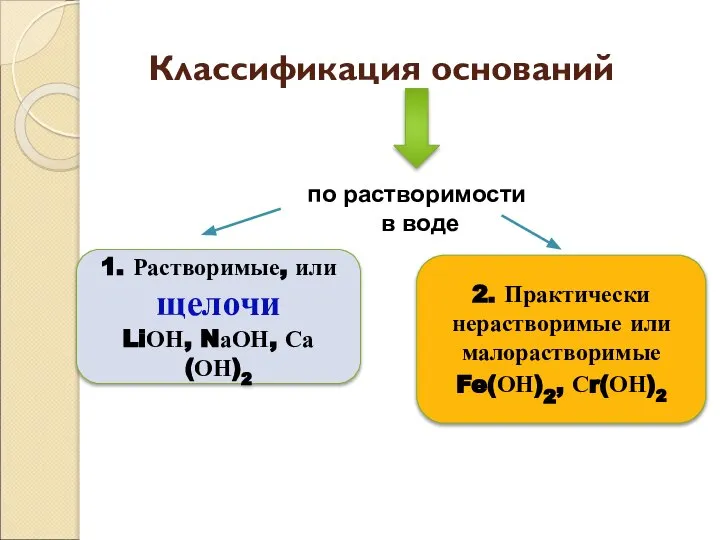
- 7. Классификация оснований по растворимости в воде 1. Растворимые, или щелочи LiОН, NаОН, Са(ОН)2 2. Практически нерастворимые
- 8. Основания. Гидроксиды щелочных металлов Общая формула – МеОН Щелочи. Белые кристаллические вещества, гигроскопичны, хорошо растворимы в
- 9. Гидроксиды металлов IIА группы Общая формула – Ме(ОН)2 Белые кристаллические вещества, в воде растворимы хуже, чем
- 10. Изменяют цвет индикаторов: Лакмус – на синий Фенолфталеин – на малиновый Метилоранж – на желтый Химические
- 11. 2. Взаимодействуют со всеми кислотами (реакция нейтрализации) NaOH + HCl → NaCl + H2O 3. Взаимодействуют
- 12. 5. Взаимодействуют с некоторыми неметаллами (серой, кремнием, фосфором) 2 NaOH +Si + H2O → Na2SiO3 +
- 13. Химические свойства нерастворимых оснований 1. Взаимодействуют с кислотами (реакция нейтрализации) Fe(OH) 2 + H2SO4 → FeSO4
- 14. Способы получения растворимых оснований (щелочей) 1. Взаимодействие щелочных и щелочно-земельных металлов их оксидов с водой 2Na
- 15. Способы получения нерастворимых оснований 2. Взаимодействие раствора щелочи с раствором соли 3NaOH + АlCl3 = Al(OH)3
- 16. Кислоты Кислоты – это сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков. При
- 17. Физические свойства кислот При обычных условиях кислоты могут быть жидкими и твердыми (борная, ортофосфорная, вольфрамовая) Кислоты
- 18. Классификация кислот
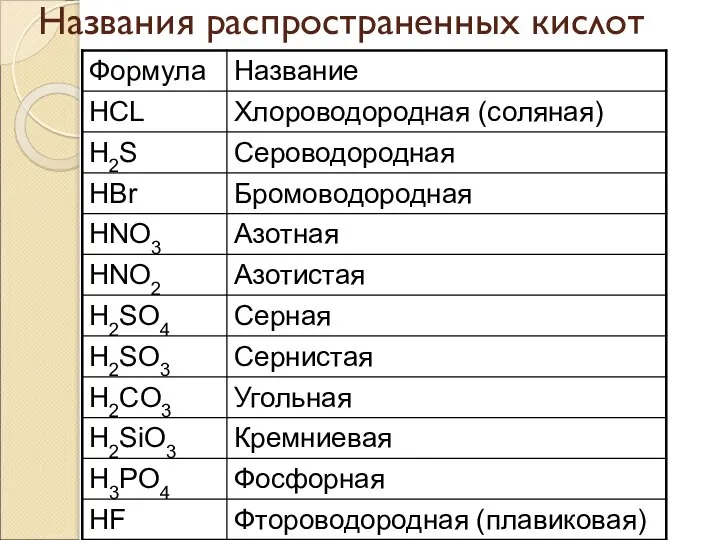
- 19. Названия распространенных кислот
- 20. Типичные реакции кислот 1. Кислота + основание = соль + вода H2SO4 +2 NaOH = Na2SO4
- 21. Типичные реакции кислот 3. Кислота + металл = водород + соль 2HCL +Zn = ZnCL2 +
- 22. Способы получения кислот 1. Взаимодействие кислотных оксидов с водой SO3 + H2O = H2SO4; CO2 +
- 23. Амфотерными называются гидроксиды , которые в зависимости от условий могут быть как донорами катионов водорода и
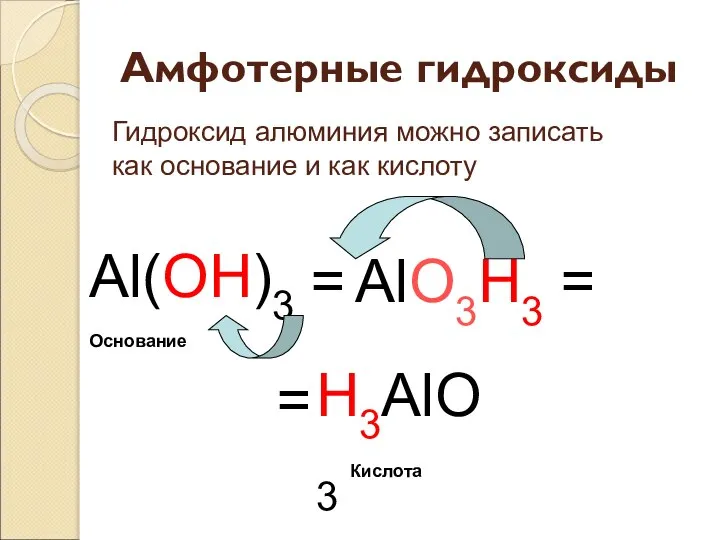
- 24. Амфотерные гидроксиды Al(OH)3 = H3AlO3 AlO3H3 = = Кислота Основание Гидроксид алюминия можно записать как основание
- 25. Некоторые гидроксиды с кислотно-основными свойствами:
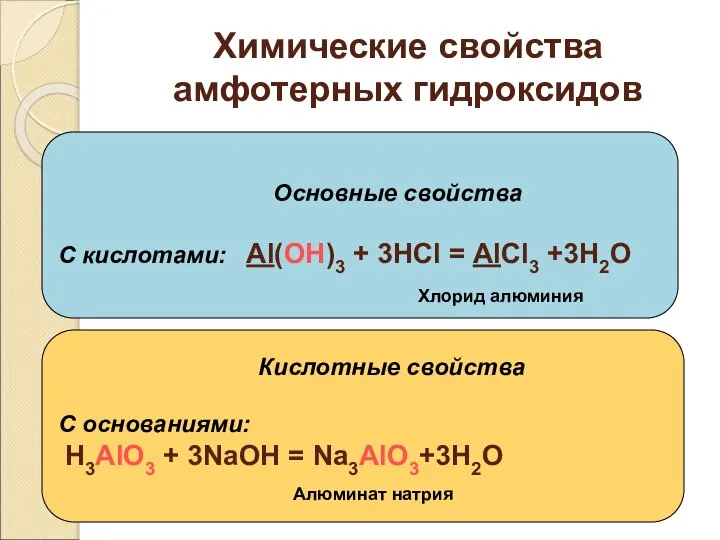
- 26. Химические свойства амфотерных гидроксидов Основные свойства С кислотами: Al(OH)3 + 3HCl = AlCl3 +3H2O Кислотные свойства
- 27. Способы получения амфотерных гидроксидов Осаждение разбавленной щёлочью из растворов солей соответствующего амфотерного элемента AlCl3 + NаOH
- 28. 1. Из предложенного перечня веществ выберите формулы гидроксидов,,, распределите их по классам и дайте им названия:
- 30. Скачать презентацию





















 Кремень. Нахождение в природе
Кремень. Нахождение в природе Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Презентация на тему Влияние пищевых добавок на здоровье человека
Презентация на тему Влияние пищевых добавок на здоровье человека  Общая характеристика МЕТАЛЛОВ
Общая характеристика МЕТАЛЛОВ Фосфор
Фосфор Хром (Cr)
Хром (Cr) Углеводороды. 9 класс
Углеводороды. 9 класс Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Химическое равновесие в гомогенных системах
Химическое равновесие в гомогенных системах Презентация на тему Угольная и кремниевая кислоты и их соли
Презентация на тему Угольная и кремниевая кислоты и их соли  Разложение отходов. 11 класс
Разложение отходов. 11 класс Свойства воды. СВФ
Свойства воды. СВФ Валентные возможности атомов элементов
Валентные возможности атомов элементов Классификация химических элементов
Классификация химических элементов Лекарственные средства – производные пиримидина
Лекарственные средства – производные пиримидина Substanță chimică
Substanță chimică Продолжение классификации
Продолжение классификации Роль химии в решении экологических проблем
Роль химии в решении экологических проблем Химические средства защиты растений
Химические средства защиты растений Азотная кислота
Азотная кислота Наука химия. Интеллектуальная игра. 5-8 класс
Наука химия. Интеллектуальная игра. 5-8 класс Литий
Литий Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Вода – уникальное вещество на планете Земля
Вода – уникальное вещество на планете Земля Химия и косметика
Химия и косметика Общая характеристика элементов VII группы главной подгруппы. Хлор
Общая характеристика элементов VII группы главной подгруппы. Хлор Кислоты
Кислоты Ионная связь. Вещества ионного ( немолекулярного) строения
Ионная связь. Вещества ионного ( немолекулярного) строения