Содержание
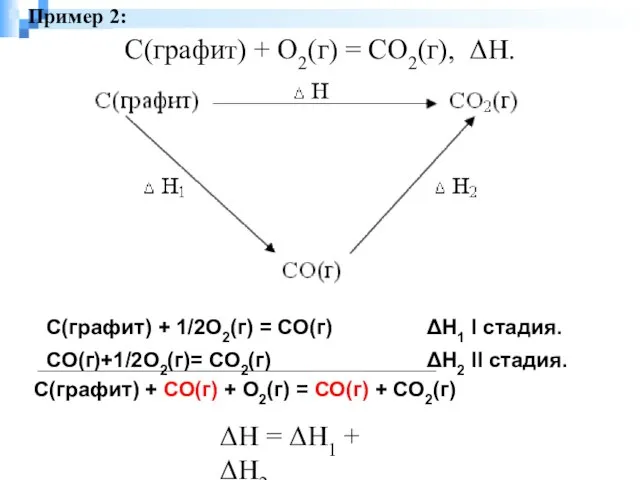
- 2. С(графит) + О2(г) = СО2(г), ΔН. ΔН = ΔН1 + ΔН2 Пример 2:
- 3. Пример 3: Рассчитайте тепловой эффект реакции горения аммиака: 4NН3 (г) + 3О2 (г) = 2N2 (г)
- 4. Пример 4:
- 5. Пример 5:
- 6. Пример 6: Гомогенные реакции: 2SO2(г) + O2(г) = 2SO3(г) υ = k ·c(SO2)2·c(O2) Гетерогенные реакции: С(тв)
- 7. Пример 7. Как изменится скорость реакции, протекающей в газовой фазе, если температуру уменьшить от 60°С до
- 8. Смещение химического равновесия Принцип Ле-Шателье При изменении внешних условий химическое равновесие смещается в сторону той реакции
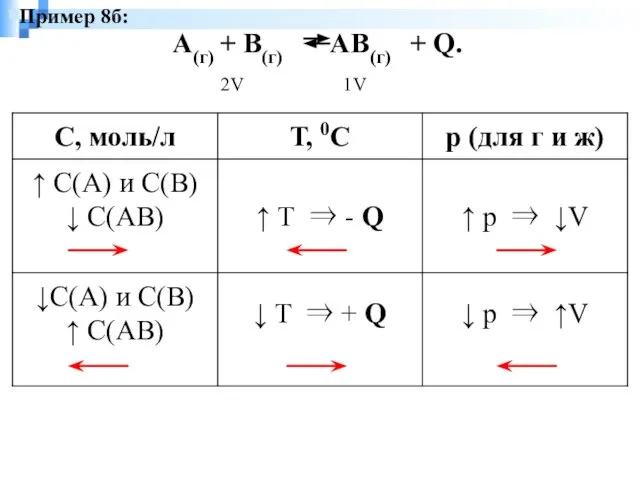
- 9. А(г) + В(г) АВ(г) + Q. 2V 1V Пример 8б:
- 11. Скачать презентацию






 Коррозия металлов
Коррозия металлов Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства Аммиак. Азот
Аммиак. Азот Статистика в аналитической химии
Статистика в аналитической химии Контроль якості імуногематологічних досліджень за допомогою діагностичних моноклональних реагентів та стандартних еритроцитів
Контроль якості імуногематологічних досліджень за допомогою діагностичних моноклональних реагентів та стандартних еритроцитів Относительный вклад % буферных систем крови в поддержание в ней протолитического гомеостаза
Относительный вклад % буферных систем крови в поддержание в ней протолитического гомеостаза Износостойкие стали и сплавы
Износостойкие стали и сплавы Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Алкадиены. Физические свойства
Алкадиены. Физические свойства Растворы. Лекция 7
Растворы. Лекция 7 Изучение геохимических свойств редкоземельных элементов
Изучение геохимических свойств редкоземельных элементов Кремний. Технический кремний
Кремний. Технический кремний Календарь юного химика. 2013-2014 учебный год
Календарь юного химика. 2013-2014 учебный год Обратимые и необратимые химические реакции. Химическое равновесие
Обратимые и необратимые химические реакции. Химическое равновесие Железо и его соединения
Железо и его соединения Магматические породы
Магматические породы Условия хранения и подготовка скоропортящихся грузов к перевозкам
Условия хранения и подготовка скоропортящихся грузов к перевозкам Тест по неметаллам
Тест по неметаллам строение атома
строение атома Алканы. Строение. Изомерия и номенклатура
Алканы. Строение. Изомерия и номенклатура Общие химические свойства неметаллов
Общие химические свойства неметаллов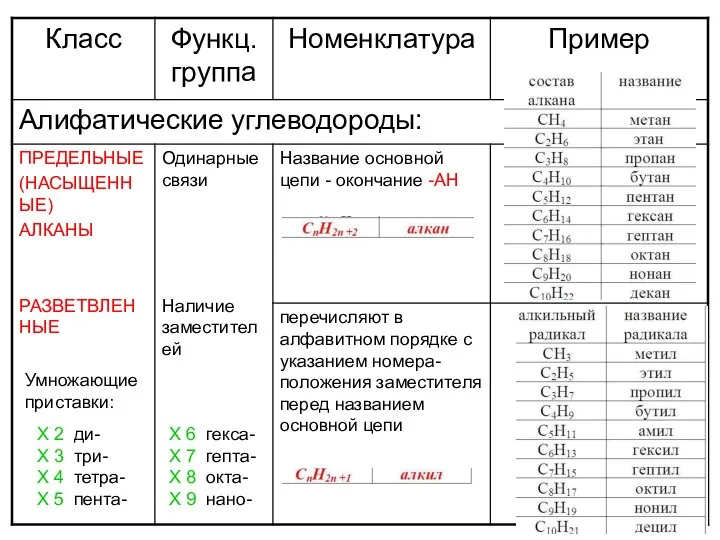 Алифатические углеводороды
Алифатические углеводороды Каких заданий не бывает на ЕГЭ по химии и почему
Каких заданий не бывает на ЕГЭ по химии и почему Сырье, продукты, параметры гидроочистки
Сырье, продукты, параметры гидроочистки Электронное и пространственное строение алкенов. Гомология и изомерия алкенов
Электронное и пространственное строение алкенов. Гомология и изомерия алкенов Решение задач. Подготовка к контрольной работе по химии
Решение задач. Подготовка к контрольной работе по химии Взаимодействие кислот с металлами. Кислоты-окислители
Взаимодействие кислот с металлами. Кислоты-окислители Реакция полимеризации
Реакция полимеризации