Содержание
- 2. Нахождение в природе В земной коре железо распространено достаточно широко. На его долю приходится: Около 4,1%
- 3. Соединения железа Fe3O4 – магнитный железняк Fe2O3 – красный железняк (гематит) 2Fe2O3 * 3H2O – бурый
- 4. Положение железа в Периодической системе химических элементов Д. И. Менделеева
- 5. Строение атома железа
- 6. Физические свойства железа Серебристо-серый металл, ковкий, пластичный, плотность 7,87г/см3; tпл.=1539°С; tкип.=2740°С; хорошо проводит тепло и электричество,
- 7. Fе3О4 + 4СО =3Fе + 4СО2 FеО + Н2 = Fе + Н2О Fе2О3 + 2Аl
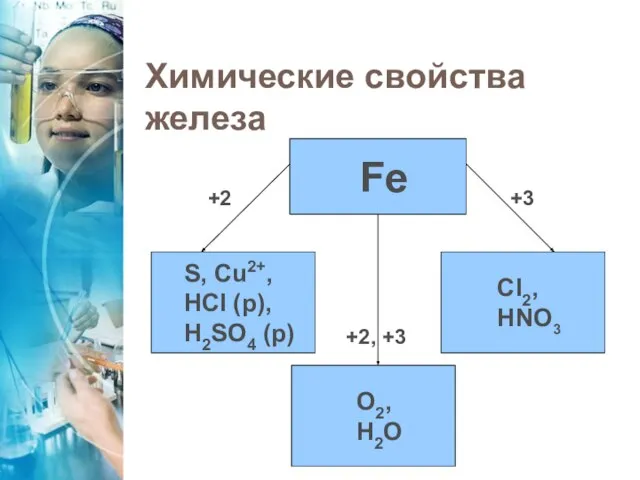
- 8. Химические свойства железа Fe S, Cu2+, HCI (р), H2SO4 (р) CI2, HNO3 O2, H2O +2 +3
- 9. Химические свойства железа
- 10. Химические свойства железа Взаимодействие железа с хлором 2Fe + 3Cl2 = 2FeCl3 https://www.youtube.com/watch?v=w6wc4PG0-es
- 11. Химические свойства железа Взаимодействие железа с кислородом 4Fe +3O2=2Fe2O3 https://www.youtube.com/watch?v=o9Rvc3Vae_c
- 12. Химические свойства железа Взаимодействия железа с серой Fe +S = FeS https://www.youtube.com/watch?v=jzEnZ6B7xNA
- 13. Химические свойства железа Реакции со сложными веществами С кислотами: А) с соляной кислотой 2HCl + Fe
- 14. Химические свойства железа Железо разрушается под действием окружающей среды, т.е. подвергается коррозии – «ржавлению». При этом
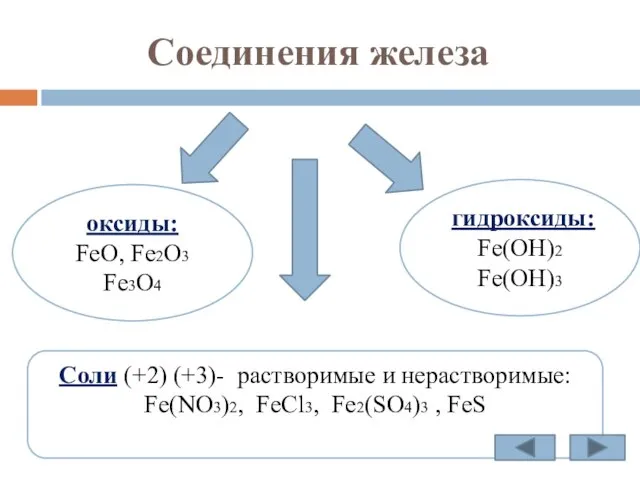
- 15. Соединения железа оксиды: FeO, Fe2O3 Fe3O4 гидроксиды: Fe(OH)2 Fe(OH)3 Соли (+2) (+3)- растворимые и нерастворимые: Fe(NO3)2,
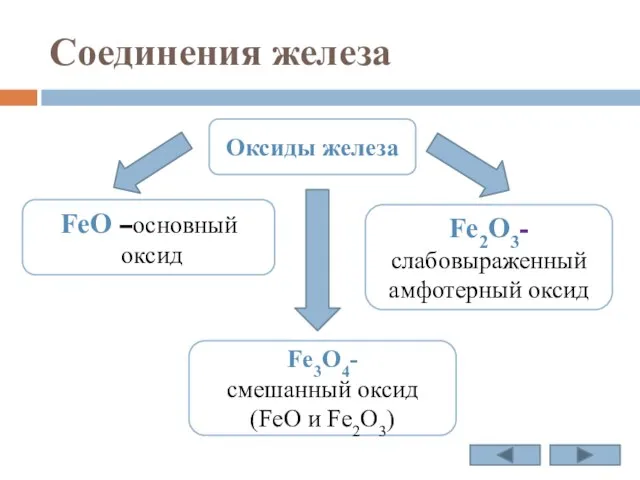
- 16. Соединения железа Оксиды железа FeO –основный оксид Fe3O4- смешанный оксид (FeO и Fe2O3) Fe2O3- слабовыраженный амфотерный
- 17. Соединения железа Химические свойства FeO 1) с кислотами: FeO + 2HCl=FeCl2 + H2O 2) с более
- 18. Соединения железа Химические свойства Fe3O4 1) с кислотами Fe3O4 + 8HCl=FeCl2 +2FeCl3 + 4H2O 2) также
- 19. Соединения железа Гидроксиды железа Fe(OH)2 Fe(OH)3
- 20. Соединения железа Fe(OH)2 и Fe(OH)3 1)Реагируют с кислотами: Fe(OH)2 + 2HNO3= Fe(NO3)2 + 2H2O Fe(OH)3 +
- 21. Качественные реакции на ионы Fe²⁺ и Fe³⁺ FeCl2 + 2NaOH=Fe(OH)2 +2NaCl Fe2+ +2Cl- + 2Na+ +
- 22. Качественные реакции на ионы Fe²⁺ На ион Fe2+ - взаимодействие с красной кровяной солью гексацианоферратом (III)калия
- 23. Качественные реакции на ионы Fe³⁺ FeCl3 + 3KSCN ? Fe(SCN)3 +3KCl роданид калия Fe+3CI3+3NH4SCN ? Fe(SCN)3↓+3NH4C
- 24. Биологическое значение железа Ионы железа входят в состав гемоглобина, который содержится в эритроцитах крови. Источники железа:
- 25. Применение Железо - самый употребляемый металл, на него приходится до 90 % мирового производства металлов. Железный
- 26. Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры
- 28. Скачать презентацию





















 Презентация на тему Синтетические материалы
Презентация на тему Синтетические материалы  Автомобильные бензины. Свойства топлив
Автомобильные бензины. Свойства топлив Вариативные задачи по химии различных типов в тестовой форме
Вариативные задачи по химии различных типов в тестовой форме Согласованное и несогласованное действие заместителей в бензольном кольце
Согласованное и несогласованное действие заместителей в бензольном кольце obschaya_kharakteristika_prostykh_alifaticheskikh_efirov
obschaya_kharakteristika_prostykh_alifaticheskikh_efirov Техника безопасности на уроках химии
Техника безопасности на уроках химии 11 типы связей
11 типы связей Химическая связь. Типы кристаллических решёток
Химическая связь. Типы кристаллических решёток Презентация на тему Хлор - физиологическая и патологическая роль в организме человека
Презентация на тему Хлор - физиологическая и патологическая роль в организме человека  Век медный, бронзовый, железный
Век медный, бронзовый, железный Ministry of Education and Science of the Russian Federation
Ministry of Education and Science of the Russian Federation Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Химические реакции
Химические реакции Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Физико-химические основы получения лекарственных препаратов
Физико-химические основы получения лекарственных препаратов Презентация по Химии "Углекислый газ"
Презентация по Химии "Углекислый газ"  Кислоты. Тест
Кислоты. Тест Основные классы неорганических веществ
Основные классы неорганических веществ Основы химической термодинамики
Основы химической термодинамики Молекулы и атомы. Относительная атомная масса
Молекулы и атомы. Относительная атомная масса 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Пищевые кислоты
Пищевые кислоты Минеральные вещества и здоровье
Минеральные вещества и здоровье Потенциометрический анализ, титрование
Потенциометрический анализ, титрование 4. Диаграмма железо-углерод
4. Диаграмма железо-углерод Минерал гранат
Минерал гранат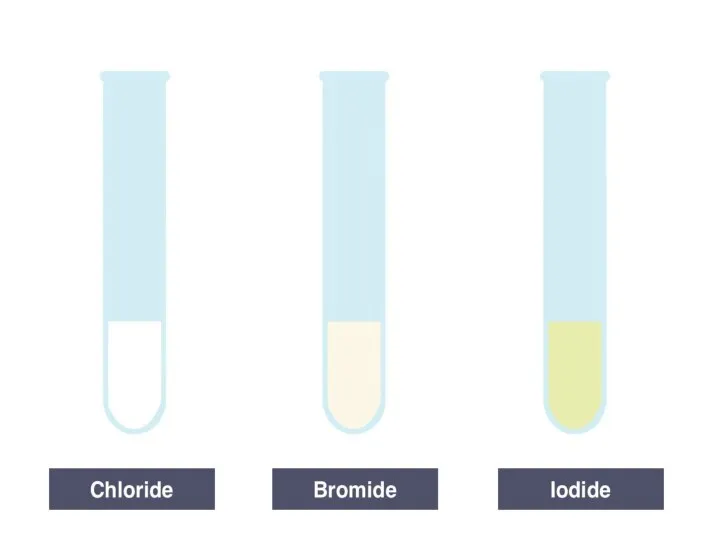 Определение галогенид-ионов в водном растворе. Лабораторный опыт
Определение галогенид-ионов в водном растворе. Лабораторный опыт Кислоты
Кислоты