Содержание
- 2. Комплексные соединения Комплексные соединения - наиболее обширный и разнообразный класс соединений. В живых организмах присутствуют комплексные
- 3. Комплексное соединение состоит из внутренней и внешней сферы. Центральная частица, вокруг которой расположены окружающие ее лиганды,
- 4. История открытия Соединения высшего порядка – так называл знаменитый шведский химик И.Я.Берцелиус (1779-1848) сложные многокомпонентные химические
- 5. Первым подобным соединением, синтезированным в лаборатории, является берлинская лазурь Fe4[Fe(CN)6]. Она была случайно получена художником Дисбахом
- 6. Комплексное соединение может состоять из комплексного катиона, комплексного аниона или может быть нейтральным. Соединения с комплексными
- 7. Вначале перечисляют лиганды анионные, затем нейтральные, затем катионные. Например, [Pt(NH3)5Cl]Cl3 – хлорид хлоропентаамминплатины (IV) . Если
- 8. Правило Сиджвика. (Правило эффективного атомного номера) Английский химик Н.-В. Сиджвик сформулировал эмпирическое правило, согласно которому «устойчивые
- 9. Однако часто наблюдаются отклонения от правила Сиджвика. Например, совершенно устойчивый мономерный ион [Рt(NНз)4] + имеет ЭАН,
- 10. Реакции образования комплексных соединений Комплексные соединения обычно получают действием избытка лигандов на содержащее комплексообразователь соединение. Координационное
- 11. Образование комплексных солей. Если комплексообразователем является Fe2+ или Fe3+, то координационные числа в обоих случаях равны
- 12. Координационные числа ртути и меди, как правило, равны четырем: Hg(NO3)2 + 4KI(изб) = K2[HgI4] + 2KNO3
- 13. Разрушение комплексных соединений происходит в результате: 1) образования малорастворимого соединения с комплексообразователем: [Cu(NH3)4]SO4 + Na2S =
- 14. 3) образования малодиссоциированного электролита: Na2[Zn(OH)4] + 4HCl(изб) = 2NaCl + ZnCl2 + 4H2O 4) действия любой
- 15. 5) нагревания некоторых комплексных соединений: [Cu(NH3)4]SO4 = CuSO4 + 4NH3↑ Na3[Al(OH)3] = Na3AlO3 + 3H2O 6)
- 17. Скачать презентацию



![Первым подобным соединением, синтезированным в лаборатории, является берлинская лазурь Fe4[Fe(CN)6]. Она была](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/890675/slide-4.jpg)

![Вначале перечисляют лиганды анионные, затем нейтральные, затем катионные. Например, [Pt(NH3)5Cl]Cl3 – хлорид](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/890675/slide-6.jpg)






![3) образования малодиссоциированного электролита: Na2[Zn(OH)4] + 4HCl(изб) = 2NaCl + ZnCl2 +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/890675/slide-13.jpg)
![5) нагревания некоторых комплексных соединений: [Cu(NH3)4]SO4 = CuSO4 + 4NH3↑ Na3[Al(OH)3] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/890675/slide-14.jpg)
 Учение о химических процессах. Лекция 3
Учение о химических процессах. Лекция 3 Жиры. Техническая переработка жиров
Жиры. Техническая переработка жиров Презентация на тему Химия в медицине
Презентация на тему Химия в медицине  Минеральные компоненты молока и молочных продуктов. Макроэлементы
Минеральные компоненты молока и молочных продуктов. Макроэлементы Технологические особенности никеля и никелевых сплавов
Технологические особенности никеля и никелевых сплавов Процесс электролиза
Процесс электролиза Основы химического анализа. Лекция 7
Основы химического анализа. Лекция 7 Биотит и тальк
Биотит и тальк Микроструктура железоуглеродистых сплавов в равновесном состоянии
Микроструктура железоуглеродистых сплавов в равновесном состоянии Великий кислород
Великий кислород Опыты с водой
Опыты с водой Презентация на тему Химические свойства металлов
Презентация на тему Химические свойства металлов  Вещества молекулярного и немолекулярного строения
Вещества молекулярного и немолекулярного строения Свойства растворов электролитов
Свойства растворов электролитов ЛК 2_окислительно-восстановительные процессы
ЛК 2_окислительно-восстановительные процессы Budowa pasmowa ciał stałych
Budowa pasmowa ciał stałych 5 группа элементов
5 группа элементов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Анализ стабильности экологических характеристик товарных дизельных топлив после перекачки
Анализ стабильности экологических характеристик товарных дизельных топлив после перекачки Решение задач ЕГЭ
Решение задач ЕГЭ Шуточные загадки Периодической системы химических элементов
Шуточные загадки Периодической системы химических элементов Равновесия в растворах электролитов. Окислительно-восстановительные реакции
Равновесия в растворах электролитов. Окислительно-восстановительные реакции Вымораживание воды
Вымораживание воды Тренажер. Химические свойства солей
Тренажер. Химические свойства солей хим связь
хим связь Агрегатные состояния веществ
Агрегатные состояния веществ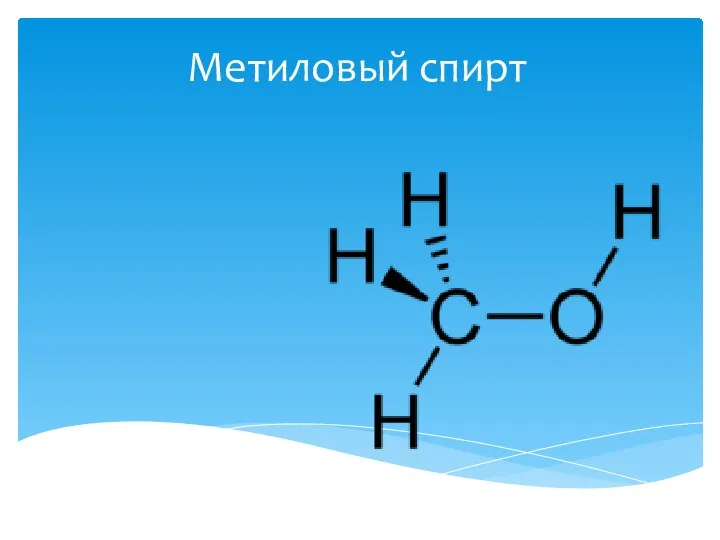 Метиловый спирт
Метиловый спирт Органическая химия и пищевые добавки
Органическая химия и пищевые добавки