Содержание
- 2. Определение Металлическая связь — химическая связь между атомами в металлическом кристалле, возникающая за счёт перекрытия (обобществления)
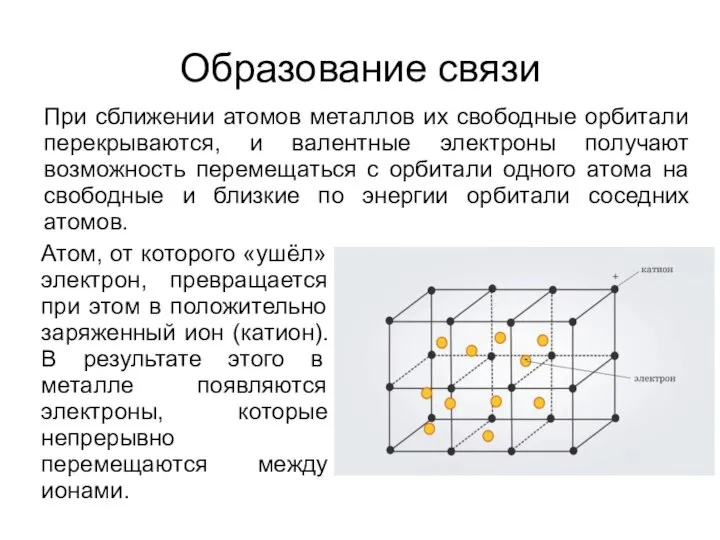
- 3. Атом, от которого «ушёл» электрон, превращается при этом в положительно заряженный ион (катион). В результате этого
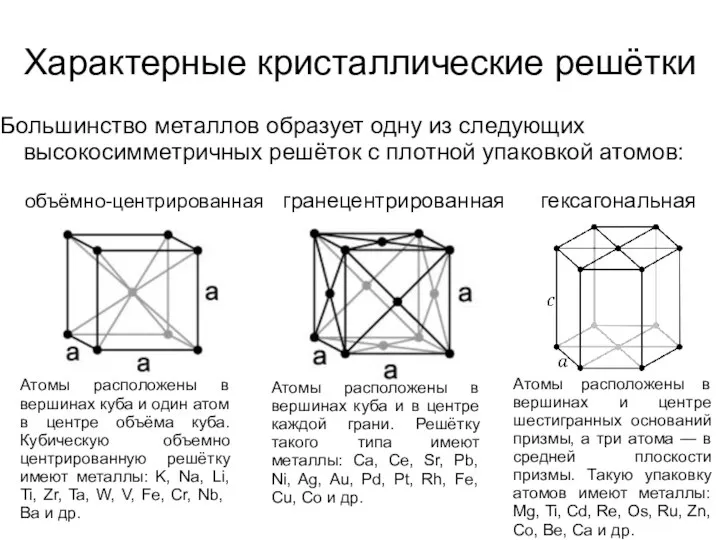
- 4. Характерные кристаллические решётки Большинство металлов образует одну из следующих высокосимметричных решёток с плотной упаковкой атомов: объёмно-центрированная
- 5. Свойства металлов Металлическая кристаллическая решётка и металлическая химическая связь определяют все наиболее характерные физические свойства металлов:
- 6. Свойства металлов Металлическая кристаллическая решётка и металлическая химическая связь определяют все наиболее характерные физические свойства металлов:
- 7. Твердость Твердость — это свойство материала сопротивляться внедрению более твёрдого тела. Все металлы (кроме ртути и,
- 8. Блеск Блеск (глянец) — оптическая характеристика свойства поверхности, отражающей свет, показывающая соотношение между интенсивностями света, зеркально
- 9. Цвет Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий
- 10. Пластичность Пластичность — важнейшее свойство металлов — выражается в их способности деформироваться под действием механической нагрузки.
- 11. Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Самыми пластичными являются
- 12. Температура плавления Температуры плавления чистых металлов лежат в диапазоне от −39 °C (ртуть) до 3410 °C
- 14. Скачать презентацию








 Великий кислород
Великий кислород Химическая термодинамика
Химическая термодинамика Оксиды, их классификация. Свойства оксидов в свете теории электролитической диссоциации
Оксиды, их классификация. Свойства оксидов в свете теории электролитической диссоциации Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Основания
Основания Химическая связь
Химическая связь Презентация на тему Целлюлоза
Презентация на тему Целлюлоза  каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами
каталитические системы на основе металлоценов и метилалюмоксана в реакциях непредельных соединений с изобутиланами Путешествие в мир кислот
Путешествие в мир кислот Ar, Mr
Ar, Mr Аэрированный сшитый полимерный раствор (АСПР)
Аэрированный сшитый полимерный раствор (АСПР) Кислород как вещество
Кислород как вещество Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Предмет органической химии. Теория химического строения органических веществ. 9 класс
Предмет органической химии. Теория химического строения органических веществ. 9 класс Окислительно-восстановительные реакции (ОВР). Лекция 1
Окислительно-восстановительные реакции (ОВР). Лекция 1 VVEDENIE_V_OGRANIChESKUYu_KhIMIYu
VVEDENIE_V_OGRANIChESKUYu_KhIMIYu Кислоты. 3 класс
Кислоты. 3 класс Научно-исследовательская деятельность учащихся в процессе изучения химии
Научно-исследовательская деятельность учащихся в процессе изучения химии Презентация на тему Нанотехнологии и Наноматериалы
Презентация на тему Нанотехнологии и Наноматериалы  Образование первичной структуры белка
Образование первичной структуры белка Кислоты. Начальные сведения
Кислоты. Начальные сведения Кислоты. 8 класс
Кислоты. 8 класс Углеродные материалы. Основные понятия и определения. Области их применения
Углеродные материалы. Основные понятия и определения. Области их применения Химический элемент Ferrum(2,3)
Химический элемент Ferrum(2,3) Структуры железоуглеродистых сплавов в равновесном состоянии
Структуры железоуглеродистых сплавов в равновесном состоянии Алканы
Алканы Презентация на тему Природный газ
Презентация на тему Природный газ  Презентация на тему Сплавы металлов (9 класс)
Презентация на тему Сплавы металлов (9 класс)