Содержание
- 2. Дать характеристику элементам IA группы по их положению в периодической системе химических элементов. На основе строения
- 3. Щелочные металлы
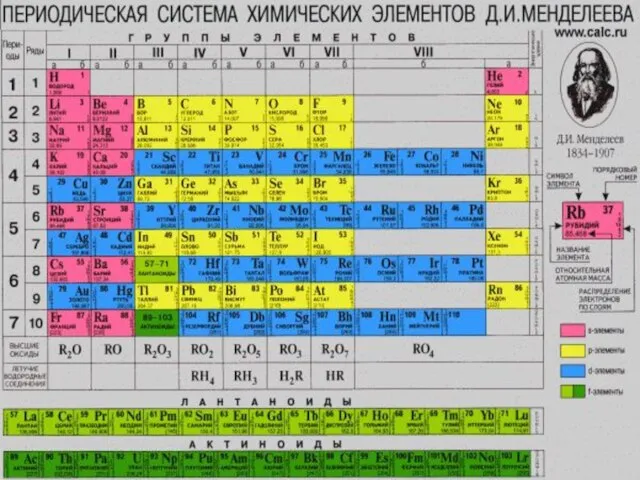
- 5. ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ I ГРУППЫ ГЛАВНОЙ ПОДГРУППЫ Li Na K Rb Cs Fr 7 23 39
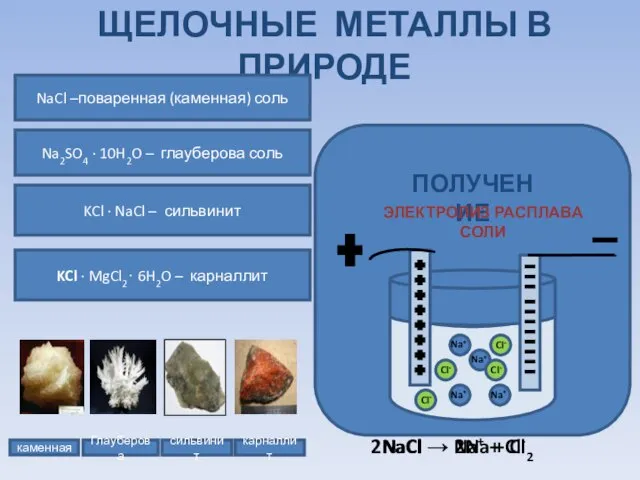
- 6. ЩЕЛОЧНЫЕ МЕТАЛЛЫ В ПРИРОДЕ каменная Глауберова сильвинит карналлит NaCl –поваренная (каменная) соль Na2SO4 ∙ 10H2O –
- 7. ФИЗИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ МЕТАЛЛИЧЕСКАЯ КРИСТАЛЛИЧЕСКАЯ РЕШЕТКА Вещества серебристо-белого цвета Электропроводны и теплопроводны Легкоплавкие. пластичные t
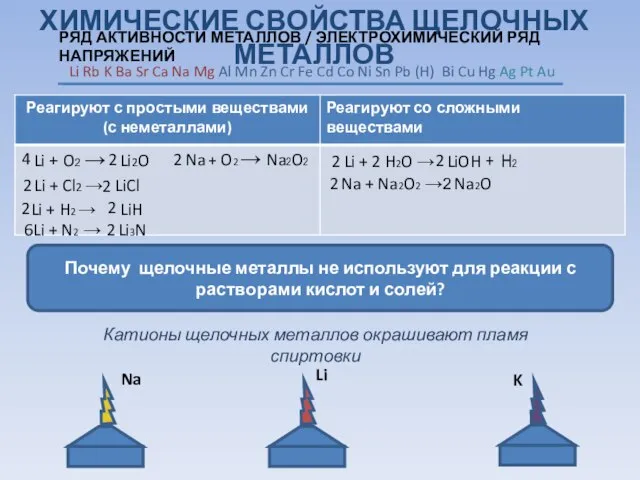
- 8. ХИМИЧЕСКИЕ СВОЙСТВА ЩЕЛОЧНЫХ МЕТАЛЛОВ Почему щелочные металлы не используют для реакции с растворами кислот и солей?
- 9. БИОЛОГИЧЕСКАЯ РОЛЬ И ПРИМЕНЕНИЕ СОЕДИНЕНИЙ КАЛИЯ И НАТРИЯ ответ ответ ответ NaCl Кристалли-ческая сода Na2CO3*10H2O Питьевая
- 10. Проверь себя: ☺ Вычеркните неверное суждение о щелочных металлах: 1. Число электронов на внешнем энергетическом уровне
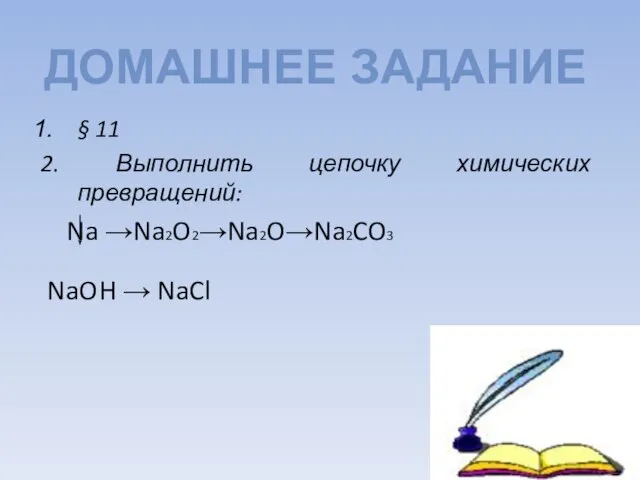
- 11. § 11 2. Выполнить цепочку химических превращений: Na →Na2O2→Na2O→Na2CO3 NaOH → NaCl ДОМАШНЕЕ ЗАДАНИЕ
- 12. СПАСИБО ЗА УРОК!!!
- 14. Скачать презентацию







 ОВР. Метод электронного баланса
ОВР. Метод электронного баланса Кислоты. Общая формула кислот
Кислоты. Общая формула кислот Презентация на тему Алюминий как химический элемент и как простое вещество
Презентация на тему Алюминий как химический элемент и как простое вещество  Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Предмет органической химии
Предмет органической химии Неметаллы
Неметаллы Химия. Соотечественники, внёсшие большой вклад в становление и развитие этой науки
Химия. Соотечественники, внёсшие большой вклад в становление и развитие этой науки Химические реакции
Химические реакции Водородная химическая связь
Водородная химическая связь Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи
Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи Тепловой эффект химических реакций
Тепловой эффект химических реакций Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов
Газоанализаторы. Измерительный прибор для определения качественного и количественного состава смесей газов Неметалічні елементи
Неметалічні елементи Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Неметаллы. Агрегатные состояния неметаллов
Неметаллы. Агрегатные состояния неметаллов Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения
Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения Процессы минералообразования
Процессы минералообразования Химическая связь и строение вещества
Химическая связь и строение вещества Фотохромные биоматериалы. Применение спиропирановых систем в медицине
Фотохромные биоматериалы. Применение спиропирановых систем в медицине Аналитическая химия
Аналитическая химия Неорганические вещества клетки. 10 класс
Неорганические вещества клетки. 10 класс Типы химических реакций. Решение примеров
Типы химических реакций. Решение примеров Основы радиохимии и радиологии
Основы радиохимии и радиологии Кислород и сера. Их положение в ПСХЭ. Значение и применение
Кислород и сера. Их положение в ПСХЭ. Значение и применение Основания
Основания Презентация на тему Самородки 9 класс
Презентация на тему Самородки 9 класс  Алкадиены. Строение. Гомологический ряд. Изомерия. Номенклатура
Алкадиены. Строение. Гомологический ряд. Изомерия. Номенклатура Окислительно-восстановительные реакции
Окислительно-восстановительные реакции