Содержание
Слайд 2 Корозійна стійкість бетону в розчинах кислот. Метод базуєть-
ся на вимірюванні швидкості хімічної
Корозійна стійкість бетону в розчинах кислот. Метод базуєть-
ся на вимірюванні швидкості хімічної

взаємодії кислоти з бетоном
при постійному занурюванні зразків бетону в розчин кислоти зада-
ної концентрації. Застосовують зразки-циліндри з бетонної суміші
заданого складу діаметром і висотою
50 або 100 мм при розмірі зерен крупного заповнювача відповідно
не більше 10 і 20 мм. Більш крупні зерна заповнювача видаляють.
Серія зразків включає 12 зразків-циліндрів.
Після набору бетоном проектної міцності в заданих умовах твер-
днення визначають його густину і відбраковують зразки, густина
Види корозії та Концентрація
показники агре-
сивності
Одини-
ці вимі-
ру основна допустима
Кислотна рН 3 4; 5
Вуглекисла, СО2 мг·л-1 80 40
Магнезіальна,
Mg2+ мг·л-1 10000 5000; 2000
Амонійна, NH4
+ мг·л-1 2000 1000; 500
Сульфатна, SO4
2- мг·л-1 10000 34000;3000; 1000
190
яких відрізняється від середньої більш ніж на ±50 кг/м3, а також
зразки які мають раковини і тріщини. Випробовують три зразки, на
бокові поверхні яких наносять ґрунтовку, шпаклівку і два шари по-
криття з епоксидного клею завтовшки не менше 0,3 мм. Шпаклівку
готують добавленням в епоксидний клей портландцементу до
2…3 мас.ч. Кожний зразок після висушування покриття встанов-
люють в окремий ексикатор, в який заливають розчин кислоти. Від-
ношення об’єму розчину в см3 до 1 см2 робочої поверхні зразка по-
винно бути не менше 50:1.
До випробувань і періодично в процесі випробувань методом
кислотно-основного титрування визначають концентрацію кисло-
ти. При зменшенні концентрації кислоти на (5±0,1)% порівняно з
початковою, розчин кислоти замінюють новим. Загальна тривалість
випробувань – 6 місяців. У перші 3 тижні проби розчину кислоти
відбирають і титрують щоденно, потім три рази в тиждень, після 3
місяців випробувань – два рази в тиждень.
Масу цементного каменю (г/см3) в перерахунку на СаО (РСаО),
яка прореагувала з кислотою розраховують за формулою:
при постійному занурюванні зразків бетону в розчин кислоти зада-
ної концентрації. Застосовують зразки-циліндри з бетонної суміші
заданого складу діаметром і висотою
50 або 100 мм при розмірі зерен крупного заповнювача відповідно
не більше 10 і 20 мм. Більш крупні зерна заповнювача видаляють.
Серія зразків включає 12 зразків-циліндрів.
Після набору бетоном проектної міцності в заданих умовах твер-
днення визначають його густину і відбраковують зразки, густина
Види корозії та Концентрація
показники агре-
сивності
Одини-
ці вимі-
ру основна допустима
Кислотна рН 3 4; 5
Вуглекисла, СО2 мг·л-1 80 40
Магнезіальна,
Mg2+ мг·л-1 10000 5000; 2000
Амонійна, NH4
+ мг·л-1 2000 1000; 500
Сульфатна, SO4
2- мг·л-1 10000 34000;3000; 1000
190
яких відрізняється від середньої більш ніж на ±50 кг/м3, а також
зразки які мають раковини і тріщини. Випробовують три зразки, на
бокові поверхні яких наносять ґрунтовку, шпаклівку і два шари по-
криття з епоксидного клею завтовшки не менше 0,3 мм. Шпаклівку
готують добавленням в епоксидний клей портландцементу до
2…3 мас.ч. Кожний зразок після висушування покриття встанов-
люють в окремий ексикатор, в який заливають розчин кислоти. Від-
ношення об’єму розчину в см3 до 1 см2 робочої поверхні зразка по-
винно бути не менше 50:1.
До випробувань і періодично в процесі випробувань методом
кислотно-основного титрування визначають концентрацію кисло-
ти. При зменшенні концентрації кислоти на (5±0,1)% порівняно з
початковою, розчин кислоти замінюють новим. Загальна тривалість
випробувань – 6 місяців. У перші 3 тижні проби розчину кислоти
відбирають і титрують щоденно, потім три рази в тиждень, після 3
місяців випробувань – два рази в тиждень.
Масу цементного каменю (г/см3) в перерахунку на СаО (РСаО),
яка прореагувала з кислотою розраховують за формулою:
Слайд 3Примітка. Знак "+" вказує на обов’язковість визначення; знак "(+)" – визначати додатково;
Примітка. Знак "+" вказує на обов’язковість визначення; знак "(+)" – визначати додатково;
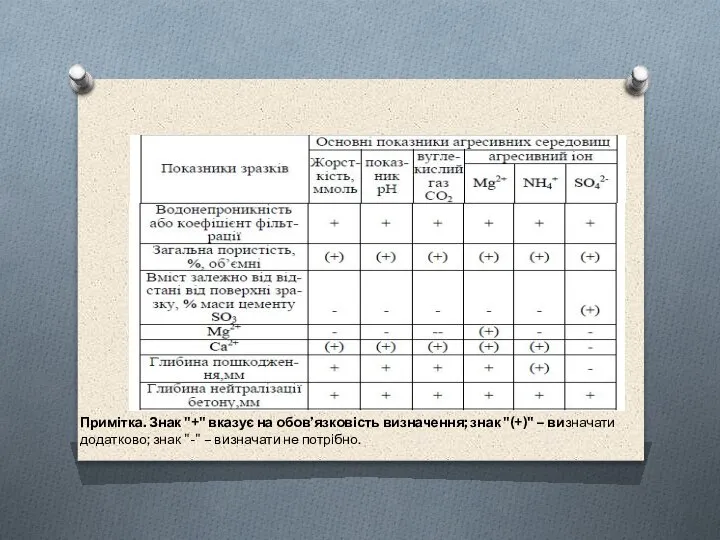
знак "-" – визначати не потрібно.
Слайд 4Таблиця 2
Таблиця 2

 Железо и его сплавы
Железо и его сплавы Вода. Общие сведения
Вода. Общие сведения Полимеры и пластмассы
Полимеры и пластмассы Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Кристаллогидраты
Кристаллогидраты Кислоты. 8 класс
Кислоты. 8 класс Презентация на тему В мире полимеров
Презентация на тему В мире полимеров  11. Дисперсные системы
11. Дисперсные системы Химическое равновесие. Экзаменационные вопросы
Химическое равновесие. Экзаменационные вопросы 8-11 2 валентность
8-11 2 валентность Анализ процесса гальванического нанесения рения. Поиск альтернативных способов нанесения рения
Анализ процесса гальванического нанесения рения. Поиск альтернативных способов нанесения рения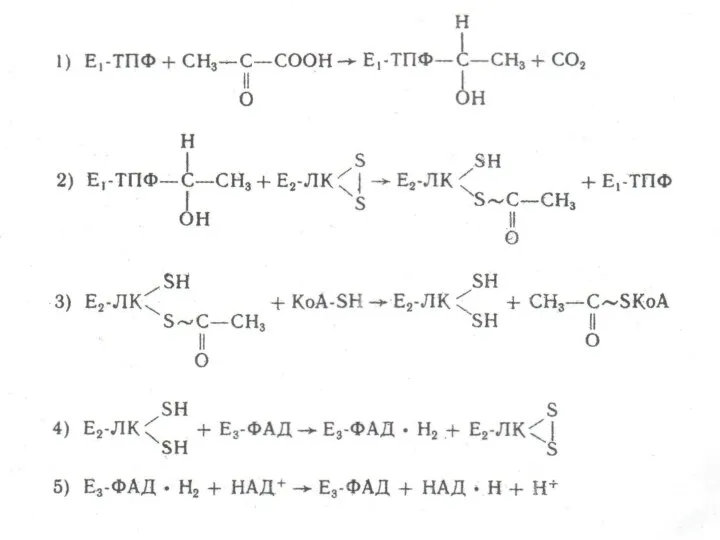 Схема интеграции пентозофосфатного шунта с гликолизом
Схема интеграции пентозофосфатного шунта с гликолизом Оценка пригодности природной воды в качестве питьевой по формуле М.Г. Курлова
Оценка пригодности природной воды в качестве питьевой по формуле М.Г. Курлова 1666603286718__4v20ts
1666603286718__4v20ts Металлы. Общая характеристика
Металлы. Общая характеристика Химическая посуда и лабораторное оборудование
Химическая посуда и лабораторное оборудование Химические равновесия в растворах. Лекция 2. Часть 1
Химические равновесия в растворах. Лекция 2. Часть 1 Способы получения металлов
Способы получения металлов Классификация неорганических соединений и реакций
Классификация неорганических соединений и реакций Кремнийорганическая гипотеза
Кремнийорганическая гипотеза 1-методы количественного анализа
1-методы количественного анализа Порох. Сера, халькогены
Порох. Сера, халькогены Синтетическое моторное масло. Маркировка моторных масел
Синтетическое моторное масло. Маркировка моторных масел Основы химической кинетики
Основы химической кинетики Винная кислота
Винная кислота Строение электронных оболочек атомов химических элементов
Строение электронных оболочек атомов химических элементов Пятичленные гетероциклы с двумя и более атомами азота
Пятичленные гетероциклы с двумя и более атомами азота Химическое равновесие. Протолитические равновесия и процессы в растворах электролитов
Химическое равновесие. Протолитические равновесия и процессы в растворах электролитов