Слайд 2Часть 3. Определение формулы вещества по химическим свойствам.

Слайд 33–1. Определить формулу алкена, если известно, что он 5,6 г его при присоединении

воды образуют 7,4 г спирта.
Слайд 43–2. Для окисления 2,9 г предельного альдегида до кислоты потребовалось 9,8 г гидроксида

меди (II). Определить формулу альдегида.
Слайд 53–3. Одноосновная моноаминокислота массой 3 г с избытком бромоводорода образует 6,24 г соли.

Определить формулу аминокислоты.
Слайд 63–4. При взаимодействии предельного двухатомного спирта массой 2,7 г с избытком калия выделилось

0,672 л водорода. Определить формулу спирта.
Слайд 73–5. (ЕГЭ–2011) При окислении предельного одноатомного спирта оксидом меди (II) получили 9,73 г

альдегида, 8,65 г меди и воду. Определить молекулярную формулу этого спирта.
Слайд 8
Ответы и комментарии к задачам для самостоятельного решения.
3–1. С4Н8
3–2. С3Н6О
3–3. С2Н5NO2
3–4. C4H8(OH)2
3–5.

C4H9OH
Слайд 9Источники
http://ege-study.ru/materialy-ege/ximiya-chast-s-zadacha-s5-opredelenie-formul-organicheskix-veshhestv/









 Пластмассы
Пластмассы ВКР: Определение показателей качества мясной и колбасной продукции различных производителей
ВКР: Определение показателей качества мясной и колбасной продукции различных производителей Галогенопроизводные углеводородов
Галогенопроизводные углеводородов Реакции ионного обмена, гидролиз солей
Реакции ионного обмена, гидролиз солей Протолитическая теория кислот и оснований. Буферные растворы
Протолитическая теория кислот и оснований. Буферные растворы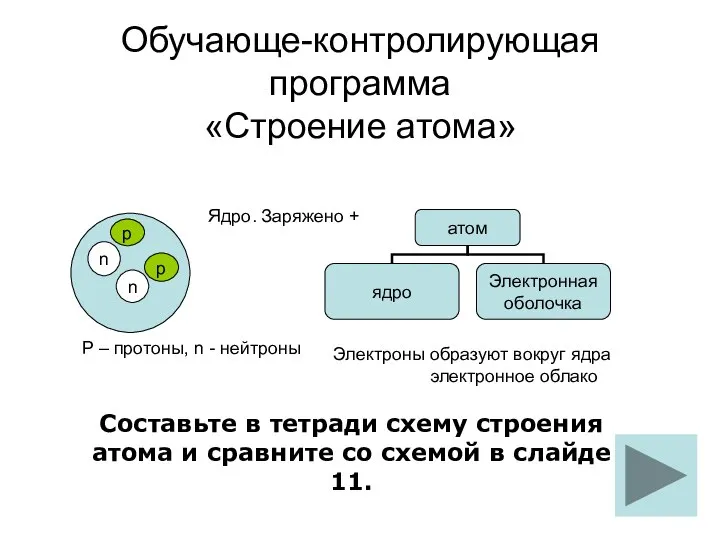 строение атома обуч-контр прогр
строение атома обуч-контр прогр Транспорт веществ
Транспорт веществ Коррозия металла
Коррозия металла Алкадиены: строение, номенклатура, гомологи, изомерия
Алкадиены: строение, номенклатура, гомологи, изомерия Кислород
Кислород Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Молекулярно-механическое изнашивание
Молекулярно-механическое изнашивание Классификация и номенклатура ОС
Классификация и номенклатура ОС Посвящение в химики
Посвящение в химики 1399920
1399920 Приемы разделения мембранных липидов на классы
Приемы разделения мембранных липидов на классы Фторсодержащие полимеры
Фторсодержащие полимеры Реакция нейтрализации
Реакция нейтрализации Застосування рідких кристалів
Застосування рідких кристалів Интеллектуальная игра По страницам истории химии
Интеллектуальная игра По страницам истории химии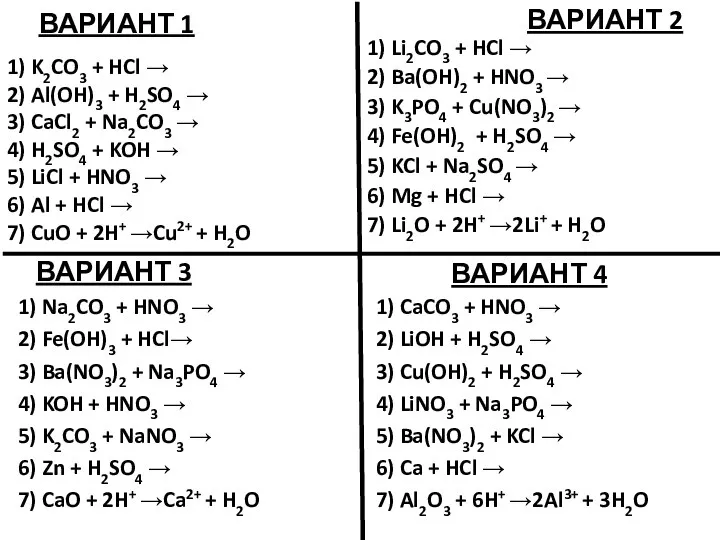 Уравнения возможных реакций. Задание
Уравнения возможных реакций. Задание Презентация по Химии "Углекислый газ"
Презентация по Химии "Углекислый газ"  Nevarne snovi
Nevarne snovi Качественные реакции в химии
Качественные реакции в химии Композитные материалы
Композитные материалы Анилин. Строение и свойства анилина
Анилин. Строение и свойства анилина Тест по химии
Тест по химии Вспоминаем химию
Вспоминаем химию