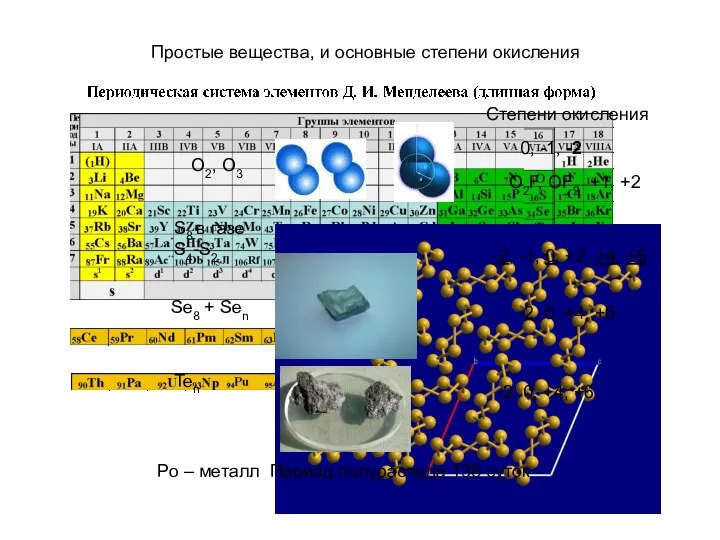
Содержание
- 3. O2, O3 Степени окисления 0, -1, -2 O2F, OF2 +1, +2 S8 в газе S4-S2 -2,
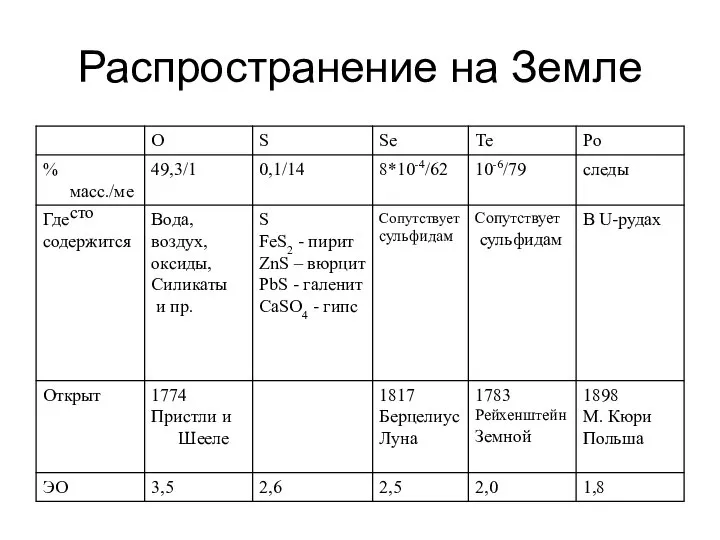
- 4. Распространение на Земле
- 5. Кислород получение Промышленное Фракционная перегонка жидкого воздуха Электролиз воды Применение Металлургия, получение стали Космические программы Химическая
- 6. Лабораторные способы получения Термическое разложение солей 2KMnO4 = K2MnO4 + MnO2 + O2 KClO3 = KCl
- 7. Хранение кислорода
- 8. Свойства Кислород окислитель!!! Сильный!!! O2 + 4H+ + 4e = 2H2O ΔE°=1.23В O3 + 2H+ +
- 10. Скачать презентацию





 Развитие познавательной активности творческих способностей и индивидуализация на уроках химии
Развитие познавательной активности творческих способностей и индивидуализация на уроках химии Углеродистые стали
Углеродистые стали Целестин
Целестин Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год
Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год Гальванический элемент
Гальванический элемент Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Степень окисления. Классификация неорганических соединений
Степень окисления. Классификация неорганических соединений Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Органическая химия
Органическая химия Соединения азота в атмосфере. Лекция 4
Соединения азота в атмосфере. Лекция 4 Структура к свойства веществ
Структура к свойства веществ Химические вещества парабены
Химические вещества парабены Влияние меди на коррозию низколегиованных сталей
Влияние меди на коррозию низколегиованных сталей Серная кислота
Серная кислота Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров Окислители в пиросоставах
Окислители в пиросоставах Вода. Строение молекулы. Водородная связь. Физические и химические свойства
Вода. Строение молекулы. Водородная связь. Физические и химические свойства Презентация на тему Гидролиз
Презентация на тему Гидролиз  Электролиз
Электролиз Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Основания и их свойства
Основания и их свойства Презентация на тему Многоатомные спирты
Презентация на тему Многоатомные спирты  Жидкое состояние вещества
Жидкое состояние вещества Поделочный камень родонит
Поделочный камень родонит Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора
Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Получение металлов
Получение металлов Степени окисления
Степени окисления