Содержание
- 2. Проверка. Ответы: 1 вариант HCl 2HCl + BaCO3 = BaCl2 + CO2+ H2O 2H+ +2Cl- +
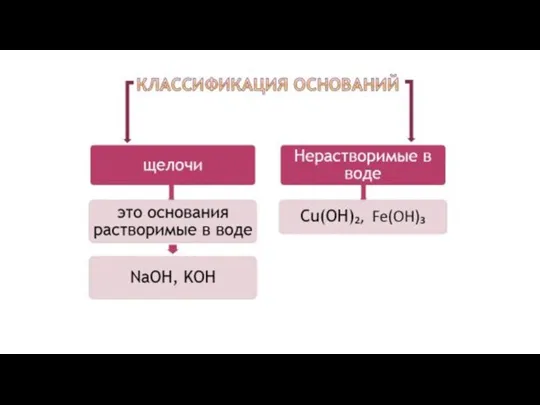
- 3. Основания (гидроксиды) Основания – электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы ОН-
- 4. Номенклатура оснований (правила составления химических названий) Пример: NaOH – гидроксид (чего?) натрия Fe2+ (OH)2 – гидроксид
- 5. Тривиальные названия (разговорные) NaOH Гидроксид натрия Едкий натр, Каустическая сода KOH Гидроксид калия Едкое кали
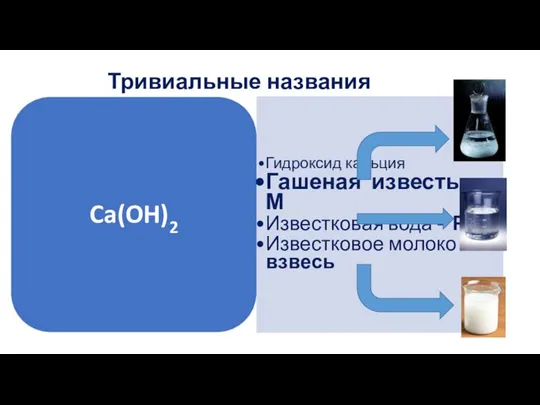
- 6. Тривиальные названия Ca(OH)2 Гидроксид кальция Гашеная известь – М Известковая вода – Р Известковое молоко -
- 8. Выполнить задания Карточка 2
- 9. Ответы Карточка 2 Распознать основания: 1. CH3OH 2. CrPO4 3. H2SiO3 4. CsOH
- 10. Ответы 2. Составить формулы оснований, образованных следующими металлами, назвать их: К - KOH Al - Al(OH)3
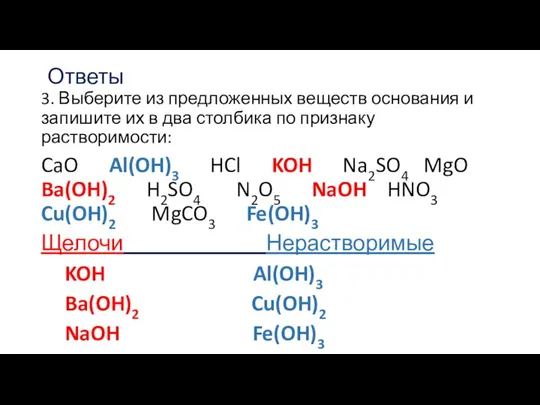
- 11. Ответы 3. Выберите из предложенных веществ основания и запишите их в два столбика по признаку растворимости:
- 12. ОБЖ щелочи Разъедают кожу и слизистые ткани Все работы проводить в очках и резиновых перчатках При
- 13. Химические свойства оснований. 1 задание: Прилить к р-ру КOH + р-р фенолфталеина 1) свойство: 2 задание:
- 14. Запись в тетради: 1 свойство: изменяет окраску индикатора KOH + фенолфталеин = малиновый цвет раствора Почему?
- 15. 2. Написать уравнение реакции Cu(OH)2 + HNO3→ В чем суть реакции? Какие ионы «встретились»?
- 16. 3. Написать уравнение реакции NaOH + Zn(NO3)2 → В чем суть реакции? Какие ионы «встретились»?
- 17. Кислотные оксиды – им соответствуют кислоты N2O5 СO2
- 18. 4) свойство: Щелочь + Кислотный оксид = Соль + Вода (оксид неметалла) - это реакция обмена
- 19. Сначала под формулой кислотного оксида пишем формулу соответствующей кислоты. NaOH + N2O5 = (HNO3) азотная кислота
- 20. Cu(OH)2 = CuO + H2O 5) свойство: нерастворимые основания разлагаются при нагревании
- 21. Какие ионы определяют свойства растворов оснований?
- 22. 5. Написать уравнение реакций разложения Fe(OH)3 = Zn(OH)2 =
- 23. Получение оснований просмотр: mmlab.chemistry.527.oms
- 25. Скачать презентацию


















 Производство серной кислоты
Производство серной кислоты Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Вода. Растворы
Вода. Растворы Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Соли
Соли Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Металлы побочных подгрупп
Металлы побочных подгрупп Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Химический элемент кислород
Химический элемент кислород Химическая география чудес природы
Химическая география чудес природы Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1) Презентация по Химии "Схема получения моноизотопного кремния"
Презентация по Химии "Схема получения моноизотопного кремния"  Посвящение в химики
Посвящение в химики Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты)
Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты) Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Общая характеристика оксидов
Общая характеристика оксидов Серная кислота
Серная кислота Основные понятия химии
Основные понятия химии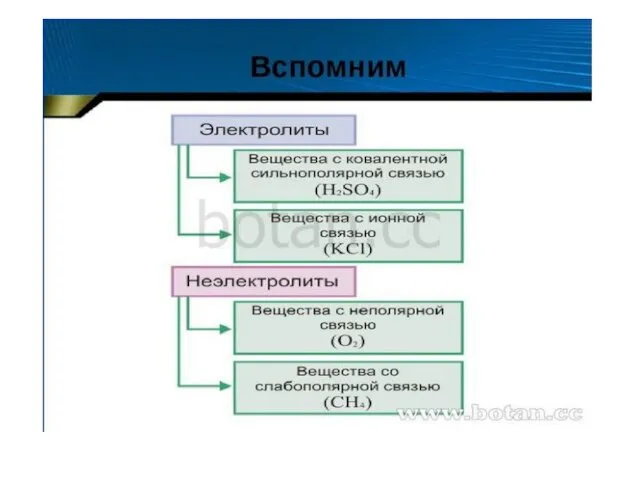 Диссоциация веществ
Диссоциация веществ Химическая связь и ее типы
Химическая связь и ее типы Соли. Химические свойства
Соли. Химические свойства Соль. Добыча соли
Соль. Добыча соли Металлы. Атомы металлов
Металлы. Атомы металлов Природные источники углеводорода
Природные источники углеводорода Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас