Слайд 2Комментарии по ДЗ
Ca+2HCl=CaCl2+H2
Fe+2HBr=FeBr2+H2
H3PO3 соответствует оксид Р2О3

Слайд 3Комментарии по ДЗ
MnO2 не реагирует с водой, как и CuO, Al2O3

Слайд 4Комментарии по ДЗ
Реакция между NO2 и ZnO не приведет к образованию Zn(NO3)2
ZnO+N2O5=Zn(NO3)2

Слайд 5Repetitio est mater studiorum

Слайд 6Бескислородным основанием является аммиак NH3
При растворении в воде он образует неустойчивый гидрат

NH3*H2O, который по свойствам во многом похож на типичные основания
Основания делят на 2 большие группы: растворимые и нерастворимые
Растворимые основания(щелочи) – гидроксиды подгруппы Лития и Кальция + гидрат аммиака
Нерастворимые – все остальные
Есть несколько неустойчивых оснований, которые самопроизвольно разлагаются даже без нагревания:
Слайд 8Химические свойства оснований

Слайд 13Аммиак растворяет гидроксиды некоторых металлов – Cu, Zn – за счет образования

устойчивых комплексов
Слайд 14Разложение при нагревании
2LiOH=Li2O+H2O

Слайд 17Равновесия в растворах электролитов
Константа диссоциации:

Слайд 22Расчеты pH растворов кислот
Уравнение материального баланса
Уравнение электронейтральности




























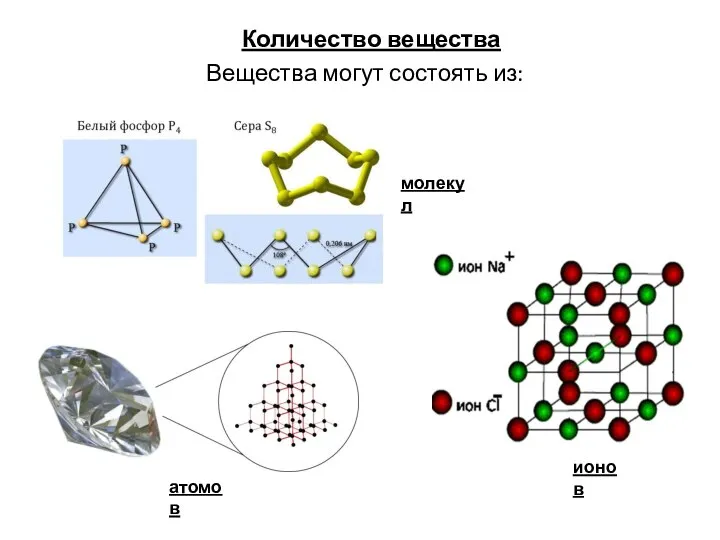 Количество вещества
Количество вещества Кислоты в химии
Кислоты в химии Алкадиены. Строение. свойства и применение
Алкадиены. Строение. свойства и применение Малотоннажные термопласты
Малотоннажные термопласты Органика из аптеки
Органика из аптеки Три секрета прочности волокнистых композитов
Три секрета прочности волокнистых композитов Определение качества дизельного топлива
Определение качества дизельного топлива Строение атома в ЭЖ (1)
Строение атома в ЭЖ (1) Основания, их классификация и свойства в свете теории электролитической диссоциации
Основания, их классификация и свойства в свете теории электролитической диссоциации Характеристика кислорода и серы
Характеристика кислорода и серы Химические реакции
Химические реакции Предельные одноосновные карбоновые кислоты. Сложные эфиры
Предельные одноосновные карбоновые кислоты. Сложные эфиры Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Кислоты
Кислоты Классификация органических соединений
Классификация органических соединений Каскадный синтез пептидов
Каскадный синтез пептидов Халькогены. Электронное строение кислорода и серы
Халькогены. Электронное строение кислорода и серы Химия в быту
Химия в быту Презентация Повторение к СОЧ-10 кл (1)
Презентация Повторение к СОЧ-10 кл (1) Органическая химия. Подготовка к экзамену
Органическая химия. Подготовка к экзамену Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Презентация на тему Производство стекла
Презентация на тему Производство стекла  Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Химическое равновесие
Химическое равновесие Применение неметаллов
Применение неметаллов Тепловой эффект химических реакций
Тепловой эффект химических реакций Проект по химии. Минералы на нашей коже
Проект по химии. Минералы на нашей коже Основные классы неорганических соединений
Основные классы неорганических соединений