Содержание
- 2. ПРЕДМЕТ БИООРГАНИЧЕСКОЙ ХИМИИ БИООРГАНИЧЕСКАЯ ХИМИЯ ИЗУЧАЕТ СТРОЕНИЕ, СВОЙСТВА, ПРЕВРАЩЕНИЯ, БИОЛОГИЧЕСКИЕ ФУНКЦИИ И ПРИМЕНЕ-НИЕ БИООРГАНИЧЕСКИХ СОЕДИНЕНИЙ БИООРГАНИЧЕСКИЕ
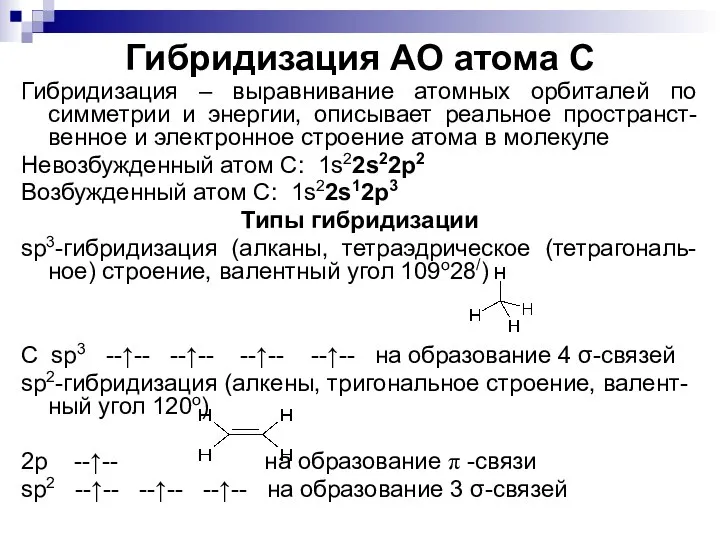
- 3. Гибридизация АО атома С Гибридизация – выравнивание атомных орбиталей по симметрии и энергии, описывает реальное пространст-венное
- 4. Сопряжение. Сопряженные системы Сопряженные системы – молекулы (или их фрагменты) определенного строения, обладающие характерным комплексом физико-химических
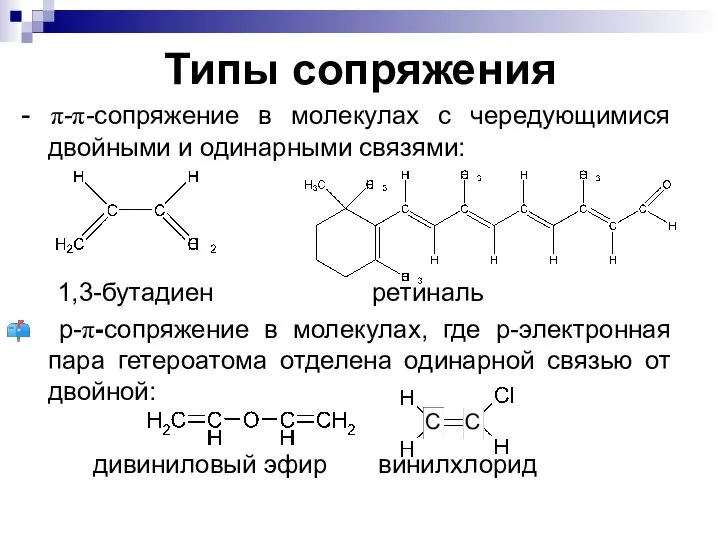
- 5. Типы сопряжения - π-π-сопряжение в молекулах с чередующимися двойными и одинарными связями: 1,3-бутадиен ретиналь р-π-сопряжение в
- 6. Ароматичность. Ароматические соединения Ароматические соединения – циклические сопряженные молекулы, подчиняющиеся критериям ароматичности и обладающие характерным комплексом
- 7. Критерии ароматичности - циклическая сопряженная система без разрывов сопряжения; - плоский цикл; число π - и
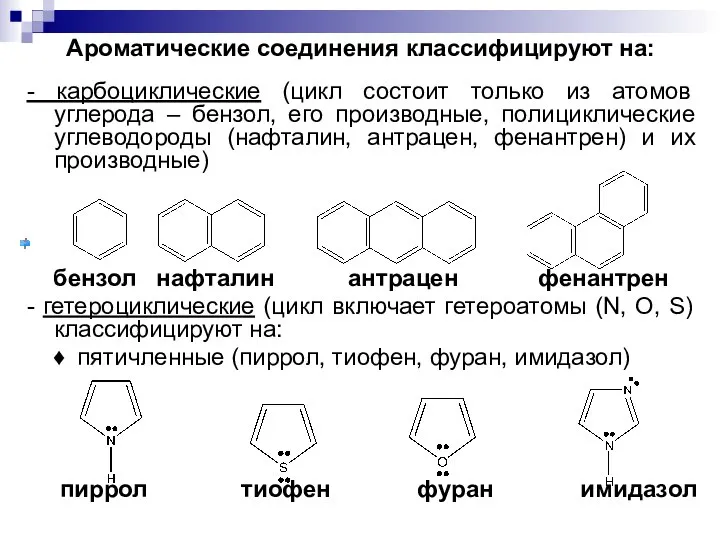
- 8. Ароматические соединения классифицируют на: - карбоциклические (цикл состоит только из атомов углерода – бензол, его производные,
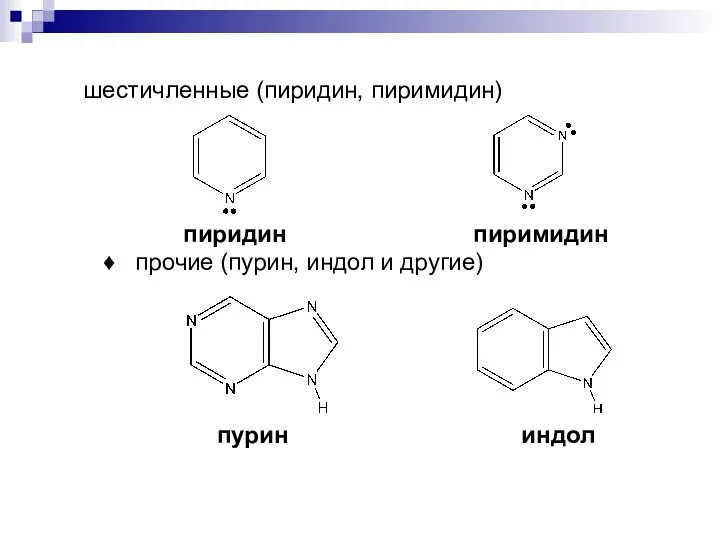
- 9. шестичленные (пиридин, пиримидин) пиридин пиримидин ♦ прочие (пурин, индол и другие) пурин индол
- 10. Ряды по ароматичности - бензол > нафталин > фенантрен > антрацен - бензол > тиофен >
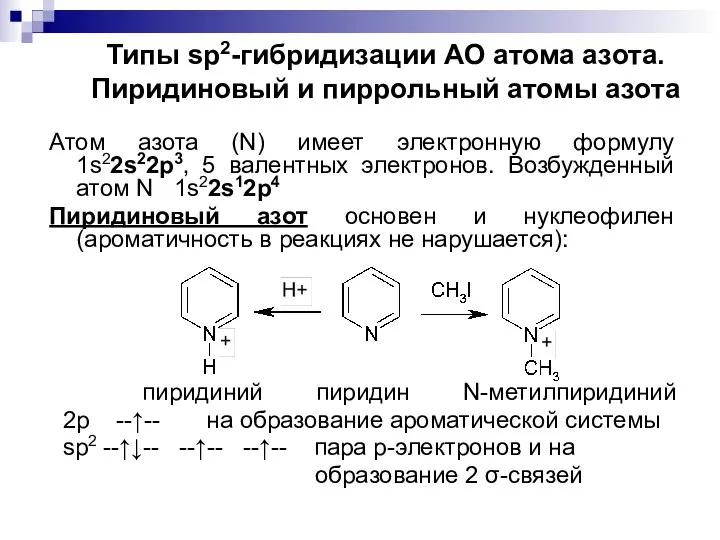
- 11. Типы sp2-гибридизации АО атома азота. Пиридиновый и пиррольный атомы азота Атом азота (N) имеет электронную формулу
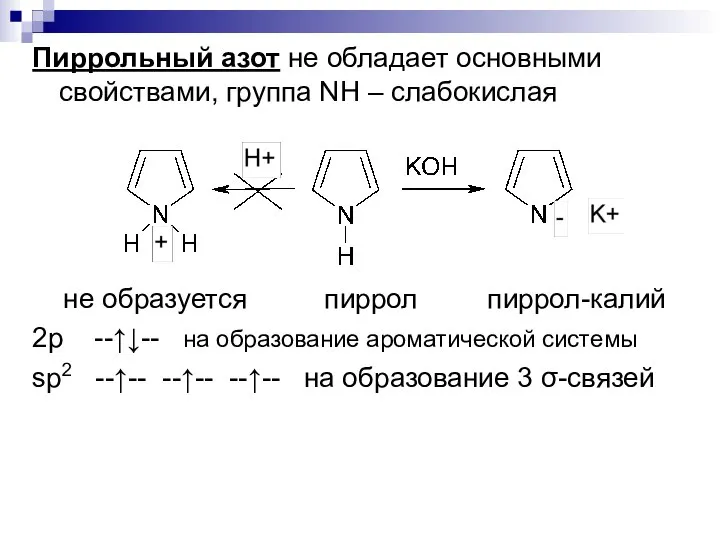
- 12. Пиррольный азот не обладает основными свойствами, группа NH – слабокислая не образуется пиррол пиррол-калий 2p --↑↓--
- 13. Биозначение сопряженных и ароматических соединений 1 Сопряженные и ароматические молекулы широко представлены в живых клетках
- 14. Биозначение сопряженных и ароматических соединений 2 кофермент гем и метаболит билирубин – производные пиррола; азотистые основания
- 15. ЭЛЕКТРОННЫЕ ЭФФЕКТЫ В ОРГАНИЧЕСКИХ МОЛЕКУЛАХ Электронные эффекты – перераспределение электронов химических связей и разделение зарядов между
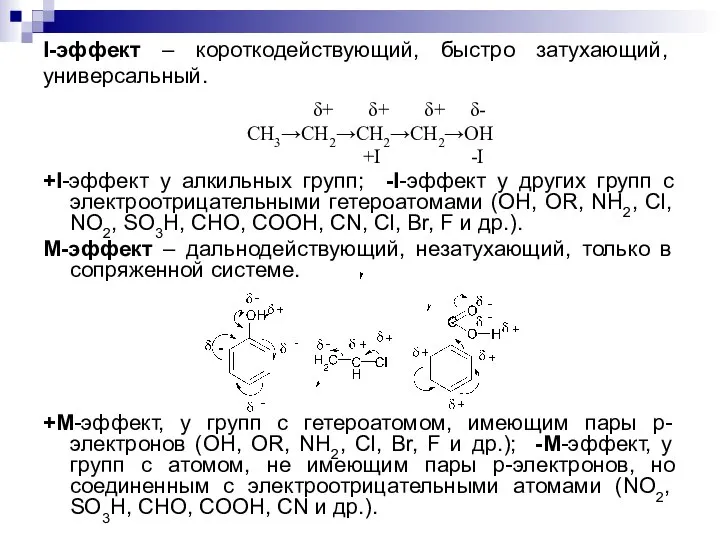
- 16. I-эффект – короткодействующий, быстро затухающий, универсальный. δ+ δ+ δ+ δ- CH3→CH2→CH2→CH2→OH +I -I +I-эффект у алкильных
- 17. КИСЛОТНОСТЬ – ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Кислота (по Брёнстеду) – химическое соединение, отщепляющее протон: R-A-H R-Ä- +
- 18. ПРОТОЛИТИЧЕСКАЯ ТЕОРИЯ СОПРЯЖЕННЫХ КИСЛОТ И ОСНОВАНИЙ БРЁНСТЕДА – ЛОУРИ. ОСНОВНЫЕ ПОЛОЖЕНИЯ 1. Если в системе имеется
- 19. ФАКТОРЫ, ВЛИЯЮЩИЕ НА КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ Кислота R-A-H R-Ä- + H+ Основание R-B: +
- 20. Кислота R-A-H R-Ä- + H+ Основание R-B: + H+ R-B+-H 3. Природа заместителя R Электроноакцепторные заместители
- 22. Скачать презентацию












 Ковалентная неполярная химическая связь
Ковалентная неполярная химическая связь Кислород. 8 класс
Кислород. 8 класс Альдегиды, их химические и физические свойства. Получение и применение альдегидов
Альдегиды, их химические и физические свойства. Получение и применение альдегидов Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Метаболизм липидов
Метаболизм липидов Жиры. Определение и общая формула
Жиры. Определение и общая формула Алюминий и его соединения
Алюминий и его соединения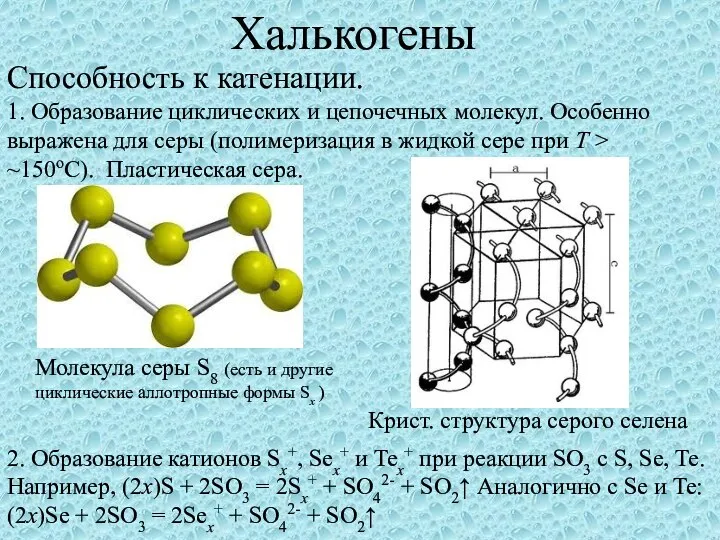 Халькогены. Способность к катенации
Халькогены. Способность к катенации Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Арбузный снег. Предположения
Арбузный снег. Предположения Презентация на тему ОВР в органической химии
Презентация на тему ОВР в органической химии  Её величество – вода Интегрированный урок химии в 8 классе
Её величество – вода Интегрированный урок химии в 8 классе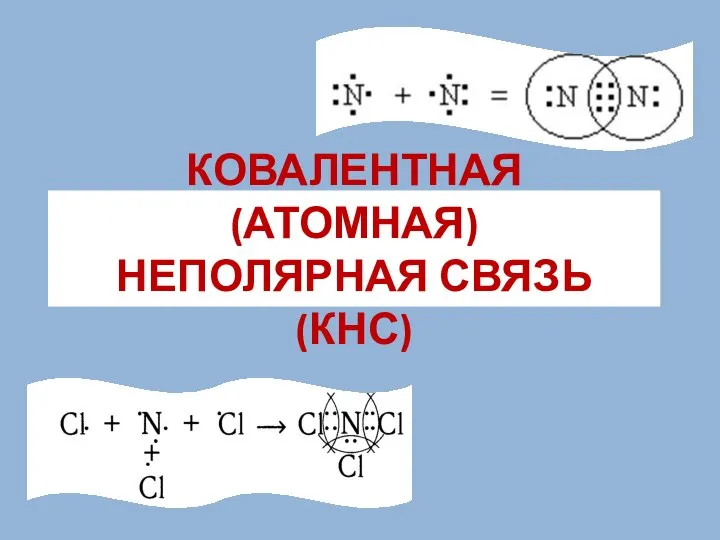 676a1c5e85f2455c9a6d495b8a94b9f9
676a1c5e85f2455c9a6d495b8a94b9f9 Периодическая система
Периодическая система Кислород. Оксиды. Валентность
Кислород. Оксиды. Валентность Презентация на тему Лекарства дома
Презентация на тему Лекарства дома  Радиоактивность. Тест
Радиоактивность. Тест Презентация на тему Лабораторное оборудование. Посуда и средства защиты
Презентация на тему Лабораторное оборудование. Посуда и средства защиты  Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность
Комплексы хлорида и иодида цинка (II) с карбамидом: синтез, характеристика и биологическая активность Закон сохранения массы веществ
Закон сохранения массы веществ Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Основные понятия химической термодинамики
Основные понятия химической термодинамики Основы химической термодинамики. Основные понятия химической термодинамики. Лекция 1
Основы химической термодинамики. Основные понятия химической термодинамики. Лекция 1 Сокровища соляных дворцов
Сокровища соляных дворцов Презентация на тему Занимательная химия
Презентация на тему Занимательная химия  Подготовка к административной контрольной работе по химии
Подготовка к административной контрольной работе по химии Гидроксид кальция – гашеная известь
Гидроксид кальция – гашеная известь Анализ свойств карбамидоформальдегидных смол
Анализ свойств карбамидоформальдегидных смол