Содержание
- 2. Физические свойства алкинов С2 – С4 газы С5 – С 15 жидкости Свыше С16 – твердые
- 3. Химические свойства алкинов 1. Реакции присоединения АЕ Н.Б.Давыдова, учитель химии МБОУ "Вадская СОШ"
- 4. Химические свойства алкинов 1. Реакции присоединения АЕ а) Гидрирование(+Н2) в 2 стадии: Н.Б.Давыдова, учитель химии МБОУ
- 5. 1. Реакции присоединения АЕ б) Галогенирование (+Г2) в 2 стадии: Качественная реакция на алкины – бромная
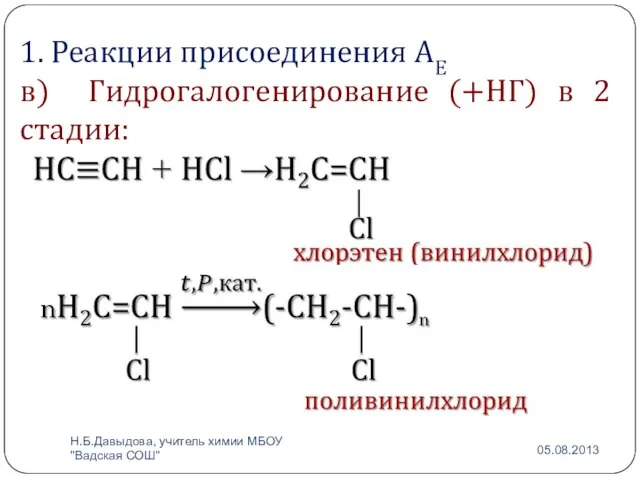
- 6. 1. Реакции присоединения АЕ в) Гидрогалогенирование (+НГ) в 2 стадии: Н.Б.Давыдова, учитель химии МБОУ "Вадская СОШ"
- 7. Применение поливинилхлорида: Изоляция для проводов, изоляционная лента, искусственная кожа, плащи, кленка. Н.Б.Давыдова, учитель химии МБОУ "Вадская
- 8. Присоединение НГ к несимметричным алкинам (по правилу Марковникова) МАРКОВНИКОВ Владимир Васильевич Н.Б.Давыдова, учитель химии МБОУ "Вадская
- 9. МАРКОВНИКОВ Владимир Васильевич (13 декабря 1837—29 января 1904) — русский химик, основатель научной школы. Развивая теорию
- 10. 1. Реакции присоединения АЕ г)Гидратация (+НОН). Реакция Кучерова. КУЧЕРОВ Михаил Григорьевич Правило Эльтекова: Спирты, содержащие гидроксо-группу
- 11. КУЧЕРОВ Михаил Григорьевич (3 июня1850 – 26 июня 1911). Русский химик-органик. Основные работы посвящены развитию органического
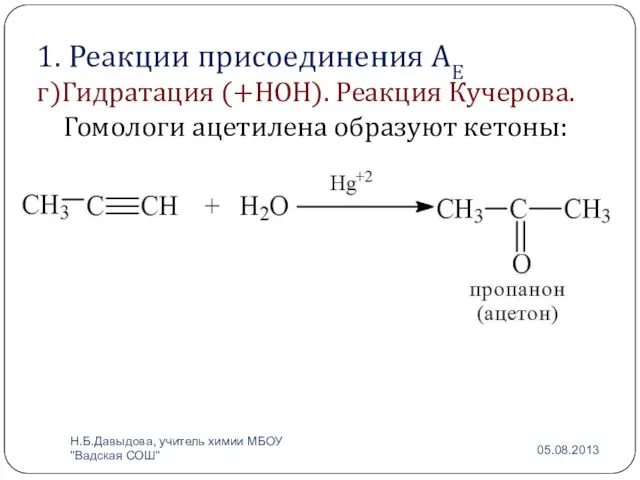
- 12. 1. Реакции присоединения АЕ г)Гидратация (+НОН). Реакция Кучерова. Гомологи ацетилена образуют кетоны: Н.Б.Давыдова, учитель химии МБОУ
- 13. Опыт. Горение ацетилена Ацетилен образует с воздухом и кислородом взрывоопасные смеси. Опыт . Взрыв смеси ацетилена
- 14. 2. Реакции окисления. а) Окисление раствором водным раствором перманганата калия (качественная реакция). В нейтральной и слабощелочной
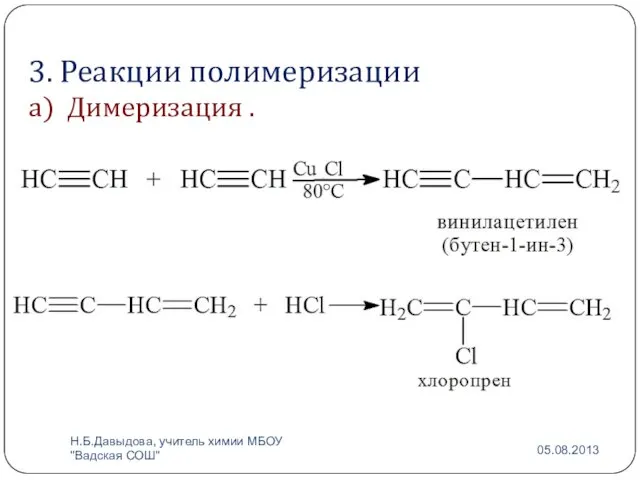
- 15. 3. Реакции полимеризации а) Димеризация . Н.Б.Давыдова, учитель химии МБОУ "Вадская СОШ"
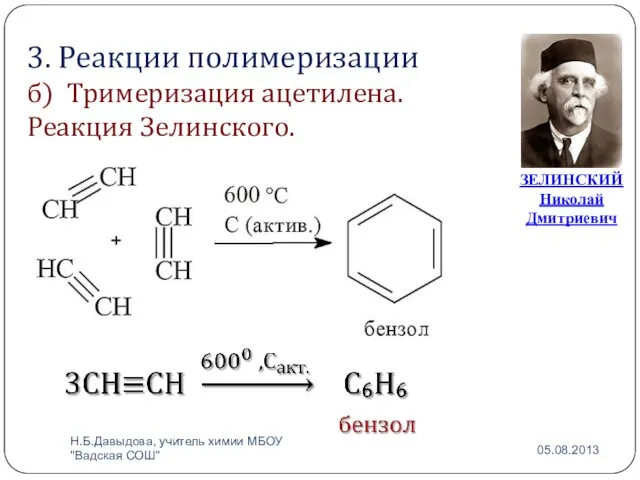
- 16. 3. Реакции полимеризации б) Тримеризация ацетилена. Реакция Зелинского. ЗЕЛИНСКИЙ Николай Дмитриевич Н.Б.Давыдова, учитель химии МБОУ "Вадская
- 17. Николай Дмитриевич Зелинский (25 января 1861 — 31 июля 1953) — замечательный русский химик, основоположник учения
- 18. 4. Реакции замещения (кислотные свойства) HC≡CH + Ag2O → AgC≡CAg↓+ H2O амм. р-р ацетиленид серебра, белый
- 19. ТРЕНАЖЁРЫ: Закрепление материала Типы химических реакций, характерные для алкинов Уравнения реакций, характеризующие химические свойства ацетилена Химические
- 20. ПОДГОТОВКА К ЕГЭ: Закрепление материала Базовый уровень сложности 1. При гидратации ацетилена образуется 1) этанол 2)
- 21. ПОДГОТОВКА К ЕГЭ: Базовый уровень сложности 5. Пропин можно отличить от пропена с помощью 1) водного
- 22. Повышенный уровень сложности 8. Бутин-1 способен реагировать с 1) натрием 4) кислородом 2) гидроксидом натрия 5)
- 23. Домашнее задание: Учебник: Кузнецова Н.Е., Гара Н.Н. Титова И.М.; под ред. Н. Е. Кузнецовой. Химия: профильный
- 25. Скачать презентацию


















 Кетоны. Реагирующие вещества
Кетоны. Реагирующие вещества Какую воду мы пьем
Какую воду мы пьем 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Тестовая работа по теме: Реакции ионного обмена. Химия. 9 класс
Тестовая работа по теме: Реакции ионного обмена. Химия. 9 класс Сурьма, Sb
Сурьма, Sb Органическая химия. Химические свойства и типы реакций. (9 класс)
Органическая химия. Химические свойства и типы реакций. (9 класс) Способы разделение смесей. 7 класс
Способы разделение смесей. 7 класс Общая формула оксидов
Общая формула оксидов Čo sú chemické reakcie
Čo sú chemické reakcie Амины, азо- и диазосоединения (продолжение)
Амины, азо- и диазосоединения (продолжение) Карбоцепные полимеры
Карбоцепные полимеры Характеристика кислорода и серы
Характеристика кислорода и серы Застосування рідких кристалів
Застосування рідких кристалів Алюминий. Положение алюминия в периодической системе и строение его атома
Алюминий. Положение алюминия в периодической системе и строение его атома Періодична система хімічних елементів
Періодична система хімічних елементів Сложные эфиры
Сложные эфиры Михаил Васильевич Ломоносов (1711-1765)
Михаил Васильевич Ломоносов (1711-1765) Создание учебно-методических материалов по химии в современной форме (презентации уроков)
Создание учебно-методических материалов по химии в современной форме (презентации уроков) Алюминий (AI)
Алюминий (AI) Количественный анализ. Методы количественного анализа
Количественный анализ. Методы количественного анализа Предмет органическая химия. Теория строения органических веществ
Предмет органическая химия. Теория строения органических веществ Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Мутагены окружающей среды
Мутагены окружающей среды Химическая термодинамика
Химическая термодинамика Роль металлов в искусстве
Роль металлов в искусстве Молекулярная химия
Молекулярная химия Энергетическая диаграмма орбиталей многоэлектронного атома
Энергетическая диаграмма орбиталей многоэлектронного атома Алюминий
Алюминий