Содержание
- 2. Химия – это наука о веществах, их свойствах и превращениях Физическое тело вещество Химический элемент -
- 4. Вещества – это то, из чего состоят тела
- 5. Химический элемент – определенный вид атома.
- 6. План характеристики элемента: 1. Символ и название. 2. Положение в ПСХЭ. 3. Строение атома. 4. Электронная
- 7. Ион - Заряженная частица вещества NA+, Cl- , SO4 2-, Al3+
- 8. это вещества, состоящие из атомов одного химического элемента это вещества, состоящие из атомов двух или нескольких
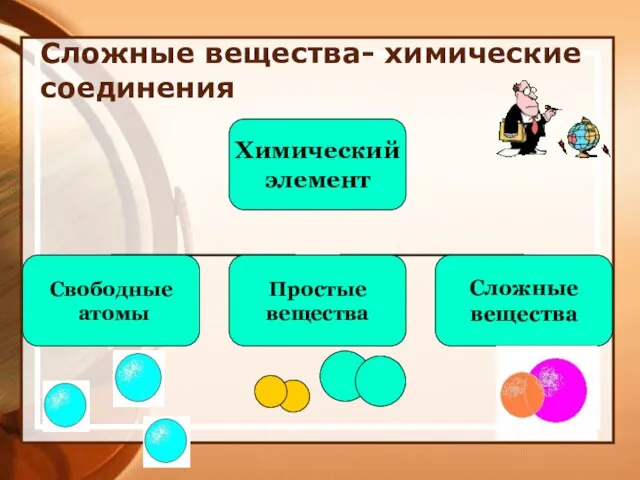
- 9. Сложные вещества- химические соединения
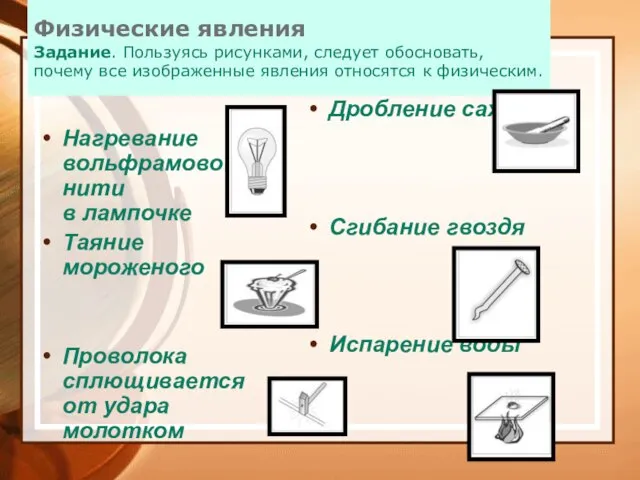
- 10. Физические явления Задание. Пользуясь рисунками, следует обосновать, почему все изображенные явления относятся к физическим. Нагревание вольфрамовой
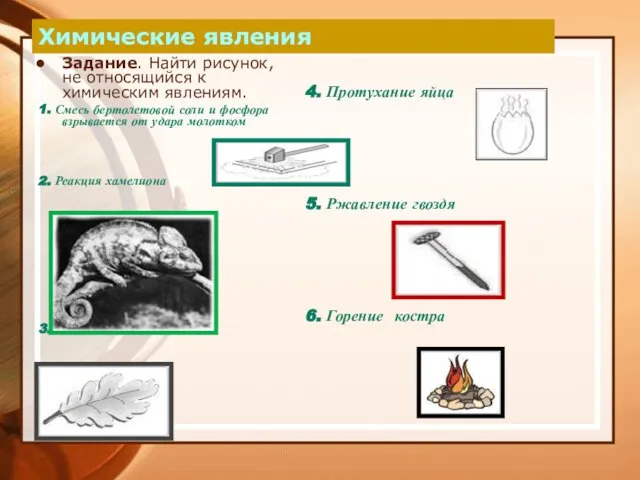
- 11. Химические явления Задание. Найти рисунок, не относящийся к химическим явлениям. 1. Смесь бертолетовой соли и фосфора
- 12. Признаки химической реакции Изменение окраски. Выделение или поглощение теплоты. Появление запаха. Образования осадка. Выделение газа.
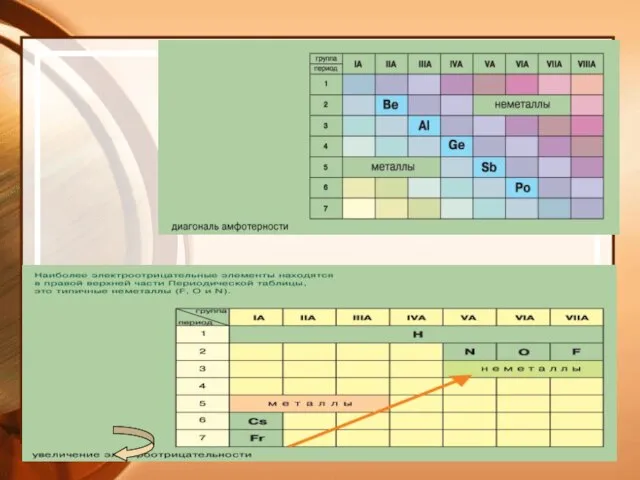
- 13. ПЕРИОДИЧНОСТЬ СВОЙСТВ в ПЕРИОДАХ: В пределах одного периода слева направо металлические свойства ослабевают; А неметаллические возрастают.
- 14. Под ВАЛЕНТНОСТЬ (сила) понимают свойства атомов образовывать химические связи с другими атомами, а также число одинарных
- 15. Химические формулы Химическая формула – это условная запись состава вещества посредством химических знаков и индексов.
- 16. Химическая формула.
- 17. Закон постоянства состава вещества или закон Пруста. каждое химически чистое вещество с молекулярным строением независимо от
- 18. Индекс показывает количество атомов данного элемента в молекуле. Итак, состав веществ выражается химическими формулами с целочисленными
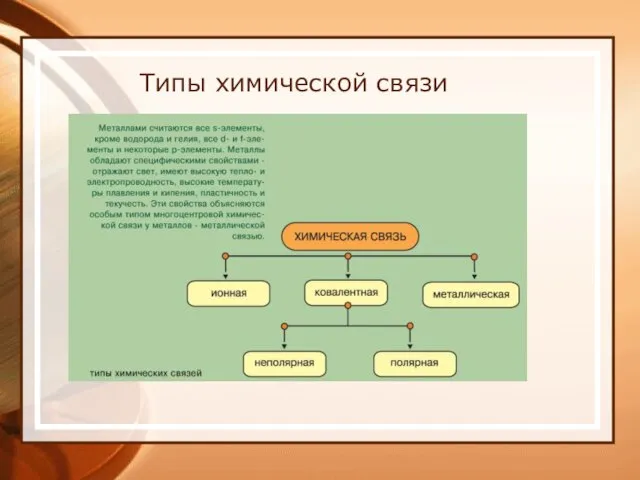
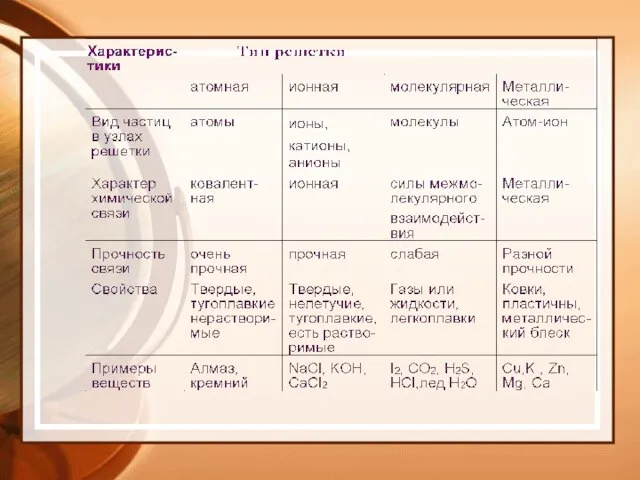
- 19. Типы химической связи
- 21. Электроотрицательность - способность атомов оттягивать на себя электроны. Ряд ЭО: Si H P C S Br
- 23. Металлы Na K Ca Ba Cu Ag Au Zn Pb Hg Al Mg Mn Fe натрий
- 24. Неметаллы S Cl Br C Si J N P O F H cера углерод водород кремний
- 25. Au 79 196, 97 число, показывающее во сколько раз масса данного атома больше массы атома водорода
- 26. Массовые доли элементов. ФОРМУЛА: Ar (эл.)• n W(эл.) Mr (в-ва) Единицы измерения [доли] или [%], в
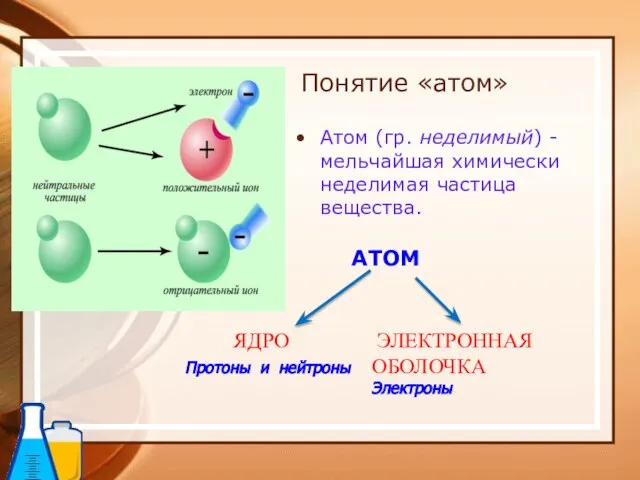
- 27. Понятие «атом» Атом (гр. неделимый) - мельчайшая химически неделимая частица вещества. АТОМ
- 28. ОСНОВНЫЕ ПОЛОЖЕНИЯ ПЛАНЕТАРНОЙ МОДЕЛИ: Атом – это микрочастица, которая имеет форму шара. Атом – это сложная
- 29. Как измерить вещество? Необходимо точно знать число частиц вещества, т.е. его количество Единица количества вещества –
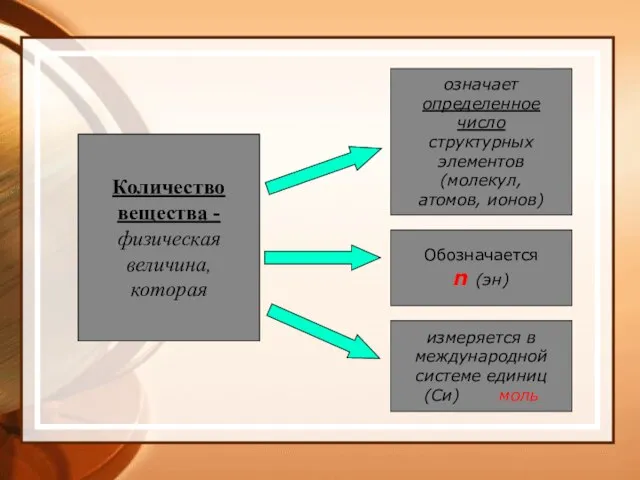
- 30. Количество вещества - физическая величина, которая означает определенное число структурных элементов (молекул, атомов, ионов) Обозначается n
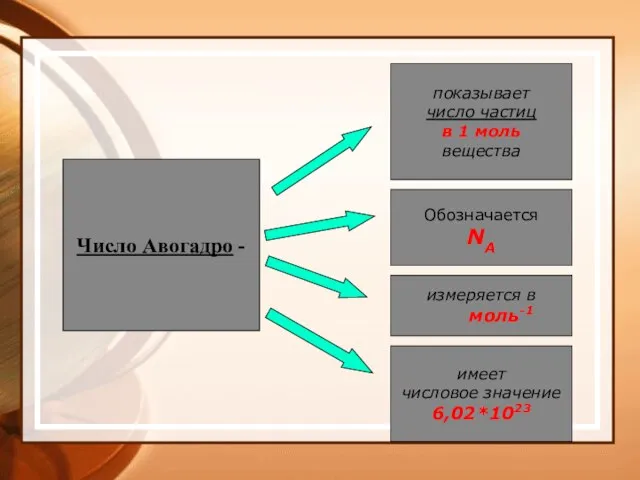
- 31. Число Авогадро - показывает число частиц в 1 моль вещества Обозначается NA измеряется в моль-1 имеет
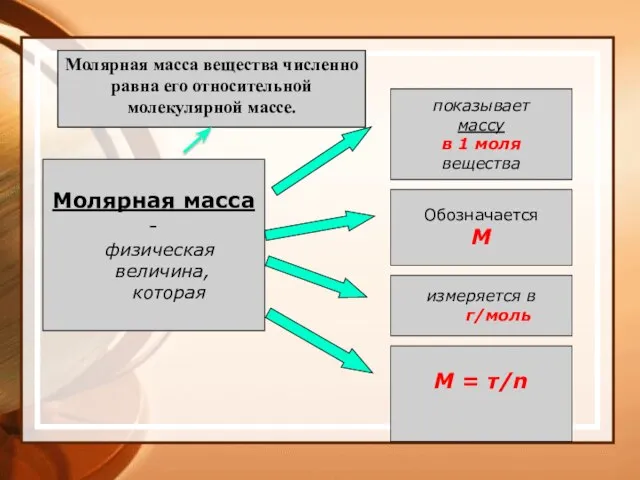
- 32. Молярная масса - физическая величина, которая показывает массу в 1 моля вещества Обозначается М измеряется в
- 33. Для расчёта количества n= m / М n=V/Vm n =N / Na
- 34. Но если число частиц известно? В 1 моле содержится 6 ● 10 23 частиц Эта величина
- 35. Амедео Авогадро высказал предположение в 1811 году, что В равных объемах различных газов при одинаковых условиях
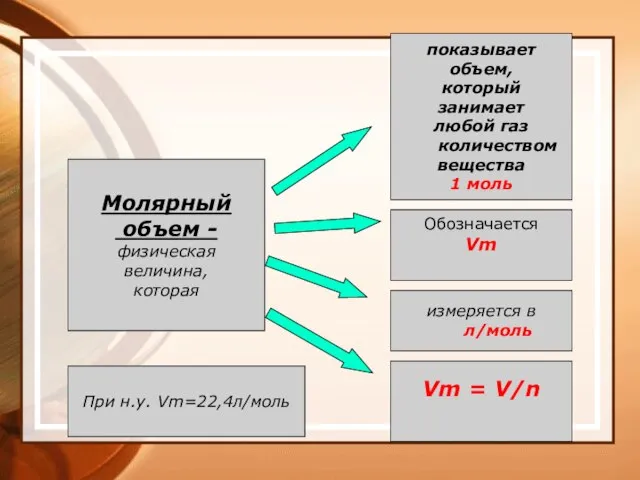
- 36. Молярный объем газа Vm — величина, определяемая отношением объема данной порции газа V к химическому количеству
- 37. Молярный объем - физическая величина, которая показывает объем, который занимает любой газ количеством вещества 1 моль
- 38. Производные формулы Иванова Г.А. [email protected] m= n ● М V=n ● Vm N =n ● Na
- 39. Отношение массы растворимого вещества к общей массе раствора называют массовой долей растворенного вещества. Массовую долю обозначают
- 41. Скачать презентацию

























 Презентация на тему Ковалентная связь: полярная и неполярная
Презентация на тему Ковалентная связь: полярная и неполярная  Производство нитрата аммония (лекция 16)
Производство нитрата аммония (лекция 16) Презентация на тему В мире индикаторов - исследовательская работа
Презентация на тему В мире индикаторов - исследовательская работа  Современные подходы к преподаванию химии
Современные подходы к преподаванию химии Алюминий. Строение и свойства атома
Алюминий. Строение и свойства атома Жизнь и деятельность Д.И.Менделеева «Если не будешь знать имен, то умрет и познание вещей» К.Линей. Автор: Ватитова А.А. МОУ Еласов
Жизнь и деятельность Д.И.Менделеева «Если не будешь знать имен, то умрет и познание вещей» К.Линей. Автор: Ватитова А.А. МОУ Еласов Природные источники углеводородов
Природные источники углеводородов Химия вокруг нас. 10 класс
Химия вокруг нас. 10 класс Амины. Аминокислоты
Амины. Аминокислоты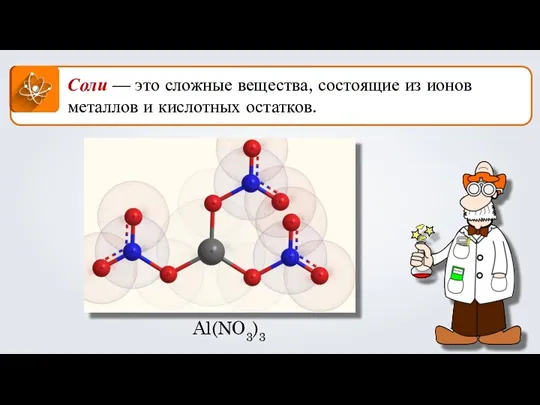 Соли. Формула соли
Соли. Формула соли Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Ковалентная полярная связь
Ковалентная полярная связь Коллоидные системы Классификация. Получение. Очистка. Свойства. Устойчивость и коагуляция. Применение
Коллоидные системы Классификация. Получение. Очистка. Свойства. Устойчивость и коагуляция. Применение Основные соединения кальция и их применение – вчера, сегодня, завтра.
Основные соединения кальция и их применение – вчера, сегодня, завтра. Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Алотропия углерода
Алотропия углерода ÐÐÐÐ ÐÐТÐÐРХÐÐÐЧÐСÐÐÐ¥ Ð ÐÐÐЦÐÐ
ÐÐÐÐ ÐÐТÐÐРХÐÐÐЧÐСÐÐÐ¥ Ð ÐÐÐЦÐÐ Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл.
Изменения, происходящие с веществами Урок химии 8 класс Учитель химии МОУ «СОШ №7» г. Балаково Саратовская обл. Химический процесс: энергетика и равновесие
Химический процесс: энергетика и равновесие Презентация на тему Химическое равновесие
Презентация на тему Химическое равновесие 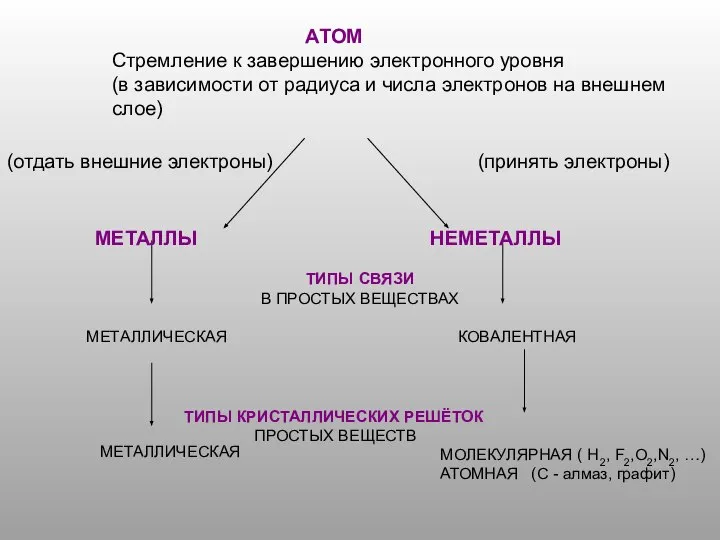 Атом. Стремление к завершению электронного уровня
Атом. Стремление к завершению электронного уровня Кислоты. Классификация кислот
Кислоты. Классификация кислот Коррозия металлов
Коррозия металлов Теория активированного комплекса
Теория активированного комплекса Л-1-5
Л-1-5 Презентация на тему Фенол и его свойства
Презентация на тему Фенол и его свойства  Процессы растворения твёрдых веществ
Процессы растворения твёрдых веществ Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения