Содержание
- 2. Fe Это элемент № 26 Это элемент 4- ого периода Четвертый по распространенности элемент в земной
- 3. Электронное строение железа
- 4. Нахождение в природе В земной коре железо распространено достаточно широко — на его долю приходится около
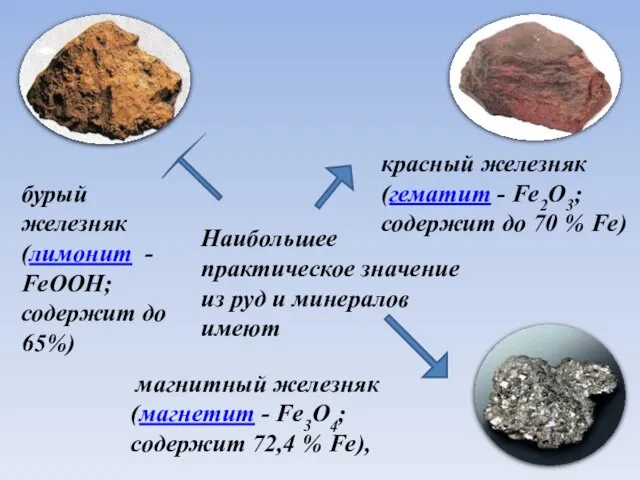
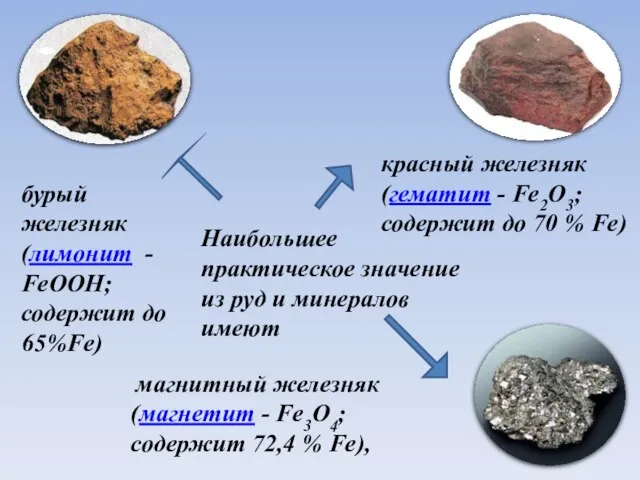
- 5. Наибольшее практическое значение из руд и минералов имеют магнитный железняк (магнетит - Fe3O4; содержит 72,4 %
- 6. Наибольшее практическое значение из руд и минералов имеют магнитный железняк (магнетит - Fe3O4; содержит 72,4 %
- 7. Физические свойства железа Железо- сравнительно мягкий , ковкий серебристо-серый металл Температура плавления 15350C Температура кипения 28000C
- 8. Химические свойства 1. Реакции с простыми веществами Железо сгорает в чистом кислороде при нагревании:4Fe +3O2=2Fe2O3 Реагирует
- 9. Химические свойства 2. Реакции со сложными веществами С кислотами: А) с соляной кислотой 2HCL + Fe
- 10. Железо в организме Железо присутствует в организмах всех растений и животных, но в малых количествах (в
- 11. Биологическая роль железа Железо играет важную роль в жизнедеятельности живых организмов. Оно входит в состав гемоглобина
- 12. Первое металлическое железо, попавшее в руки человека, имело, вероятно, метеоритное происхождение. Руды железа широко распространены и
- 13. Люди впервые овладели железом в четвертом-третьем тысячелетиях до н. э., подбирая упавшие с неба камни —
- 14. Применение железа, его сплавов и соединений Чистое железо имеет довольно ограниченное применение. Его используют при изготовлении
- 15. «Чистое железо способно быстро намагничиваться и размагничиваться, поэтому его применяют для изготовления сердечников, трансфо-, мембраноматоров, электромагнитов
- 17. Скачать презентацию










 Что такое эксперимент?
Что такое эксперимент? Щелочные металлы
Щелочные металлы Магний (Mg, Magnesium). Общая характеристика магния
Магний (Mg, Magnesium). Общая характеристика магния Кетоны. Реагирующие вещества
Кетоны. Реагирующие вещества Полезные ископаемые
Полезные ископаемые Презентация на тему Полимеры
Презентация на тему Полимеры  Растительные жиры. Пальмовое масло
Растительные жиры. Пальмовое масло Aspergillus promising biological properties
Aspergillus promising biological properties Сложные эфиры. Жиры
Сложные эфиры. Жиры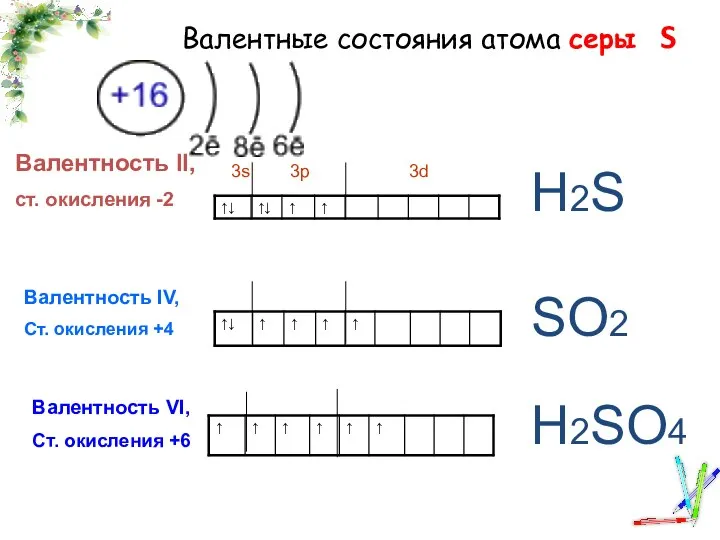 Валентные состояния атома серы
Валентные состояния атома серы относительная атомная масса
относительная атомная масса Типы химических реакций
Типы химических реакций Химическое равновесие
Химическое равновесие Предмет органической химии. Урок №1
Предмет органической химии. Урок №1 In aqua veritas. Правда в воде. Задача 12
In aqua veritas. Правда в воде. Задача 12 Витамины. Классификация витаминов
Витамины. Классификация витаминов Натуральный каучук
Натуральный каучук Вводный урок по химии
Вводный урок по химии Направление процесса. ОВР
Направление процесса. ОВР Масс-спектрометрия шерсти волка обыкновенного Canis lupus
Масс-спектрометрия шерсти волка обыкновенного Canis lupus Температурная зависимость скорости химической реакции
Температурная зависимость скорости химической реакции Микроэмульсия. Микроэмульсияның макроэмулсиядан айырмашылығы
Микроэмульсия. Микроэмульсияның макроэмулсиядан айырмашылығы Клуб юных химиков. Школа №3
Клуб юных химиков. Школа №3 Презентация по Химии "Строение и физические свойства металлов"
Презентация по Химии "Строение и физические свойства металлов"  Выращивание кристаллов соли и сахара в домашних условиях
Выращивание кристаллов соли и сахара в домашних условиях Щелочноземельные металлы
Щелочноземельные металлы Массовая доля химического элемента
Массовая доля химического элемента Валентность, Составление формул
Валентность, Составление формул