Содержание
- 2. История создания 1840 г. – Ю.Ф.Фрицше обнаружил, что при нагревании с щелочью синяя окраска индиго исчезает
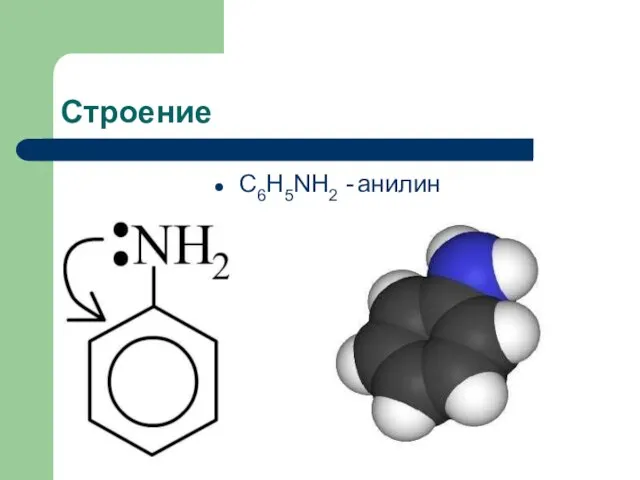
- 3. Строение C6H5NH2 - анилин
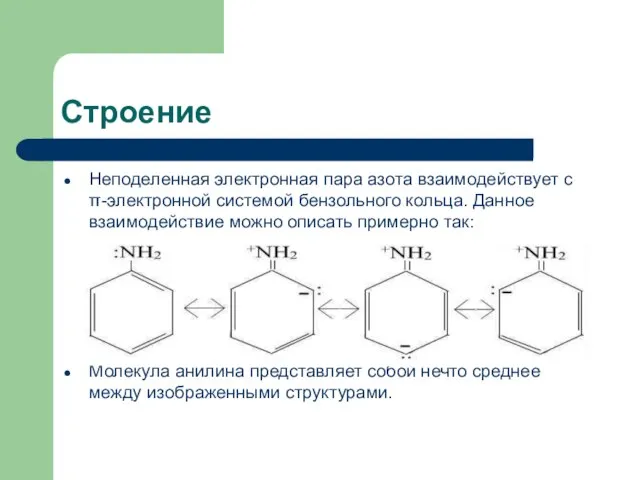
- 4. Строение Неподеленная электронная пара азота взаимодействует с π-электронной системой бензольного кольца. Данное взаимодействие можно описать примерно
- 5. Общая информация о строении Эти структурные формулы показывают, что электронная пара азота втягивается в бензольное кольцо,
- 6. Физические свойства Анилин - бесцветная маслянистая жидкость. При окислении на воздухе становится светло-коричневого цвета. Немного тяжелее
- 7. Получение В промышленности C6H5NO2 + 3H2 250-300C,Ni,Cu C6H5NH2 + 2H2O C6H5NO2 + 6[H] Fe,HCl,H2O C6H5NH2 +
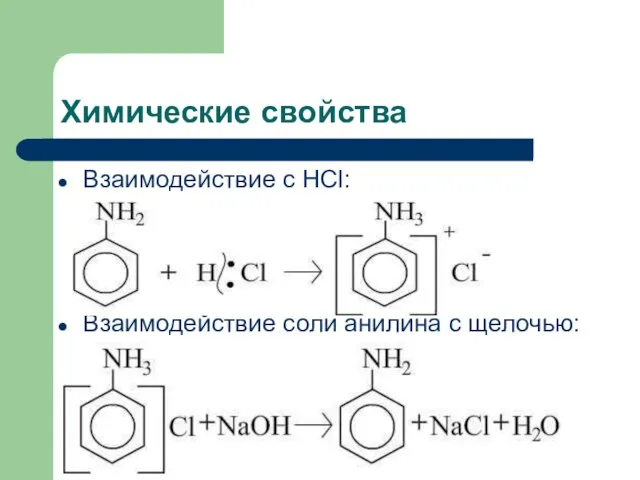
- 8. Химические свойства Взаимодействие с HCl: Взаимодействие соли анилина с щелочью:
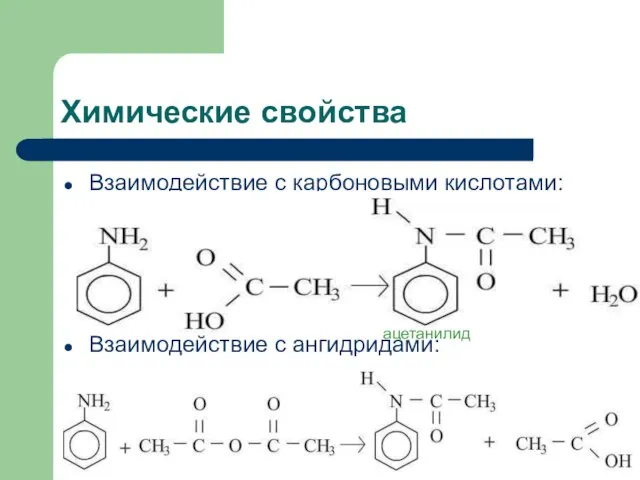
- 9. Химические свойства Взаимодействие с карбоновыми кислотами: Взаимодействие с ангидридами:
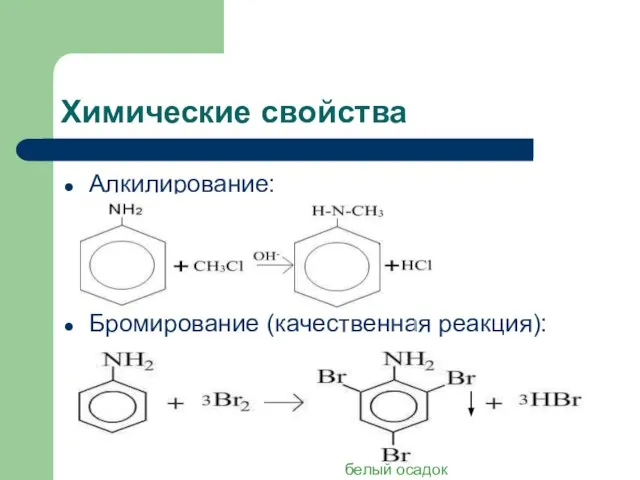
- 10. Химические свойства Алкилирование: Бромирование (качественная реакция): белый осадок
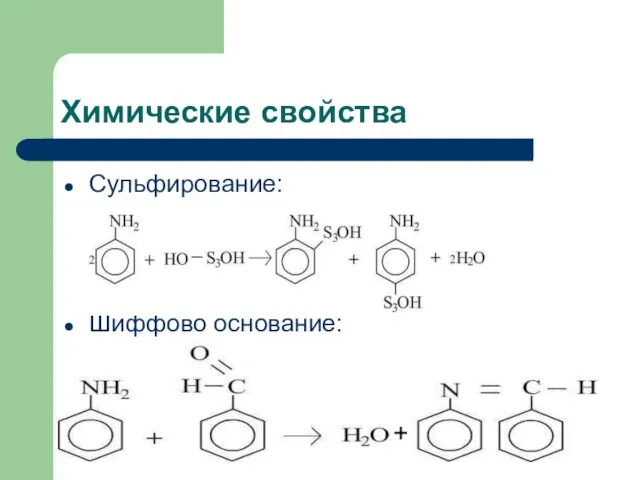
- 11. Химические свойства Сульфирование: Шиффово основание:
- 12. Химические свойства Нитрование: C6H5NH2+NaNO2+2HCl [C6H5-N≡N]+Cl- +NaCl + 2H2O хлорид диазония Диазосоединения можно выделить в виде кристаллических,
- 13. Применение В настоящий момент в мире основная часть (85%) производимого анилина используется для производства метилдиизоционатов (MDI),
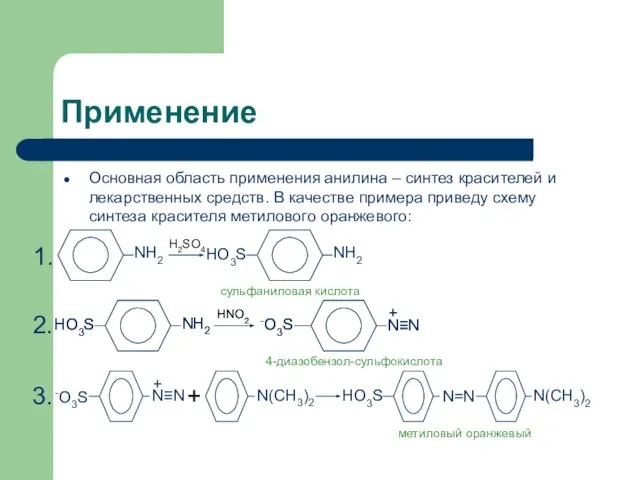
- 14. Применение Основная область применения анилина – синтез красителей и лекарственных средств. В качестве примера приведу схему
- 16. Скачать презентацию




![Химические свойства Нитрование: C6H5NH2+NaNO2+2HCl [C6H5-N≡N]+Cl- +NaCl + 2H2O хлорид диазония Диазосоединения можно](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/480258/slide-11.jpg)

 Развитие познавательной активности творческих способностей и индивидуализация на уроках химии
Развитие познавательной активности творческих способностей и индивидуализация на уроках химии Углеродистые стали
Углеродистые стали Целестин
Целестин Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год
Презентацию выполнила ученица 10 класса Поликарпова Диана 2010 год Гальванический элемент
Гальванический элемент Углеводы. Классификация углеводов
Углеводы. Классификация углеводов Степень окисления. Классификация неорганических соединений
Степень окисления. Классификация неорганических соединений Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Органическая химия
Органическая химия Соединения азота в атмосфере. Лекция 4
Соединения азота в атмосфере. Лекция 4 Структура к свойства веществ
Структура к свойства веществ Химические вещества парабены
Химические вещества парабены Влияние меди на коррозию низколегиованных сталей
Влияние меди на коррозию низколегиованных сталей Серная кислота
Серная кислота Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров Окислители в пиросоставах
Окислители в пиросоставах Вода. Строение молекулы. Водородная связь. Физические и химические свойства
Вода. Строение молекулы. Водородная связь. Физические и химические свойства Презентация на тему Гидролиз
Презентация на тему Гидролиз  Электролиз
Электролиз Презентация на тему Глюкоза (10 класс)
Презентация на тему Глюкоза (10 класс)  Основания и их свойства
Основания и их свойства Презентация на тему Многоатомные спирты
Презентация на тему Многоатомные спирты  Жидкое состояние вещества
Жидкое состояние вещества Поделочный камень родонит
Поделочный камень родонит Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора
Фосфор. Аллотропия фосфора. Физические и химические свойства фосфора Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Получение металлов
Получение металлов Степени окисления
Степени окисления