Содержание
- 2. 4. Что такое кислоты? 1. Какие классы веществ вы знаете? 2. Что такое оксиды? 3. Что
- 3. К какому классу соединений относятся формулы веществ? Назовите их. H2SO4 Na2O Ba(OH)2 H2CO3 N2O5 KOH
- 4. О каком веществе идёт речь? У травоядных животных потребность в этом веществе велика. В тех странах,
- 5. • научить составлять формулы солей и давать им названия; • узнать классификацию, свойства солей, способы получения
- 6. Задачи: Научить находить среди неорганических веществ формулы солей; составлять формулы солей; называть соли.
- 7. План урока: 6. Химические свойства. 1. Что такое соли? 2. Классификация солей. 3. Номенклатура солей. 4.
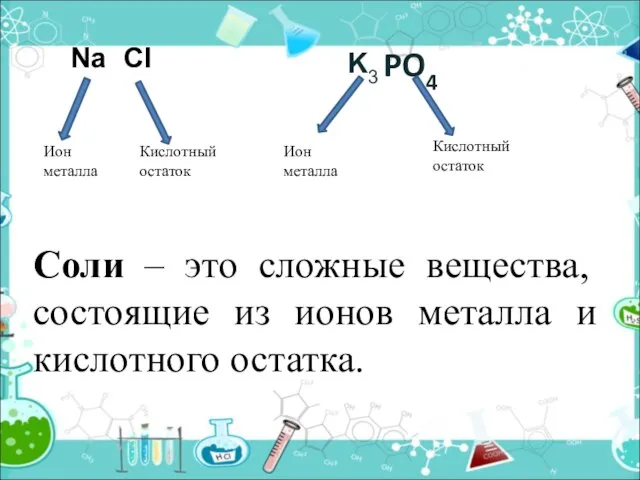
- 8. PO4 Ион металла Кислотный остаток Ион металла Кислотный остаток Na Cl K3 Соли – это сложные
- 9. Найдите среди формул веществ- формулы солей CO2 H2 SO4 CaO BaSO4 K2SO4 Fe(OH)3 HCl MgCO3 H2O
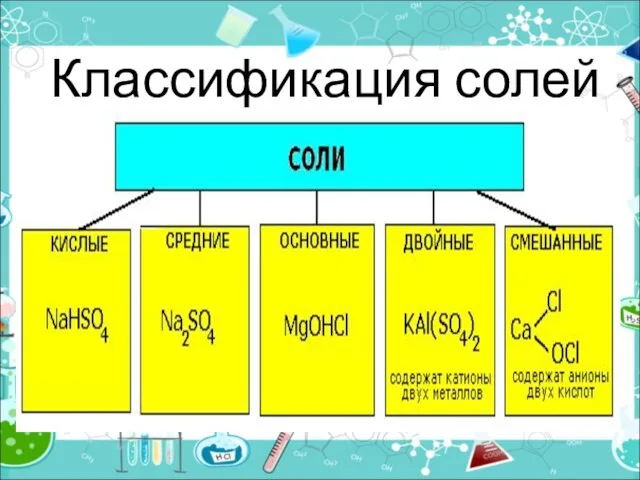
- 10. Классификация солей
- 11. Средние (нормальные) соли — все атомы водорода в молекулах кислоты замещены на атомы металла (KCl) Кислые
- 12. Двойные соли — в их составе присутствует два различных катиона, получаются кристаллизацией из смешанного раствора солей
- 13. Номенклатура средних солей магния Название кислотного остатка Наименование металла в родительном падеже МgСL2 хлорид
- 14. Номенклатура кислых солей Указать название кислотного остатка К названию кислотного остатка прибавить «гидро-» Наименование металла в
- 15. Номенклатура основных солей Указать название кислотного остатка К названию кислотного остатка прибавить «основной-» Наименование металла в
- 16. Номенклатура двойных солей таллия (I) -натрия Название кислотного остатка Наименование металлов в родительном падеже NaTl(NO3)2 нитрат
- 17. Номенклатура смешанных солей кальция Название кислотных остатков Наименование металла в родительном падеже CaCLOCL хлорид-гипохлорит
- 18. Составить формулы солей: нитрита магния, силиката натрия, фосфата кальция.
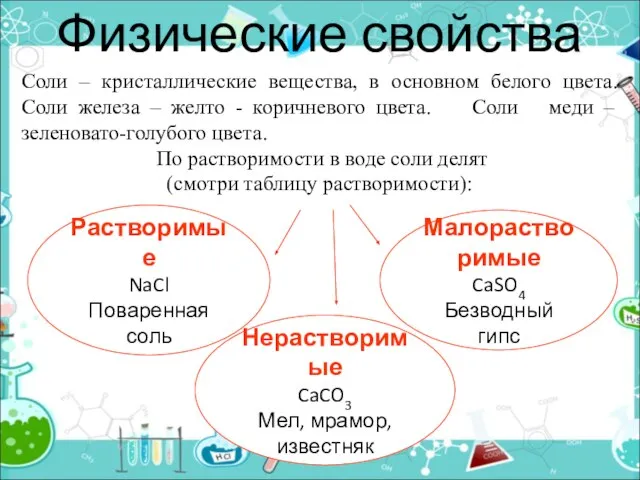
- 19. Физические свойства Растворимые NaCl Поваренная соль Соли – кристаллические вещества, в основном белого цвета. Соли железа
- 20. Химические свойства 1. Взаимодействие с металлами. Каждый левее стоящий металл в ряду напряжений вытесняет последующий из
- 21. Химические свойства 2. Взаимодействие со щелочами: В результате обязательно должно образоваться нерастворимое основание. 3. Взаимодействие солей
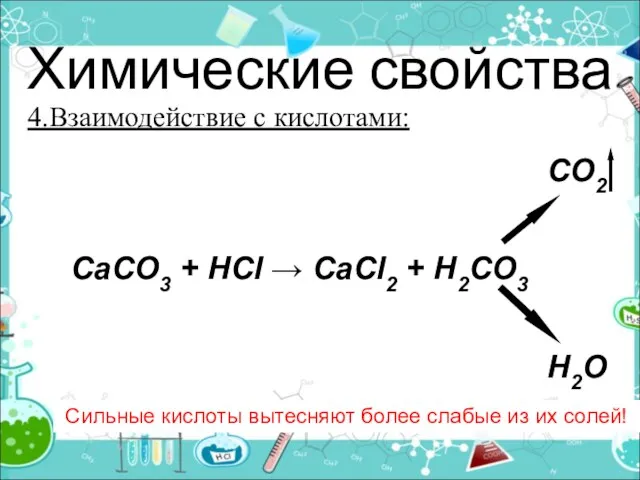
- 22. Химические свойства 4.Взаимодействие с кислотами: Сильные кислоты вытесняют более слабые из их солей! CO2 CaCO3 +
- 23. Химические свойства 5. Разложение при нагревании: СаСО3= СО2 + Н2О
- 24. Способы получения 1. Кислота + основание = соль + вода H2SO4 +2NaOH = Na2SO4 + 2H2O
- 25. Способы получения 5. Основание + соль = новое основание + новая соль 2КОН + СаSO4 =
- 26. Применение солей Соли соляной кислоты. Из хлоридов больше всего используют хлорид натрия и хлорид калия. Хлорид
- 27. Применение солей Соли серной кислоты. В строительстве и в медицине широко используют полуводный гипс, получаемый при
- 28. Применение солей Соли азотной кислоты. Нитраты больше всего используют в качестве удобрений в сельском хозяйстве. Важнейшим
- 29. Применение солей Соли угольной кислоты. Карбонат кальция используют в качестве сырья для получения извести. Карбонат натрия
- 30. О соли Мёртвое море
- 31. Розовое озеро в Сенегале Это озеро имеет такой цвет из-за большого количества микроорганизмов и полезных ископаемых.
- 32. Самое большое солевое озеро в мире расположено на юге пустынной равнины Альтиплано, в Боливии, на высоте
- 33. Химический диктант 1 вариант 1.соли металла 2. сульфат алюминия 3. белого 4. Cu(OH)2 5. хлора, соды
- 34. Сиквейн 1. В первой строчке тема называется одним словом (обычно существительным). 2. Вторая строчка — это
- 35. Сиквейн 1. Соль 2. Белая, кристаллическая 3. Солит, удобряет, растворяется 4. Соль наносит вред здоровью 5.
- 36. Домашнее задание §33, Упр.2, 3, 6 (письменно)
- 37. СПАСИБО ЗА УРОК!
- 39. Скачать презентацию































 Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием
Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием Основные понятия химической термодинамики
Основные понятия химической термодинамики Биологическая роль III(A) группы
Биологическая роль III(A) группы Органические вещества
Органические вещества Презентация на тему Кристаллические решетки
Презентация на тему Кристаллические решетки  Адсорбция твёрдыми адсорбентами
Адсорбция твёрдыми адсорбентами Фторсодержащие полимеры
Фторсодержащие полимеры Презентация на тему Волокна
Презентация на тему Волокна  Презентация на тему Путешествие по континенту Химия
Презентация на тему Путешествие по континенту Химия  Соли в природе и их значение
Соли в природе и их значение Задача №3: Трансмутация. Команда: Карбораны
Задача №3: Трансмутация. Команда: Карбораны Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Металлическая химическая связь
Металлическая химическая связь Карбид кремния
Карбид кремния Кетоновые тела
Кетоновые тела Химия в еде
Химия в еде Степени окисления
Степени окисления Алкины
Алкины Презентация на тему Коррозия
Презентация на тему Коррозия  Ренгеноструктурный и рентгеноспектральный анализы
Ренгеноструктурный и рентгеноспектральный анализы Ароматические углеводороды
Ароматические углеводороды Алканы
Алканы Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов
Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Физическая химия, термодинамика
Физическая химия, термодинамика Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 valentnost
valentnost