Слайд 2МЕТАЛЛЫ. СТРОЕНИЕ, СВОЙСТВА, ПРИМЕНЕНИЕ
«Металл суть светлое тело,
которое ковать можно».
Ломоносов М.В.

Слайд 3Содержание
Характеристика элемента-металла по положению в ПСХЭ
Изменение металлических свойств в ПСХЭ
Металлы – простые

вещества
Химическая связь в металлах
5-6.Физические свойства
Металлы – рекордсмены
О применении металлов
Металлы древности на службе у человека
10-11. Из истории сплавов
12-18. Чугун-материал для создания шедевров мирового искусства
О роли металлов
Используемая литература
21. Авторская страница
Слайд 4Характеристика элемента – металла по положению в ПСХЭ Д.И.Менделеева
Li B 1.

Металлы находятся в I-III группе главной
подгруппе (искл. H -1e, Hе-2e, B-3e),
а также в I-VIII группах побочной подгруппе.
Fr At 2. На внешнем энергетическом уровне у
металлов от 1 до 3-х электронов.
3. Ме0 - п е = Ме+п (окисление)
восстановитель
4. Степень окисления металла:
0, +1, +2, +3 (низшая)
+4, +5, +6, +7, +8 (высшая)
Слайд 5 Понятие металлов. Положение в периодической системе.
Металлы – это химические элементы, атомы

которых
способны только отдавать электроны, имеют низкие значения электроотрицательности (от 0,7 до 2,0), им соответствуют простые вещества, металлы.
М е т а л л ы
все s-элементы некоторые р-элементы
(кроме Н и Не) (III-VI групп) І-А, ІІ-А группа Аl, Sn, Bi…
все d- и f-элементы
Cu, Zn, Cr, Mn…
Чем отличается строение атомов металлов от атомов
неметаллов и как это отражается на их химических
свойствах?
Низшая степень окисления Ме = 0, высшая =№ группы (искл.Ι-Б и VΙΙ-Б).
Слайд 6Ряд стандартных электродных потенциалов металлов.
Положение того или иного металла в ряду

напряжений характеризует его способность к окислительно-восстановительным взаимодействиям в водных растворах при стандартных условиях.
Чем ближе металл к началу ряда, тем более сильные восстановительные свойства проявляет металл как простое вещество.
Чем дальше расположен металл в ряду напряжений, тем более сильными окислителями в водном растворе являются его ионы.
Слайд 7Изменение металлических свойств в ПСХЭ
В группах: металлические свойства усиливаются
причина:

1.увеличивается заряд ядра,
2.число электронов на внешнем э.у.
не изменяется
3.радиус атома увеличивается
В периодах:
металлические свойства уменьшаются
причина: 1. увеличивается заряд ядра
2. число электронов на внешнем э.у.
увеличивается
3. радиус атома уменьшается
Слайд 8Металлы –простые вещества
Типы кристаллических решёток металлов
Кубическая Объёмно-центрированная
кубическая
Гранецентрированная Гексагональная
кубическая
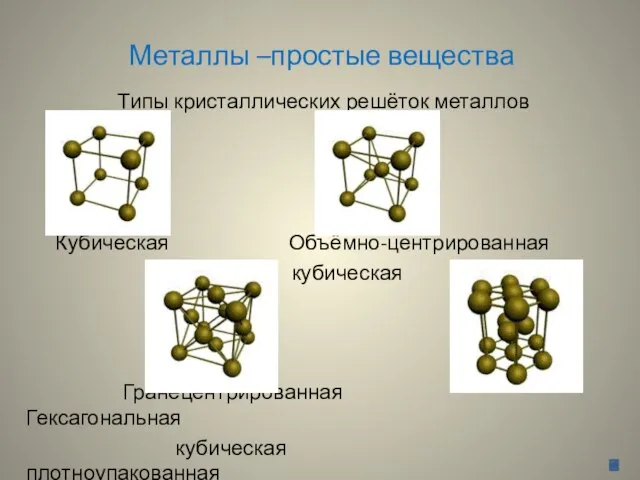
плотноупакованная
Слайд 9Химическая связь в металлах
В узлах кристаллической решётки атом-ионы, между которыми свободно

перемещаются свободные электроны («электронный газ»)
Металлическая связь – связь
между атом-ионами и относительно
свободными электронами за счёт
сил электростатического притяжения
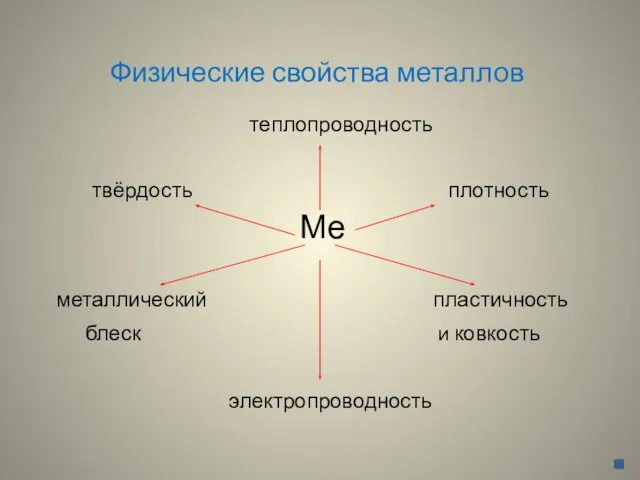
Слайд 10Физические свойства металлов
теплопроводность
твёрдость плотность
Ме
металлический пластичность
блеск и ковкость
электропроводность
Слайд 11 Общие физические свойства металлов.
Пластичность
Au, Ag, Cu, Sn, Pb, Zn, Fe

(уменьшается) Au–0,003 мм
Электропроводность, теплопроводность
Ag, Cu, Au, Аl, Fe (уменьшается)
Классификация металлов:
а) по плотности (лёгкие и тяжелые); б) по температурам плавления (легкоплавкие и тугоплавкие); в) по твёрдости (мягкие и твердые); г) по отношению к магнитному полю (ферромагнетики и парамагнетики)
Слайд 12Физические свойства металлов
(продолжение)
Физические свойства металлов:
пластичность, металлический блеск,
теплопроводность и

электропро-
водность обусловлены наличием в
кристаллической решётке металлов
свободных электронов - «электронный газ».
Слайд 13Металлы - «рекордсмены»
W - самый тугоплавкий
Ag - самый электропроводный
Li

- самый лёгкий
AI - самый распространённый
Cs - самый легкоплавкий
Au - лучший катализатор
Cr - самый твёрдый
Os - самый тяжёлый
Слайд 14Металлы древности на службе
у человека
Семь металлов создал свет
по числу

семи планет …
Алхимики
Золото (Au) – солнце
Серебро (Ag) – луна
Ртуть (Hg) – меркурий
Медь (Cu) – меркурий
Железо (Fe) – марс
Олово (Sn) – юпитер
Свинец (Pb) – сатурн
Слайд 15О применении металлов
Медь была первым металлом,
которым овладел человек. Она

открыла эру металлургии и дала
миру первый сплав. Многие
тысячелетия медь была основой
материальной культуры и искусств
Трудно переоценить уникальную
роль меди в истории
человеческой цивилизации.
Слайд 16«Металлы отверзают недро земное к плодородию; металлы служат нам в ловлении земных

и морских животных для пропитания нашего; металлы облегчают купечество удобною к сему монетою…
И кратко сказать, ни едино художество, ни едино ремесло простое употребление металлов миновать не может»
(М.В.Ломоносов)
Слайд 18 Родий. Стоимость примерно за 1 гр 225 долларов. На Земле его

всего несколько тонн.
Используется, в основном, как автомобильный катализатор
Добывают в ЮАР, встречается в Заполярье, Норильске, на Урале.
Слайд 19Платина – «белое золото»
Стоимость – примерно за 1 гр 70 долларов

Золото
Стоимость – примерно за 1 гр 30 долларов
Слайд 20Иридий
(за 1 гр 17 долларов)
Открыт в 1803 году.
Внешне похож на олово, твердый.

тяжелый.
Иридий идет на изготовление эталонов длины и веса, химических весов, хирургических инструментов.
Слайд 21Осмий
(стоимость за 1 гр 10 000 долларов)
Osme (запах) – греческое слово.
Оно

дало название платиновому металлу осмию 200 лет назад. У него неприятный раздражающий запах, он похож на смесь хлорки и чеснока. В природе чистого осмия не найдено. Металл очень хрупкий, его просто растолочь в обычной ступке.
Используют в фармакологической отрасли в качестве катализатора во многих хим. процессах. Применяют для изготовления деталей измерительных приборов.
Слайд 22КАЛИФОРНИЙ-252
(стоимость за 1 гр – 6 млн.500 тыс. долларов)
В мире его

всего несколько граммов (около 5). Его вырабатывают 2 реактора (США, Россия). Каждый производит около 20-40 мгр в год. 2 грамма металла в 1 секунду выделяет 2,4 биллиарда нейтронов, что соответствует нейтронному потоку обычного реактора (такой эффект можно получить с использованием 200 кг радия).
Калиформий-252 используется в медицине для обработки злокачественных опухолей.
Калифорний может заменить средний атомных реактор.
Слайд 24Активные металлы и металлы средней активности

Слайд 25ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
Металлы – восстановители
Металлы взаимодействуют с :
Кислородом
Неметаллами
Водой (активные)
Кислотами (только

металлы, стоящие до Н в ряду активности металлов)
Солями (условие: металл в соли должен быть менее активным)
Слайд 26Из истории сплавов
Бронза была первым сплавом,
полученным человеком.
Распространение бронзы
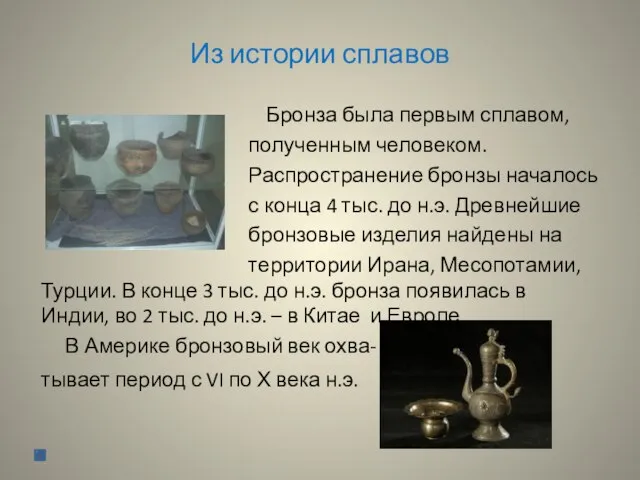
началось
с конца 4 тыс. до н.э. Древнейшие
бронзовые изделия найдены на
территории Ирана, Месопотамии, Турции. В конце 3 тыс. до н.э. бронза появилась в Индии, во 2 тыс. до н.э. – в Китае и Европе.
В Америке бронзовый век охва-
тывает период с VI по Х века н.э.
Слайд 27Из истории сплавов
(продолжение)
В железный век первыми пришли
народы Африки. Они перешагнули

из каменного века в железный
минуя медный и бронзовый. Это
связано с тем, что в Африке железные
руды выходят на поверхность земли.
Африканцы изобрели плавку железа в 600-400
годах до новой эры.
Слайд 28Чугун –материал для создания шедевров мирового искусства
Санкт-Петербург –своеобразный музей, в котором

собрано бесчисленное множество произведений
изобразительного искусства, выполненных из чугуна.
Рассмотрит лишь некоторые
из них – чугунные ограды
дворцов и набережных рек
Санкт – Петербурга.
Слайд 29Чугун – материал для создания шедевров мирового искусства (продолжение)
Воронихинская решётка у Казанского
собора.

Отлита в 1811 году.
(Архитектор Воронихин А.Н.)
Слайд 30Чугун –материал для создания шедевров мирового искусства (продолжение)
Решётка Летнего сада. 36

гранитных колонн, увенчанных вазами и урнами, и тончайшие ажурные звенья, украшенные позолоченными розетками, стали сокровищем мирового искусства.
(Архитекторы Фельтен Ю.М. и Егоров П.Е.)
Слайд 31Чугун – материал для создания шедевров мирового искусства (продолжение)
Ограда Русского

музея
(Михайловского дворца),
1819-1825 г
(Архитектор Росси К.И.)
До 1917 года назывался
музеем Александра III.
Слайд 32 Чугун – материал для создания шедевров мирового искусства (продолжение)
Ограда набережной

реки Фонтанки. Сооружена в 1780-1789 г по проекту архитектора Квасова А.В.
Слайд 33Чугун –материал для создания шедевров мирового искусства (продолжение)
Ограда набережной
реки

Мойки
(1798-1810 годы)
































 Лабораторно-практическое занятие № 5. Неметаллические материалы
Лабораторно-практическое занятие № 5. Неметаллические материалы Электролиз
Электролиз Физическое явление в химии
Физическое явление в химии Алканы: состав, строение, изомерия, номенклатура, получение
Алканы: состав, строение, изомерия, номенклатура, получение Свойства жидкостей
Свойства жидкостей Исследование влияния изменения технических параметров на производительность установки замедленного коксования
Исследование влияния изменения технических параметров на производительность установки замедленного коксования Физическая химия. Лекция 1. Предмет задачи, разделы, методы физической химии. Основные понятия и законы химической
Физическая химия. Лекция 1. Предмет задачи, разделы, методы физической химии. Основные понятия и законы химической Углеводороды: соединения, состоящие из углерода и водорода
Углеводороды: соединения, состоящие из углерода и водорода Знатоки химии. Химия первопричина всех причин
Знатоки химии. Химия первопричина всех причин Химические свойства классов неорганических соединений
Химические свойства классов неорганических соединений Презентация на тему Химия и музыка 11 класс
Презентация на тему Химия и музыка 11 класс  Расшифровка структуры гликозидов
Расшифровка структуры гликозидов Применение некоторых химических веществ. Задание 1
Применение некоторых химических веществ. Задание 1 Знаки химических элементов
Знаки химических элементов Минеральные компоненты молока и молочных продуктов. Макроэлементы
Минеральные компоненты молока и молочных продуктов. Макроэлементы Строение, свойства и функции аминокислот и белков
Строение, свойства и функции аминокислот и белков Диффузия в газах, жидкостях и твердых телах
Диффузия в газах, жидкостях и твердых телах Алкины: получение и применение
Алкины: получение и применение Классификация углеводов: моносахариды, дисахариды, полисахариды. Химическая структура. Свойства и функция углеводов
Классификация углеводов: моносахариды, дисахариды, полисахариды. Химическая структура. Свойства и функция углеводов 10 класс Алкадиены более совершенная (2)
10 класс Алкадиены более совершенная (2) Осуществление цепочки химических превращений. Практическая работа №1
Осуществление цепочки химических превращений. Практическая работа №1 Золото. Физические свойства золота
Золото. Физические свойства золота Строение и номенклатура карбонильных соединений
Строение и номенклатура карбонильных соединений Железо Fe
Железо Fe Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие
Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов 1_
1_ Фенолы. Классификация
Фенолы. Классификация