Слайд 2Лекция №1
Основные понятия
и законы химии
Химия –
наука о веществах

и превращениях их
друг в друга
Слайд 3Основные положения
атомно-молекулярного учения
Все вещества состоят из атомов, молекул или ионов.

Слайд 4Основные положения
атомно-молекулярного учения
Атом
– микроскопическая частица вещества, наименьшая часть химического элемента,

являющаяся носителем его свойств.
Электронейтрален.
Слайд 5Основные положения
атомно-молекулярного учения
Химический элемент
– вид атомов,
имеющих одинаковый заряд ядер.

Слайд 6Основные положения
атомно-молекулярного учения
Молекула
– наименьшая частица вещества, состоящая из соединенных между

собой атомов.
Электронейтральна.
Слайд 7Основные положения
атомно-молекулярного учения
Ион
– электрически заряженная частица, образующаяся при отдаче или

приобретении е.
(Н+ - катион, Сl- - анион)
Слайд 8Основные положения
атомно-молекулярного учения
Атомы одного элемента сходны друг с другом,
но отличаются

от атомов другого элемента.
Слайд 9Основные положения
атомно-молекулярного учения
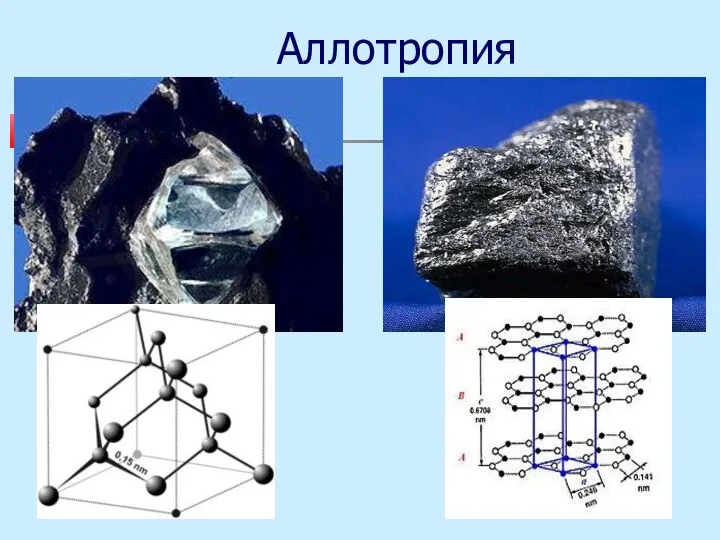
Аллотропия
существование химического элемента в виде нескольких простых веществ

Белый и черный фосфор – различное число атомов;
Алмаз и графит – разное строение кристаллов.
Слайд 12Основные положения
атомно-молекулярного учения
При химическом взаимодействии атомов образуются молекулы:
гомоядерные
(при взаимодействии

атомов одного элемента)
гетероядерные
(при взаимодействии атомов разных элементов).
Слайд 13Основные положения
атомно-молекулярного учения
При физических явлениях молекулы сохраняются,
при химических – разрушаются.

Слайд 14Основные положения
атомно-молекулярного учения
Все молекулы, атомы и ионы находятся в непрерывном движении.
Химические

реакции
заключаются в образовании новых веществ из тех же самых атомов, из которых состоят первоначальные вещества.
Слайд 15Основные величины
Относительная атомная масса элемента (Ar)
– отношение массы его атома

к 1\12 части массы атома углерода (12С)
Относительная молекулярная масса (Mr)
– …его молекулы… Сумма Ar
Величины безразмерные
Слайд 16Основные величины
Количество вещества (n)
– число структурных единиц
(атомов, молекул, ионов),
образующих

это вещество
(моль)
Слайд 17Основные величины
Моль
– количество вещества,
содержащее столько структурных единиц, сколько содержится атомов

в 12 г. углерода (12С).
Слайд 18Основные величины
6,02 х 1023 моль-1
– NА - постоянная Авогадро

Слайд 19Основные величины
Мольная масса вещества (М) – масса одного моль вещества
(численно равна

Аr или Mr) (г\моль)
m = n х M
Слайд 20Основные величины
Эквивалент элемента (Э) – количество элемента, которое соединяется с 1 молем

атома водорода
Эквивалентная масса – масса 1 Э вещества
Эквивалентный объем – V, занимаемый 1 Э вещества
Слайд 21Основные величины
Валентность
– способность атомов элемента
к образованию химических связей
Римские числа

Слайд 22Основные величины
Степень окисления
- условный заряд атома
в соединении
Арабские числа, включая

«0»,
со знаками «+» или «-»
Слайд 23Основные величины
Массовая доля элемента (W):
W = Ar элемента х количество атомов /

Mr соединения
Слайд 24Физические явления
- явления, при которых изменяется форма (ковка металла)
или физическое состояние

веществ (вода в лед или пар)
или образуются новые вещества за счет изменения состава ядер атомов
Слайд 25Химические реакции
– явления, при которых одни вещества превращаются в другие, отличающиеся

от исходных составом и свойствами
(но не происходит изменение состава ядер атомов)
Слайд 26Классификация химических реакций
выделение или поглощение теплоты
Н2 + СL2 = 2 HCL

+ 184,6 кДж (экзотермическая)
N2 + O2 = 2 NO - 180,8 кДж (эндотермическая)
Слайд 27Классификация химических реакций
изменение числа исходных и конечных веществ:
Соединения А+В=АВ
Разложения АВ=А+В
Замещения АВ+С=АС+В
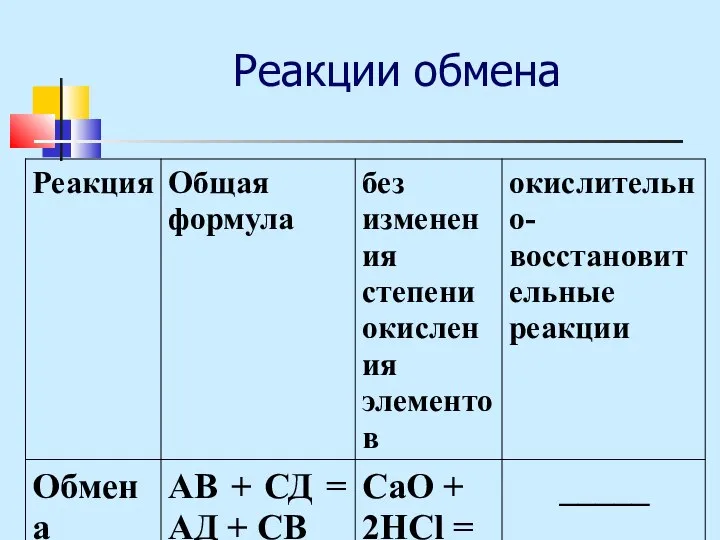
Обмена АВ+СД=АД+СВ

Слайд 32Классификация химических реакций
обратимость реакции
обратимые
необратимые

Слайд 33Обратимые реакции
N2 + O2 ↔ 2NO
обратимая,
т.к. одновременно протекает в двух

взаимно противоположных направлениях
Слайд 34Необратимые реакции
BaCl2 + H2SO4 = BaSO4↓ + 2HCl
(продукты выпадают в виде

осадка)
2KClO3 = 2KCl + 3O2↑
(продукты выделяются в виде газа)
2Mg + O2 = 2MgO
(сопровождается большим выделением Е)































 кулонометрия Дастан
кулонометрия Дастан Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН
Методы отбора проб воды. Оформление и подготовка к анализу, протокол исследования воды, определение рН Кремнийорганическая гипотеза
Кремнийорганическая гипотеза Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Строение атома
Строение атома Галогеноводородные кислоты
Галогеноводородные кислоты Сухой метод определения глюкозы. Глюкометры
Сухой метод определения глюкозы. Глюкометры Современные сплавы на основе циркония
Современные сплавы на основе циркония Комплексное задание по дисциплине основы материаловедения для группы 18
Комплексное задание по дисциплине основы материаловедения для группы 18 Соли
Соли Минералы и горные породы
Минералы и горные породы lektsia_6 (1)
lektsia_6 (1) Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Азотосодержащие соединения: Амины. Аминокислоты. Белки
Азотосодержащие соединения: Амины. Аминокислоты. Белки Угольная кислота и её соли
Угольная кислота и её соли Комплексные соединения
Комплексные соединения Альдегиды, строение и свойства
Альдегиды, строение и свойства Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение
Презентация на тему Алкены. Строение. Изомерия. Химические свойства. Получение  Распределение электронов в атомах
Распределение электронов в атомах Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Пищевые добавки: вред и польза
Пищевые добавки: вред и польза Строение и функции нуклеиновых кислот. Лекция №3
Строение и функции нуклеиновых кислот. Лекция №3 Исследование биодеградации полимерных материалов методом АСМ
Исследование биодеградации полимерных материалов методом АСМ Коррозия металлов
Коррозия металлов Кислород. Физические и химические свойства. Получение
Кислород. Физические и химические свойства. Получение Классификация сложных неорганических веществ. Оксиды
Классификация сложных неорганических веществ. Оксиды Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Стелс-материалы
Стелс-материалы