Содержание
- 2. «Просто знать – мало, знания нужно уметь использовать» Гёте
- 3. Определите валентность углерода: Какие формулы веществ вам знакомы, назовите их. СО2 ;СН4;С4Н10 ;С2Н6 ;С3Н8 IV IV
- 4. Применение метана – СН4. метан – является основным компонентом природных попутных газов и широко используется в
- 5. Напишите формулы метана : а) молекулярную формулу б) электронную формулу в) структурную формулу. Что означает каждая
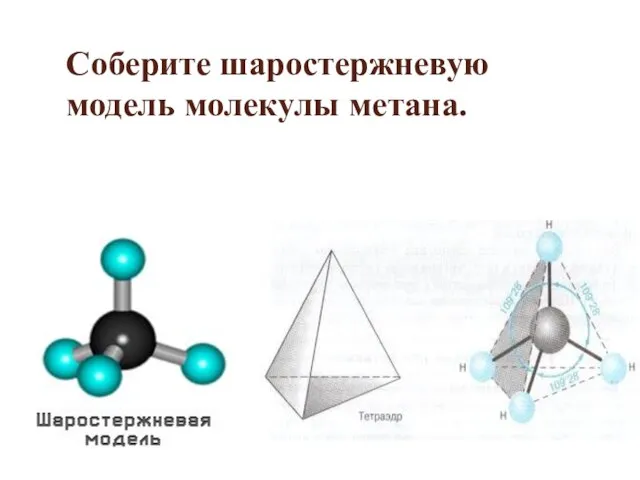
- 6. Соберите шаростержневую модель молекулы метана.
- 7. Вы не смогли определить валентность в С2Н6; С3Н8; С4Н10 . Углеводороды - это органические соединения, состоящие
- 8. Тема урока: «Пространственное строение углеводородов».
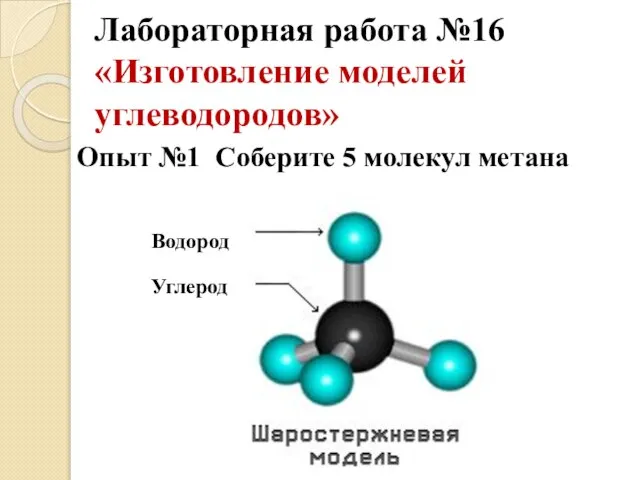
- 9. Лабораторная работа №16 «Изготовление моделей углеводородов» Опыт №1 Соберите 5 молекул метана Углерод Водород
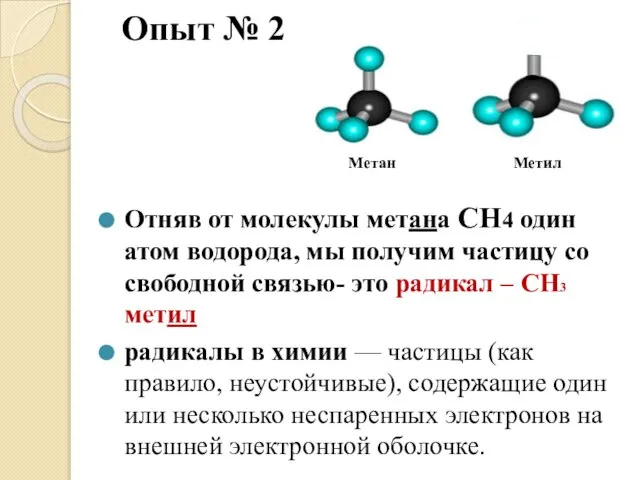
- 10. Опыт № 2 Отняв от молекулы метана СН4 один атом водорода, мы получим частицу со свободной
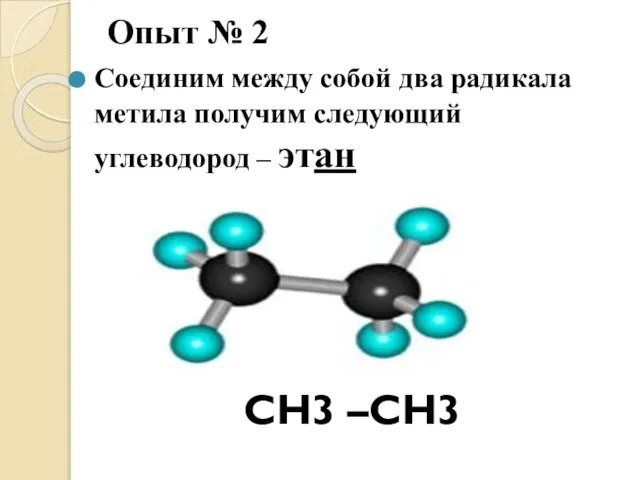
- 11. Опыт № 2 Соединим между собой два радикала метила получим следующий углеводород – этан СН3 –СН3
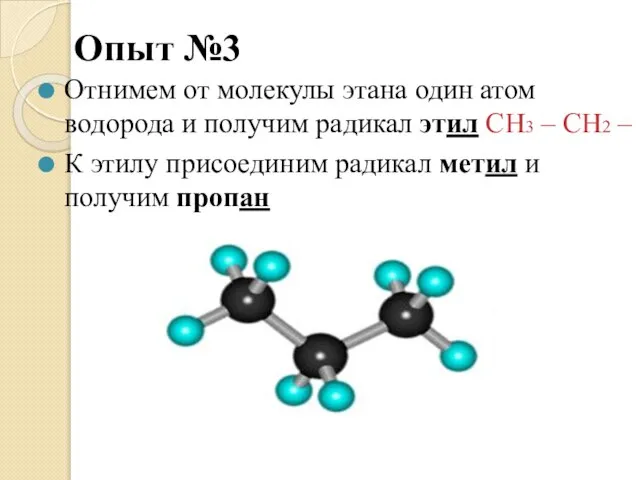
- 12. Опыт №3 Отнимем от молекулы этана один атом водорода и получим радикал этил СН3 – СН2
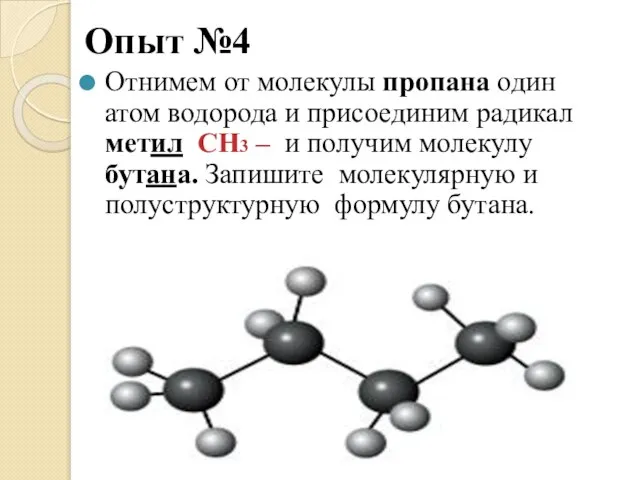
- 13. Опыт №4 Отнимем от молекулы пропана один атом водорода и присоединим радикал метил СН3 – и
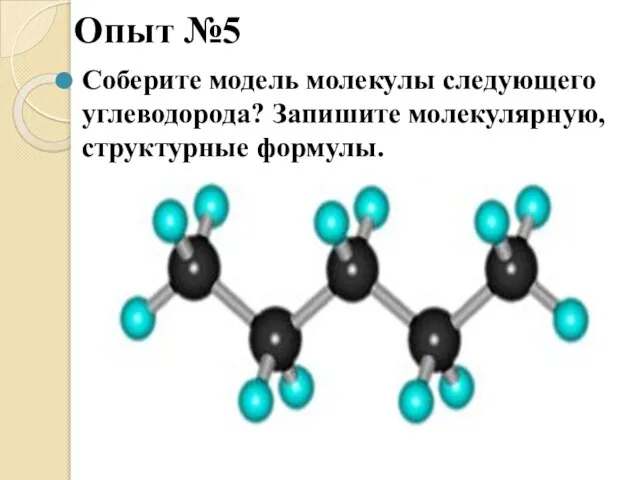
- 14. Опыт №5 Соберите модель молекулы следующего углеводорода? Запишите молекулярную, структурные формулы.
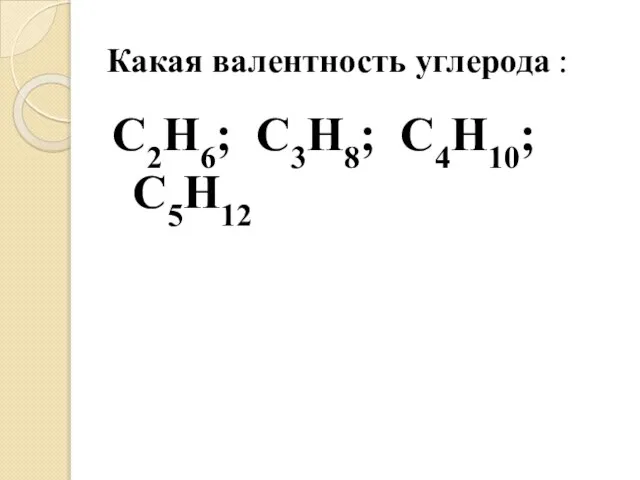
- 15. Какая валентность углерода : С2Н6; С3Н8; С4Н10; С5Н12
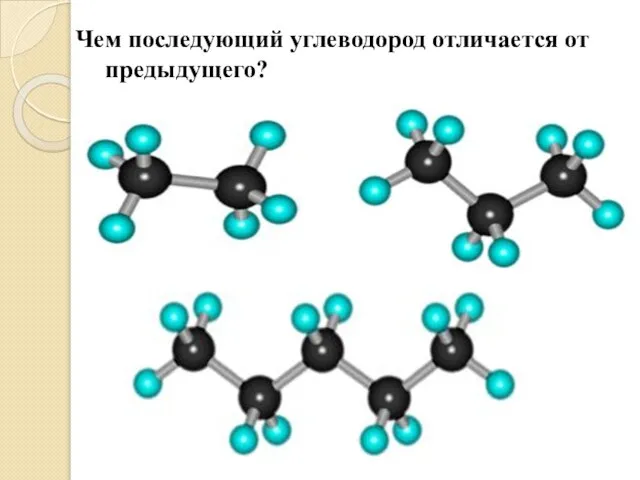
- 17. Чем последующий углеводород отличается от предыдущего?
- 18. Гомологи– это вещества, сходные по строению и свойствам, но отличающиеся друг от друга по составу на
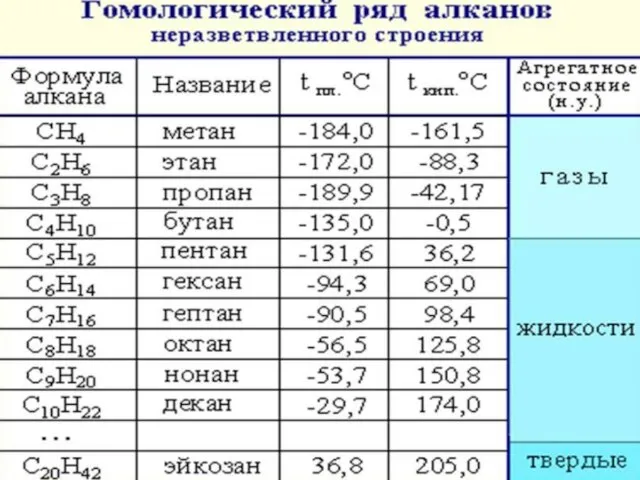
- 19. Углеводороды с общей формулой СпН2п+2 называются предельными углеводородами алканами. У этих веществ только простые одинарные связи
- 21. Применение углеводородов
- 22. В книге А. Азимова«Мир углерода» 1978 г. - Известно 1.700.000 органических веществ. 1995 г.- 10 млн.
- 23. Основные положения теории строения органических соединений А.М. Бутлерова Атомы в молекулах соединены в определенной последовательности, соответствии
- 24. Александр Михайлович Бутлеров Русский химик, родился в Татарстане Алексеевском районе 1828г. Профессор химии Казанского университета (1857-1868).
- 25. Проверим полученные знания. 1) Гомологом метана является углеводород: А) С2Н4 Б) С3Н8 В) С4Н8 Г) С2Н2
- 26. Домашнее задание Сообщение. Где и в каком виде предельные углеводороды встречаются в природе? Стр148-151прочитать,выучить формулы алканов,
- 27. "Химия - это область чудес, в ней скрыто счастье человечества, величайшие завоевания разума будут сделаны именно
- 29. Скачать презентацию















 Полисахариды
Полисахариды Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Замедленное коксование нефтяного сырья
Замедленное коксование нефтяного сырья Водные растворы электролитов
Водные растворы электролитов Посвящение в химики
Посвящение в химики Открытый урок на тему: Степень окисления
Открытый урок на тему: Степень окисления Презентация на тему Скорость химических реакций
Презентация на тему Скорость химических реакций  Задача на химическое равновесие
Задача на химическое равновесие Спирты. Классификация спиртов
Спирты. Классификация спиртов Порох: из грязи в князи
Порох: из грязи в князи Alkalické kovy
Alkalické kovy Превращения серосодержащих соединений
Превращения серосодержащих соединений Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи
Понятие аналитической химии, её цели и задачи. Химический анализ, его задачи получение Ме презентация
получение Ме презентация Органика из аптеки
Органика из аптеки Азот
Азот Презентация на тему Решение задач на смеси, сплавы, растворы
Презентация на тему Решение задач на смеси, сплавы, растворы  Металл XXI века титан
Металл XXI века титан Всё о нефти. Часть 5
Всё о нефти. Часть 5 Закон сохранения массы и энергии
Закон сохранения массы и энергии Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19 Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок
Фізика гірських порід і процесів. Хімічні зв'язки в мінералах. Іонний зв'язок Презентация на тему Подгруппа углерода
Презентация на тему Подгруппа углерода  Получение и химические свойства металлов
Получение и химические свойства металлов Синтез олигомеров этиленгликоля и терефталевой кислоты
Синтез олигомеров этиленгликоля и терефталевой кислоты Презентация на тему Признаки реакций
Презентация на тему Признаки реакций  Косметические средства. Виды, состав и влияние на организм
Косметические средства. Виды, состав и влияние на организм Каучук. История открытия каучука
Каучук. История открытия каучука