Слайд 2Гидролиз солей.
Гидролиз – это реакция обменного разложения веществ водой.

Слайд 3Гидролиз органических веществ.
1. Гидролиз галогеналканов.
С2Н5Сl + Н2О →С2Н5ОН + НСl
2. Гидролиз
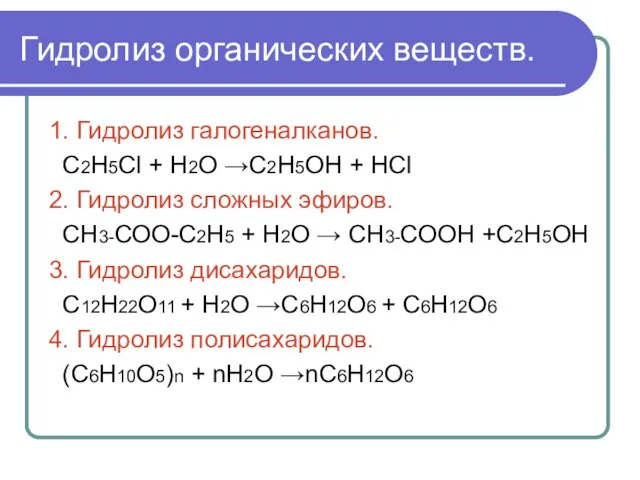
сложных эфиров.
СН3-СОО-С2Н5 + Н2О → СН3-СООН +С2Н5ОН
3. Гидролиз дисахаридов.
С12Н22О11 + Н2О →С6Н12О6 + С6Н12О6
4. Гидролиз полисахаридов.
(С6Н10О5)n + nН2О →nС6Н12О6
Слайд 4Гидролиз неорганических веществ.
Гидролизу подвергаются растворы солей. Следовательно, водные растворы солей имеют разные

значения рН и различные типы сред:
Кислотную (рН<7).
Щелочную (рН>7).
Нейтральную (рН=7).
Слайд 5Классификация солей.
Любую соль можно представить как продукт взаимодействия основания с кислотой.
В зависимости

от силы основания и кислоты можно выделить 4 типа солей:
1. Соли, образованные сильным основанием и слабой кислотой (КСN, NaCH3COO).
2. Соли, образованные сильной кислотой и слабым основанием (СuCl2, FeSO4, Mn(NO3)2.
Слайд 6Классификация солей.
3. Соли, образованные слабой кислотой и
слабым основанием
(NH4CN, Cu(CH3COO)2).
4.

Соли, образованные сильной кислотой и сильным основанием
(NaCl, K2SO4, BaI2).
Слайд 7Соли, образованные сильным основанием и слабой кислотой.
NaCN + Н2О ↔ NaOH

+ HCN
NaCN ↔Na+ + CN‾
Н2О ↔ OH ‾ + H+
Полное ионное уравнение гидролиза:
Na+ + CN¯ + Н2О ↔ Na+ + OH¯ + HCN
Сокращённое уравнение гидролиза:
CN¯ + Н2О ↔ OH¯ + HCN
рн >7, среда щелочная, гидролиз по аниону.
Слайд 8Соли, образованные сильным основанием и слабой кислотой.
Гидролиз по аниону:
Обратимый процесс.
Химическое равновесие смещено

влево.
Реакция среды - щелочная, рН>7.
При гидролизе солей, образованных слабыми многоосновными кислотами образуются кислые соли.
Слайд 9Соли, образованные сильной кислотой и слабым основанием.
NH4Cl + H2O ↔ NH3·H2О +

НСl
NH4Cl ↔ NH4+ + Cl¯
Н2О ↔ OH¯ + H+
Полное ионное уравнение гидролиза:
NH4+ + Cl¯ + Н2О ↔ NH3 · H2О + H+ + Cl¯
Сокращённое уравнение гидролиза:
NH4+ + Н2О ↔ NH3 · H2О + H+
рн <7, среда кислотная, гидролиз по
катиону.
Слайд 10Соли, образованные сильной кислотой и слабым основанием.
Гидролиз по катиону:
Обратимый процесс.
Химическое равновесие смещено

влево.
Среда кислотная, рН<7.
Слайд 11Соли, образованные слабой кислотой и слабым основанием.
NH4СН3СОО + H2O ↔ СН3СООН

+ NH3 · H2О
NH4СН3СОО ↔ NH4 + + СН3СОО¯
Н2О ↔ OH¯ + H +
Ионное уравнение гидролиза:
NH4 + + СН3СОО¯ + Н2О ↔ NH3 · H2О + СН3СООН
рн = 7, среда нейтральная, гидролиз по
катиону и по аниону.
Слайд 12Соли, образованные слабой кислотой и слабым основанием.
Гидролиз по катиону и по аниону.
Химическое

равновесие смещено вправо.
Реакция среды или нейтральная, или слабокислая, или слабощелочная, что зависит от констант диссоциации кислоты и основания.
Гидролиз может быть необратимым, если хотя бы один из продуктов реакции гидролиза уходит из сферы реакции.
Слайд 13
Соли, образованные сильной кислотой и сильным основанием.
КСl + H2O ↔

КСl ↔ К + + Сl¯
Н2О ↔ OH¯ + H +
Все ионы остаются в растворе – гидролиз не происходит. Среда нейтральная, рН =7, т.к.
концентрации катионов водорода и гидроксид - анионов в растворе равны, как в чистой воде.
Слайд 14Гидролиз солей.
Гидролиз можно усилить:
Добавить воды.
Нагреть раствор (увеличится диссоциация воды).
Связать один из продуктов

гидролиза в труднорастворимое соединение или удалить один из продуктов в газовую фазу.













 Практико-ориентированные задачи по химии для студентов гуманитарных специальностей
Практико-ориентированные задачи по химии для студентов гуманитарных специальностей Электролитическая диссоциация
Электролитическая диссоциация МОУ СОШ №3 г. Хвалынска Саратовской области Тема: Ковалентная полярная связь Учитель химии и биологии Высшей квалификационно
МОУ СОШ №3 г. Хвалынска Саратовской области Тема: Ковалентная полярная связь Учитель химии и биологии Высшей квалификационно Органическая химия
Органическая химия Кристаллы. Формирование кристаллов
Кристаллы. Формирование кристаллов Двойственная природа электрона. Урок 33-34
Двойственная природа электрона. Урок 33-34 Zirconium Dioxide
Zirconium Dioxide Золото
Золото Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Коррозия металлов
Коррозия металлов Водородный показатель Ph растворов
Водородный показатель Ph растворов Минералы и их свойства
Минералы и их свойства Ароматические углеводороды
Ароматические углеводороды Общая характеристика галогенов на основе положения химических элементов в периодической системе
Общая характеристика галогенов на основе положения химических элементов в периодической системе презентация арены 1
презентация арены 1 Коштовне каміння
Коштовне каміння Альдегиды и кетоны
Альдегиды и кетоны Разработка электронных образовательных ресурсов в естественнонаучном образовании бакалавров направления Химия
Разработка электронных образовательных ресурсов в естественнонаучном образовании бакалавров направления Химия Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Углеводороды
Углеводороды Превращения серосодержащих соединений
Превращения серосодержащих соединений Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Презентация на тему Алмаз, графит и фуллерен
Презентация на тему Алмаз, графит и фуллерен  Наука химия. Интеллектуальная игра. 5-8 класс
Наука химия. Интеллектуальная игра. 5-8 класс Металдар мен қорытпалардың құрылысы және қасиеттері
Металдар мен қорытпалардың құрылысы және қасиеттері Антитела. Что такое антитела?
Антитела. Что такое антитела? Развитие творческих способностей школьников на уроках химии
Развитие творческих способностей школьников на уроках химии Пищевая сода
Пищевая сода