Содержание
- 2. Определения и классификация Номенклатура Физические свойства Способы получения Химические свойства соли
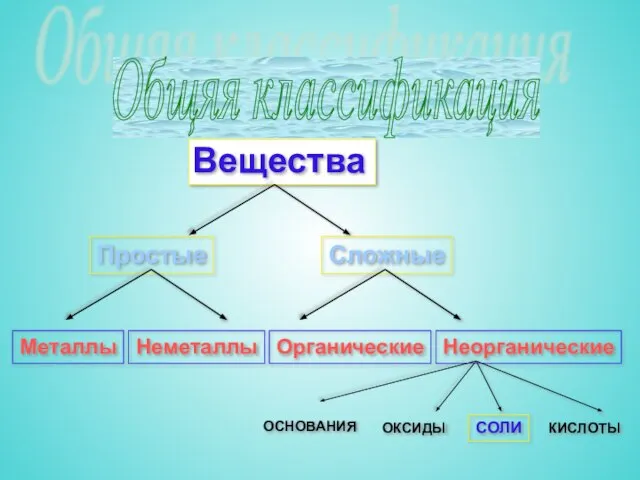
- 3. Общяя классификация Простые Сложные Металлы Неметаллы Органические Неорганические ОСНОВАНИЯ ОКСИДЫ СОЛИ КИСЛОТЫ
- 4. Классификация солей соли средние кислые основные двойные смешанные комплексные гидратные
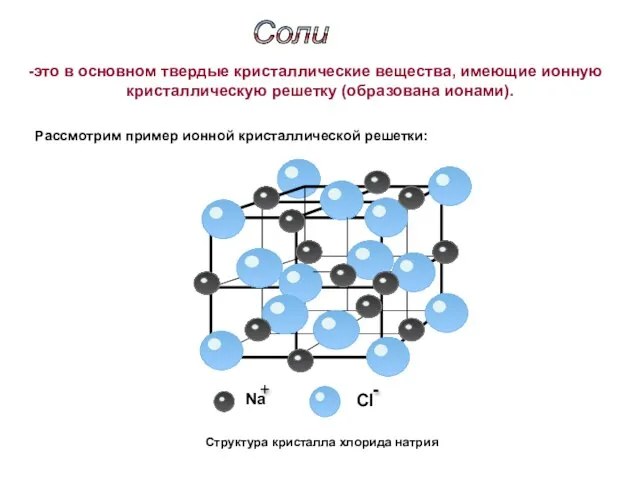
- 5. Структура кристалла хлорида натрия Соли это в основном твердые кристаллические вещества, имеющие ионную кристаллическую решетку (образована
- 6. Определения типов солей Соли состоят из атомов металла и атомов кислотного остатка. Основные типы солей это:
- 7. Примеры солей Средние соли: Ca(NO3)2; K2SO4; Al(NO3)3. Кислые соли: KHSO4; MgHPO4; NaSO3. Основные соли: LiOHPO4; CaOHP2O
- 8. а) К основным солям б) К смешанным солям в) К комплексным солям г) К двойным солям
- 9. Номенклатура солей Название солей образуется из названия аниона, за которым следует название катиона. Для солей бескислородных
- 10. Как правильно назвать соль: KCl? а) Хлор калия б) Хлорид калия в) Хлорат калия г) Хлорит
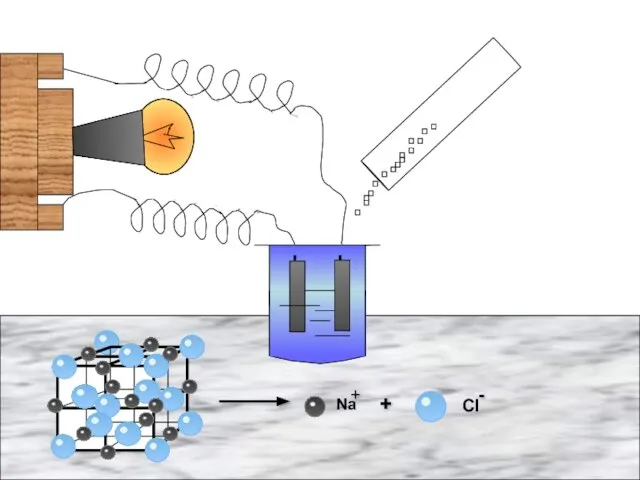
- 11. Физические свойства солей Основное свойство солей- это то, что они являются электролитами. Электролиты- это вещества, растворы
- 12. +
- 13. Способы получения солей Соли получают разнообразными способами. Вот примеры некоторых из них: а) Взаимодействием двух простых
- 14. Химические свойства солей Соли обладают общими химическими свойствами за счет сходного иона. Пример: Взаимодействие солей с
- 15. С каким из металлов будет взаимодействовать соль MgS? а) Ca б) Mn в) Zn г) Ni
- 16. Гидролиз солей Существуют четыре типа гидролиза: Соль образована ионом сильного основания и ионом слабой кислоты. 2)Соль
- 17. План составления гидролиза: 1) Проверить соль на растворимость по таблице растворимости. 2) Определить, есть ли в
- 18. Первый тип гидролиза Пример:
- 19. Второй тип гидролиза Пример:
- 20. Третий тип гидролиза В этом случае гидролиз необратим. Примеры:
- 21. Четвертый тип гидролиза NaCl Растворимые соли, образованные сильной кислотой и сильным основанием, в воде не гидролизируются.
- 22. Факторы, влияющие на гидролиз 1) Повышение температуры приводит к смещению равновесия в сторону продуктов реакции. 2)Увеличение
- 23. КОНЕЦ! P.S. Надеюсь, Вам понравилось.
- 24. ВЕРНО
- 25. Не верно
- 26. Не верно
- 27. ВЕРНО
- 28. ВЕРНО
- 30. Скачать презентацию
























 Неорганический мозговой штурм
Неорганический мозговой штурм Альдегиды и кетоны
Альдегиды и кетоны Проектная деятельность учащихся по химии
Проектная деятельность учащихся по химии Химия вокруг нас и для нас
Химия вокруг нас и для нас Уравнение материального баланса технологического процесса. (Лекция 3)
Уравнение материального баланса технологического процесса. (Лекция 3) Кинетическое лимитирование роста и жизненные стратегии микроорганизмов
Кинетическое лимитирование роста и жизненные стратегии микроорганизмов Алкадиены
Алкадиены Кинетика гомогенных реакций
Кинетика гомогенных реакций Презентация на тему Основные положения МКТ
Презентация на тему Основные положения МКТ 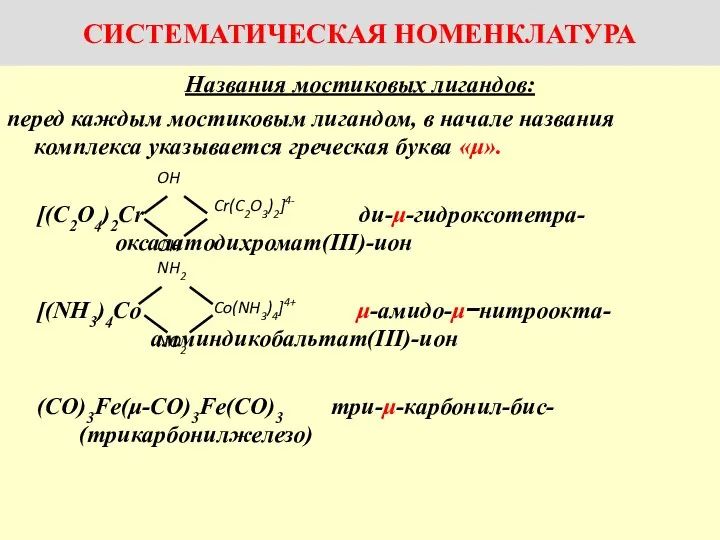 Названия комплексов с мостиковыми лигандами
Названия комплексов с мостиковыми лигандами Викторин. Диалог химии и медицины
Викторин. Диалог химии и медицины Урок изучения и первичного усвоения знаний с элементами исследования на тему: «Окислительно-восстановительные свойства соединен
Урок изучения и первичного усвоения знаний с элементами исследования на тему: «Окислительно-восстановительные свойства соединен Наноматериалы и нанотехнологии
Наноматериалы и нанотехнологии Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Чистые вещества и смеси
Чистые вещества и смеси Строение вещества. Эксперименты
Строение вещества. Эксперименты Физико-химические основы получения лекарственных препаратов
Физико-химические основы получения лекарственных препаратов Спирты. Методы получения
Спирты. Методы получения Производственно-торговая компания ООО СОЖ Синтез-Набережные Челны
Производственно-торговая компания ООО СОЖ Синтез-Набережные Челны Строение атома
Строение атома Рівноваги у розчинах електролітів
Рівноваги у розчинах електролітів Менделеев Дмитрий Иванович
Менделеев Дмитрий Иванович Химическая картина мира
Химическая картина мира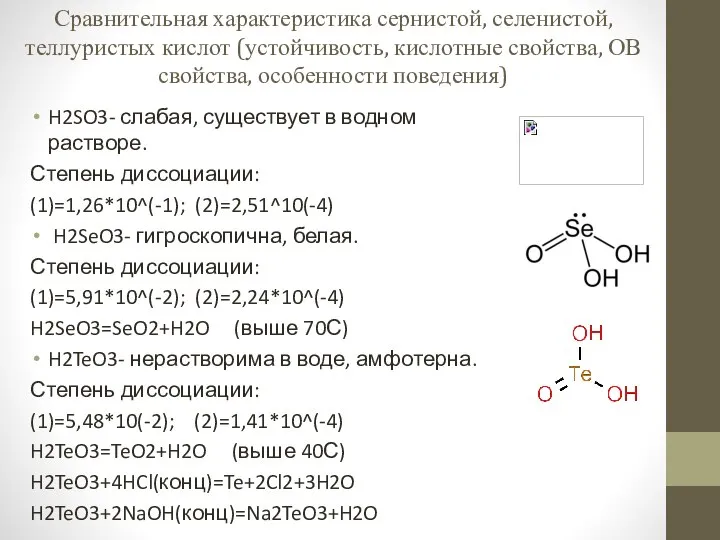 Сравнительная характеристика сернистой, селенистой, теллуристых кислот
Сравнительная характеристика сернистой, селенистой, теллуристых кислот Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Биологическое окисление
Биологическое окисление Презентация на тему Минеральные удобрения
Презентация на тему Минеральные удобрения  Художественная обработка металла
Художественная обработка металла