Содержание
- 2. Кислоты- электролиты, при диссоциации которых образуются катионы водорода и анионы кислотных остатков HCL H++CL- H2SO4 3H++PO43-
- 3. Классификация кислот
- 4. Типичные реакции кислот Кислота + основание = соль + вода H2SO4 +2 NaOH = Na2SO4 +
- 5. ПРОВЕРЬ СЕБЯ 1.Формула кислоты это: а) NaOH в) CuCL2 б) HCL г) SO3 2. Лакмус в
- 7. Скачать презентацию
Слайд 2Кислоты-
электролиты, при диссоциации которых образуются катионы водорода и анионы кислотных остатков
HCL
Кислоты- электролиты, при диссоциации которых образуются катионы водорода и анионы кислотных остатков HCL

H++CL-
H2SO4 3H++PO43-
Слайд 3Классификация кислот
Классификация кислот

Слайд 4Типичные реакции кислот
Кислота + основание = соль + вода
H2SO4 +2 NaOH
Типичные реакции кислот
Кислота + основание = соль + вода
H2SO4 +2 NaOH

= Na2SO4 + 2H2O
2H+ +2OH- = 2H2O
Кислота + оксид металла = соль + вода
CuO + 2 HCL = CuCL2 + H2O
CuO + 2H+ = H2O + Cu2+
Кислота + металл = водород + соль
2HCL +Zn = ZnCL2 + H2
2H+ + Zn0 =Zn2+ +H2
Условия: - в ряду напряжений металл должен стоять до водорода
- в результате реакции должна получиться растворимая соль
Кислота + соль = новая кислота + новая соль
Условия: - в результате реакции должны получиться газ, осадок
или вода.
BaCL2 + H2SO4 = BaSO4 + 2HCL
Ba2+ + SO42- = BaSO4
2H+ +2OH- = 2H2O
Кислота + оксид металла = соль + вода
CuO + 2 HCL = CuCL2 + H2O
CuO + 2H+ = H2O + Cu2+
Кислота + металл = водород + соль
2HCL +Zn = ZnCL2 + H2
2H+ + Zn0 =Zn2+ +H2
Условия: - в ряду напряжений металл должен стоять до водорода
- в результате реакции должна получиться растворимая соль
Кислота + соль = новая кислота + новая соль
Условия: - в результате реакции должны получиться газ, осадок
или вода.
BaCL2 + H2SO4 = BaSO4 + 2HCL
Ba2+ + SO42- = BaSO4
Слайд 5ПРОВЕРЬ СЕБЯ
1.Формула кислоты это:
а) NaOH в) CuCL2
б) HCL г) SO3
2.
ПРОВЕРЬ СЕБЯ
1.Формула кислоты это:
а) NaOH в) CuCL2
б) HCL г) SO3
2.

Лакмус в растворе, полученном при взаимодействии оксида серы (IV) с водой:
а) синий в) фиолетовый
б) красный г) малиновый
3. С раствором серной кислоты взаимодействует:
а) оксид магния в) оксид фосфора
б) оксид углерода г) сера
4. Соляная кислота не взаимодействует с металлом:
а) алюминием в) серебром
б) железом г) цинком
5. Пара ионов, которая может одновременно находится в растворе:
а) H+ и SiO3 в) Н+ и SO42-
б) Cu 2+ и ОН- г) Ag+ и CL-
6. Пара веществ взаимодействующих друг с другом:
а) H2SO4 u SiO2 в) Сu u H3PO
б) CuO u Na2O г) НСL u NaOH
а) синий в) фиолетовый
б) красный г) малиновый
3. С раствором серной кислоты взаимодействует:
а) оксид магния в) оксид фосфора
б) оксид углерода г) сера
4. Соляная кислота не взаимодействует с металлом:
а) алюминием в) серебром
б) железом г) цинком
5. Пара ионов, которая может одновременно находится в растворе:
а) H+ и SiO3 в) Н+ и SO42-
б) Cu 2+ и ОН- г) Ag+ и CL-
6. Пара веществ взаимодействующих друг с другом:
а) H2SO4 u SiO2 в) Сu u H3PO
б) CuO u Na2O г) НСL u NaOH
- Предыдущая
Дательный падеж. АдресатСледующая -
Одночлены и их свойства. Тест Презентация на тему Синтетические материалы
Презентация на тему Синтетические материалы  Автомобильные бензины. Свойства топлив
Автомобильные бензины. Свойства топлив Вариативные задачи по химии различных типов в тестовой форме
Вариативные задачи по химии различных типов в тестовой форме Согласованное и несогласованное действие заместителей в бензольном кольце
Согласованное и несогласованное действие заместителей в бензольном кольце obschaya_kharakteristika_prostykh_alifaticheskikh_efirov
obschaya_kharakteristika_prostykh_alifaticheskikh_efirov Техника безопасности на уроках химии
Техника безопасности на уроках химии 11 типы связей
11 типы связей Химическая связь. Типы кристаллических решёток
Химическая связь. Типы кристаллических решёток Презентация на тему Хлор - физиологическая и патологическая роль в организме человека
Презентация на тему Хлор - физиологическая и патологическая роль в организме человека  Век медный, бронзовый, железный
Век медный, бронзовый, железный Ministry of Education and Science of the Russian Federation
Ministry of Education and Science of the Russian Federation Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Химические реакции
Химические реакции Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Физико-химические основы получения лекарственных препаратов
Физико-химические основы получения лекарственных препаратов Презентация по Химии "Углекислый газ"
Презентация по Химии "Углекислый газ"  Кислоты. Тест
Кислоты. Тест Основные классы неорганических веществ
Основные классы неорганических веществ Основы химической термодинамики
Основы химической термодинамики Молекулы и атомы. Относительная атомная масса
Молекулы и атомы. Относительная атомная масса 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Пищевые кислоты
Пищевые кислоты Минеральные вещества и здоровье
Минеральные вещества и здоровье Потенциометрический анализ, титрование
Потенциометрический анализ, титрование 4. Диаграмма железо-углерод
4. Диаграмма железо-углерод Минерал гранат
Минерал гранат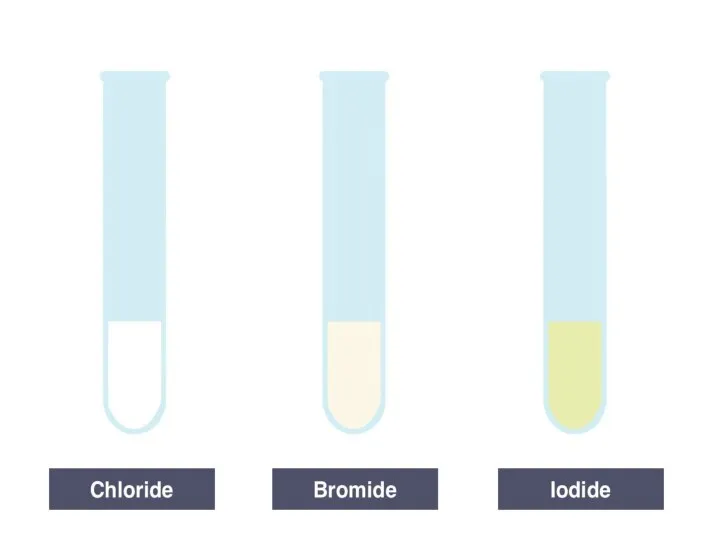 Определение галогенид-ионов в водном растворе. Лабораторный опыт
Определение галогенид-ионов в водном растворе. Лабораторный опыт Кислоты
Кислоты