Содержание
- 2. ЛЕКЦІЯ 1 Гірські породи - природні утворення, що складають різноманітні геологічні тіла, з яких побудована земна
- 3. МІНЕРАЛОМ називають однорідне за хімічним складом і фізичними властивостями кристалічне тіло, що утворюється в результаті фізико-хімічних
- 4. Хімічні і фізико-хімічні процеси утворення мінералів поділяють на три групи Ендогенні (внутрішні) або гіпогенні (глибинні) процеси
- 5. Ендогенні процеси Основними параметрами ендогенного мінералоутворення є хімічні елементи, їх концентрація і термодинамічні умови. Залежно від
- 6. Магматичні процеси протікають у земній корі на відносно великих глибинах. Магма, що являє в основному складний
- 7. Пегматитові процеси Після завершення мінералоутворення в кожному температурному діапазоні ( процес мінералоутворення є безперервним) в магмі
- 8. Гідротермальні процеси Гідротермальні родовища в залежності від температури і мінеральної спеціалізації діляться на високотемпературні (800-600 К),
- 9. Пневматолітові процеси Гази, які супроводжують виверження вулканів, виділяються не тільки з кратера, а й на схилах
- 10. Екзогенні процеси Всі процеси руйнування, що протікають на поверхні земної кори, називаються процесами вивітрювання, які поділяються
- 11. Фізичне вивітрювання характерне для пустель з високою амплітудою коливання добових температур, що досягають іноді 60 °С.
- 12. Хімічне вивітрювання пов'язують, в основному, з дією води, що міститься в ґрунті і атмосфері. Вода атмосфери
- 13. Процеси відновлення є зворотними процесам окислення. Такі процеси протікають, якщо порода містить сірководень або органічні кислоти.
- 14. Метаморфічні процеси На відміну від метасоматизму це істотно ізохімічний процес, при якому хімічний склад вихідних порід
- 15. До простих принципів можна віднести збереження або зміну хімічного складу порід. До таких відносно простих принципів
- 16. Але найбільші складності викликають два основні напрямки поділу метаморфічних процесів: 1) за фізико-хімічними умовами (головним чином
- 17. Виділяють наступні види метаморфізму: термічний, дислокаційний, контактовий, регіональний, ударний, прогресивний, регресивний, статичний, кінетичний, ізохімічний, алохімічний, магматичний,
- 18. ЛЕКЦІЯ 2 Хімічні зв'язки в мінералах Іонний зв'язок Іонний зв'язок називають іноді гетерополярним зв'язком (грец. «гетеро"
- 19. Ковалентний (гомеополярний) зв'язок Зв'язок атомів за допомогою електронних пар називається ковалентним або атомним. Цей зв'язок іноді
- 20. До речовин з ковалентним зв'язком відносяться : більшість органічних сполук; тверді і рідкі речовини, у яких
- 21. Металевий зв'язок Валентних електронів у металів завжди в кілька разів менше, ніж у найближчих сусідніх атомів
- 22. Вандерваальсові (міжмолекулярні) зв'язки Поширеною назвою сил міжмолекулярної взаємодії є вандерваальсові сили (в честь голландського фізика Я.Д.
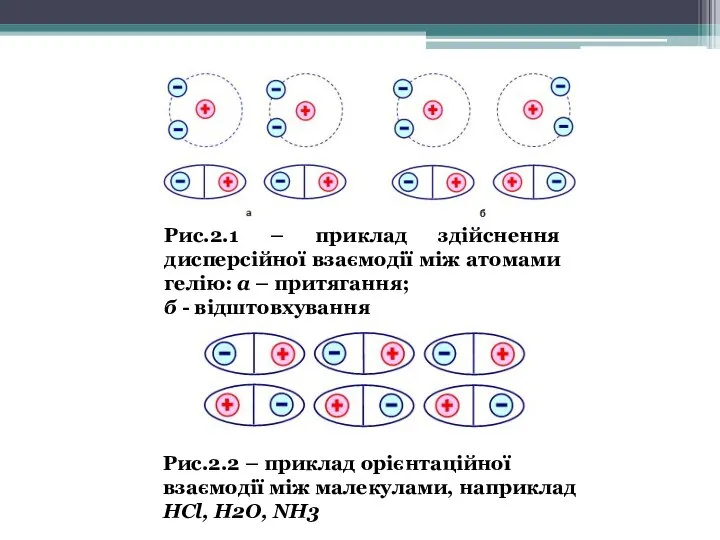
- 23. Рис.2.2 – приклад орієнтаційної взаємодії між малекулами, наприклад НСl, H2O, NH3 Рис.2.1 – приклад здійснення дисперсійної
- 24. Водневий зв'язок Цей зв'язок виникає в тому випадку, коли атом водню пов'язаний з сильно електронегативним атомом,
- 25. Кристали. Типи кристалічних решіток Всі тверді речовини можна поділити на кристалічні або аморфні, в залежності від
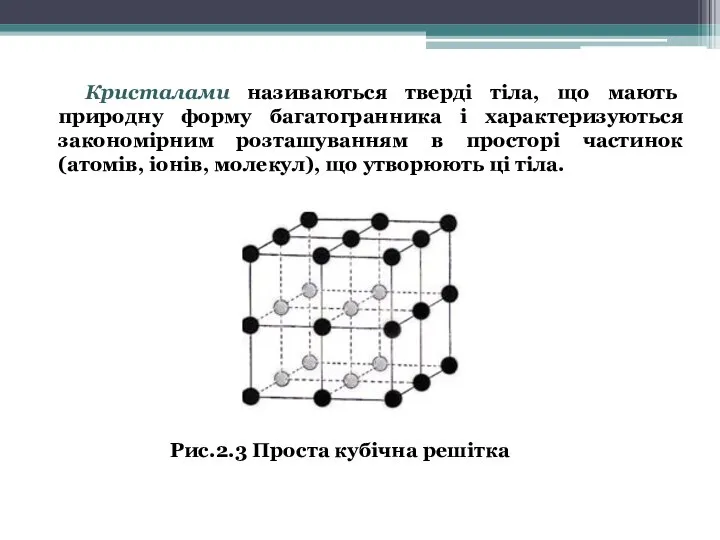
- 26. Кристалами називаються тверді тіла, що мають природну форму багатогранника і характеризуються закономірним розташуванням в просторі частинок
- 27. Кристалічним тілом називають тверде тіло, у якого розташування атомів періодично повторюється і поверхневі межі якого (якщо
- 28. Основні особливості кристалічної речовини визначаються його внутрішньою будовою. Кристали ділять на наступні групи : 1 –
- 29. 3 – металеві кристали мають в якості елементів решітки позитивні іони металів, які пов'язані між собою
- 30. Деякі загальні властивості кристалічних решіток Однорідність проявляється в тому, що два однакових елементарних об'єми, взяті в
- 31. Здатність самоогранятися - властивість кристалів утворювати межі при вільному їх зростанні. Відхилення від стехіометрії. Якщо в
- 33. Скачать презентацию




























 Химические реакции в органической химии
Химические реакции в органической химии Графический диктант. Азот и Аммиак
Графический диктант. Азот и Аммиак Неньютоновская жидкость
Неньютоновская жидкость Язык естествознания. Химия
Язык естествознания. Химия Презентация на тему Химия и сельское хозяйство Пестициды
Презентация на тему Химия и сельское хозяйство Пестициды  Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах
Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах 12 принципов зелёной химии
12 принципов зелёной химии Алканы
Алканы Химическая связь. Строение вещества
Химическая связь. Строение вещества Диены. Понятие о диенах
Диены. Понятие о диенах Минералы и горные породы
Минералы и горные породы Типы химических реакций. 8 класс
Типы химических реакций. 8 класс Кварцевые пески
Кварцевые пески Вода как хладагент (R718)
Вода как хладагент (R718) Кроссворд по теме Металлы
Кроссворд по теме Металлы Оксиды
Оксиды Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Щелочные металлы
Щелочные металлы Органическая химия
Органическая химия Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна
Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна Кислород – основа жизни?
Кислород – основа жизни? Урок-путешествие по теме «Первоначальные химические понятия»
Урок-путешествие по теме «Первоначальные химические понятия» Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии Введение в органическую химию. Состав и структура органических веществ
Введение в органическую химию. Состав и структура органических веществ Многоатомные спирты
Многоатомные спирты Строение атома. Планетарная модель атома Резерфорда
Строение атома. Планетарная модель атома Резерфорда Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"