Содержание
Слайд 2Опыт 1. Получение аммиака.
1) Возьмите два кристаллических вещества: хлорид аммония и гидроксид
Опыт 1. Получение аммиака.
1) Возьмите два кристаллических вещества: хлорид аммония и гидроксид

кальция. Какие вещества образуются при взаимодействии хлорида аммония и гидроксида кальция? Напишите уравнение реакции.
2) Соберите прибор для получения аммиака.
3) Получите аммиак и соберите его в пробирку. Для этого равные объемы хлорида аммония и гидроксида кальция перемешайте в ступке и поместите в сухую пробирку. Заполните смесью 1/3 пробирки. Осторожно нагрейте смесь.
4) Назовите четыре физических свойства аммиака, которые вы обнаружили в этом опыте.
Опыт 2. Растворение аммиака в воде.
1) Пробирку с аммиаком закройте пробкой. Не переворачивая пробирку с аммиаком, опустите её в кристаллизатор с водой. Под водой откройте пробку. После заполнения пробирки водой закройте под водой её отверстие пробкой и выньте пробирку из воды. Опишите наблюдения и объясните их. Обобщите, какими физическими свойствами обладает аммиак.
2) К полученному раствору аммиака прилейте каплю раствора фенолфталеина. Объясните наблюдения. Сделайте вывод, к какому классу соединений относится продукт взаимодействия аммиака с водой. Запишите уравнение реакции.
Опыт 3. Взаимодействие раствора аммиака с кислотами.
1) Проведите реакцию гидроксида аммония с раствором соляной кислоты: в пробирку с раствором аммиака и раствором фенолфталеина прилейте по каплям раствор соляной кислоты до исчезновения малиновой окраски. Объясните наблюдения, запишите ионные уравнения реакций (полное и сокращенное). Сформулируйте вывод о свойствах водного раствора аммиака.
2) Соберите прибор для получения аммиака.
3) Получите аммиак и соберите его в пробирку. Для этого равные объемы хлорида аммония и гидроксида кальция перемешайте в ступке и поместите в сухую пробирку. Заполните смесью 1/3 пробирки. Осторожно нагрейте смесь.
4) Назовите четыре физических свойства аммиака, которые вы обнаружили в этом опыте.
Опыт 2. Растворение аммиака в воде.
1) Пробирку с аммиаком закройте пробкой. Не переворачивая пробирку с аммиаком, опустите её в кристаллизатор с водой. Под водой откройте пробку. После заполнения пробирки водой закройте под водой её отверстие пробкой и выньте пробирку из воды. Опишите наблюдения и объясните их. Обобщите, какими физическими свойствами обладает аммиак.
2) К полученному раствору аммиака прилейте каплю раствора фенолфталеина. Объясните наблюдения. Сделайте вывод, к какому классу соединений относится продукт взаимодействия аммиака с водой. Запишите уравнение реакции.
Опыт 3. Взаимодействие раствора аммиака с кислотами.
1) Проведите реакцию гидроксида аммония с раствором соляной кислоты: в пробирку с раствором аммиака и раствором фенолфталеина прилейте по каплям раствор соляной кислоты до исчезновения малиновой окраски. Объясните наблюдения, запишите ионные уравнения реакций (полное и сокращенное). Сформулируйте вывод о свойствах водного раствора аммиака.
- Предыдущая
Музыкальный образ. Эпические образыСледующая -
Способы сжатия текста. Теория и практика Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов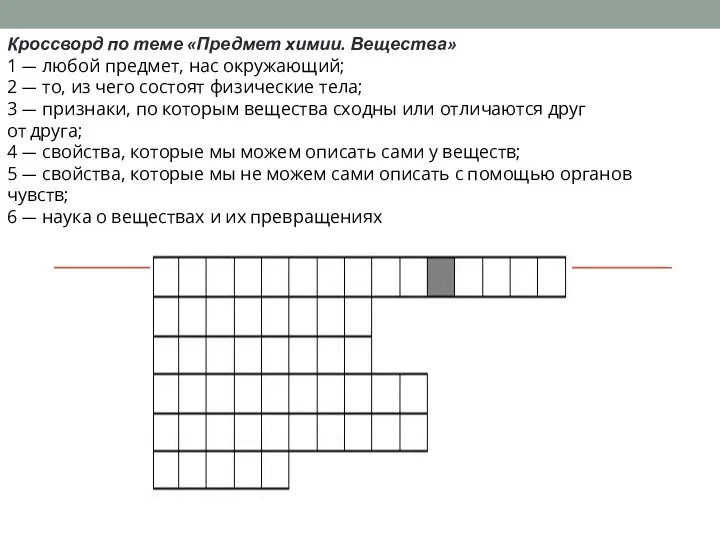 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19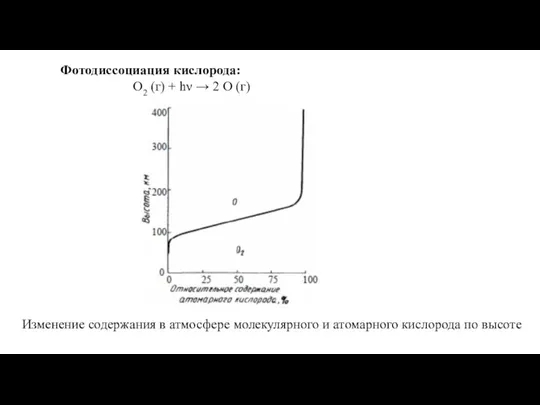 Фотодиссоциация кислорода
Фотодиссоциация кислорода