Содержание
- 2. Цели: Обобщить и систематизировать знания о щелочноземельных металлах Уметь характеризовать элементы по положению в периодической таблице
- 3. Положение в периодической таблице. Строение атома В периодической системе находятся в главной подгруппе II группы. Являются
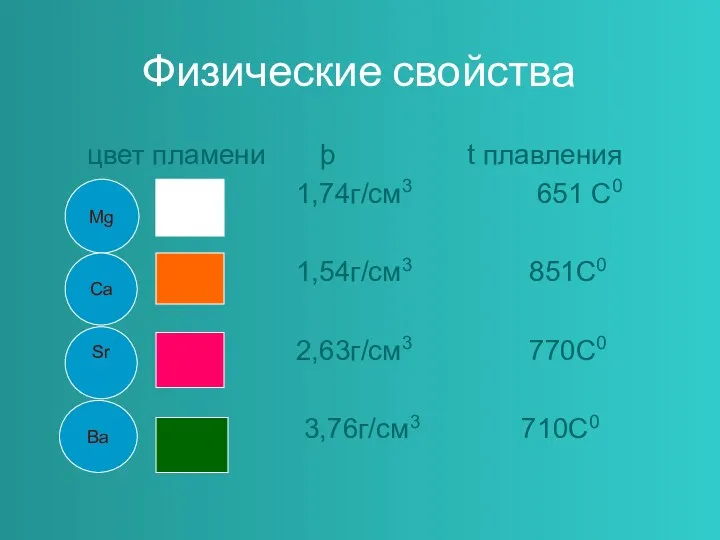
- 4. Физические свойства цвет пламени þ t плавления 1,74г/см3 651 С0 1,54г/см3 851С0 2,63г/см3 770С0 3,76г/см3 710С0
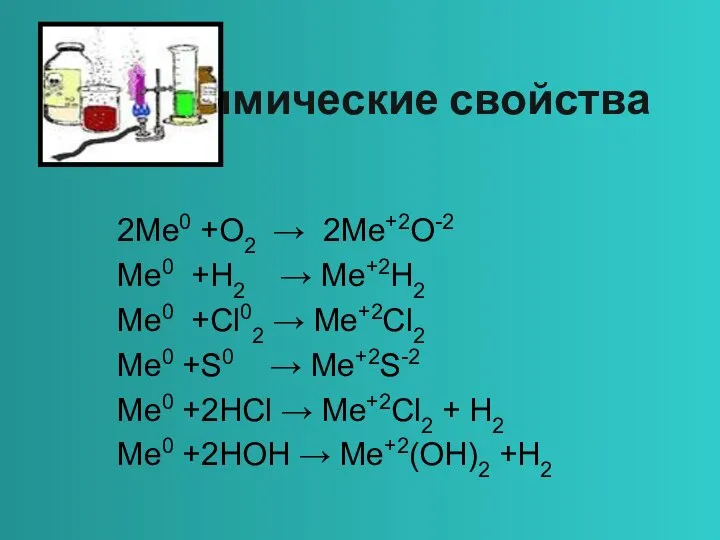
- 5. Химические свойства 2Me0 +O2 → 2Me+2O-2 Me0 +H2 → Me+2H2 Me0 +Cl02 → Me+2Cl2 Me0 +S0
- 6. Соединения щелочноземельных металлов Оксиды щелочноземельных металлов легко реагируют с оксидами неметаллов с образованием соответствующих солей.
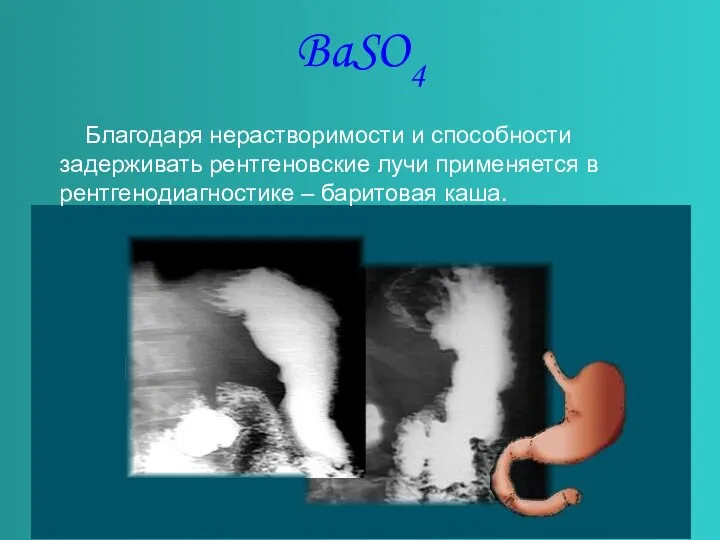
- 7. BaSO4 Благодаря нерастворимости и способности задерживать рентгеновские лучи применяется в рентгенодиагностике – баритовая каша.
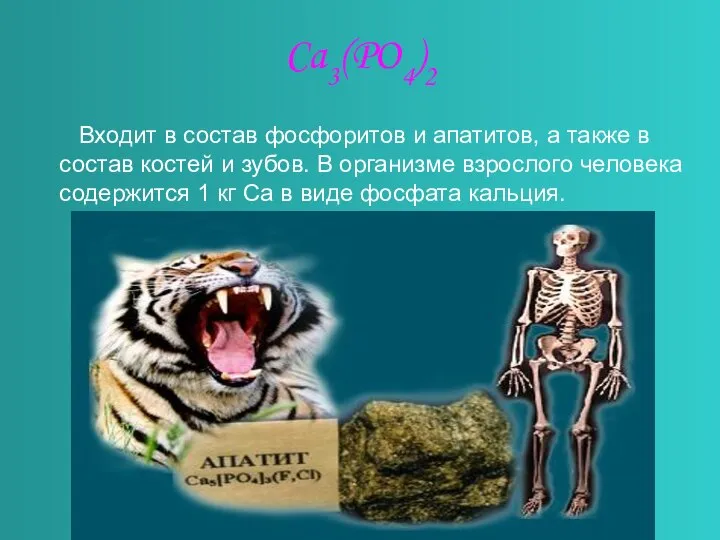
- 8. Ca3(PO4)2 Входит в состав фосфоритов и апатитов, а также в состав костей и зубов. В организме
- 9. CaCO3 Карбонат кальция – одно из самых распространённых на Земле соединений. Его содержат горные породы –
- 10. CaSO4∙ 2H2O Встречается в природе в виде минерала гипса, представляющего собой кристаллогидрат. Используется в строительстве, в
- 11. MgCO3 Широко применяется в производстве стекла, цемента, кирпича, а также в металлургии для перевода пустой породы
- 12. Са(ОН)2 Гидроксид кальция или гашёная известь с песком и водой называется известковым раствором и широко используется
- 13. Проверка знаний 1. Сравните атомы элементов, поставив знаки или = вместо *: а) заряд ядра: Mg
- 14. 2) К группе щелочных металлов относятся: а) Li Na K Cu Rb Ag б) Li Na
- 16. Скачать презентацию









 Классификация органических соединений и реакций. Изомерия. Лекция 2
Классификация органических соединений и реакций. Изомерия. Лекция 2 Проектная работа Кристаллизация
Проектная работа Кристаллизация Присоединение аммиака и аминов
Присоединение аммиака и аминов Основы химической кинетики
Основы химической кинетики Мыльная история
Мыльная история Общая характеристика аргона
Общая характеристика аргона Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Красители vs пигменты
Красители vs пигменты Химическая связь. Лекция №3
Химическая связь. Лекция №3 Химические равновесия в растворах. Лекция 2. Часть 1
Химические равновесия в растворах. Лекция 2. Часть 1 Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Сложные реакции
Сложные реакции Основания. Растворимые (гидроксиды щелочных и щелочноземельных металлов). Нерастворимые
Основания. Растворимые (гидроксиды щелочных и щелочноземельных металлов). Нерастворимые Презентация на тему Арены (10 класс)
Презентация на тему Арены (10 класс)  Презентация на тему Химия и здоровье человека (10 класс)
Презентация на тему Химия и здоровье человека (10 класс)  Шаблон для презентации по химии
Шаблон для презентации по химии Презентация на тему Все о спиртах
Презентация на тему Все о спиртах  Альдегиды. Состав. Строение. Свойства. Применение
Альдегиды. Состав. Строение. Свойства. Применение Ортофосфорная кислота
Ортофосфорная кислота Степень окисления
Степень окисления Степень окисления. Бинарные соединения
Степень окисления. Бинарные соединения Валентность. Нахождение химической формулы вещества по валентности
Валентность. Нахождение химической формулы вещества по валентности Соли
Соли Vzácne plyny
Vzácne plyny Полезные ископаемые
Полезные ископаемые Терпеноиды. Эфирные масла
Терпеноиды. Эфирные масла Введение в медицинскую химию: от молекулы к лекарству
Введение в медицинскую химию: от молекулы к лекарству Күкірт қышқылын алудың контакт әдісі
Күкірт қышқылын алудың контакт әдісі