Содержание
- 2. Содержание
- 3. СПИРТЫ R (OH)n Спиртами называются производные УВ, в которых один или несколько атомов водорода замещены на
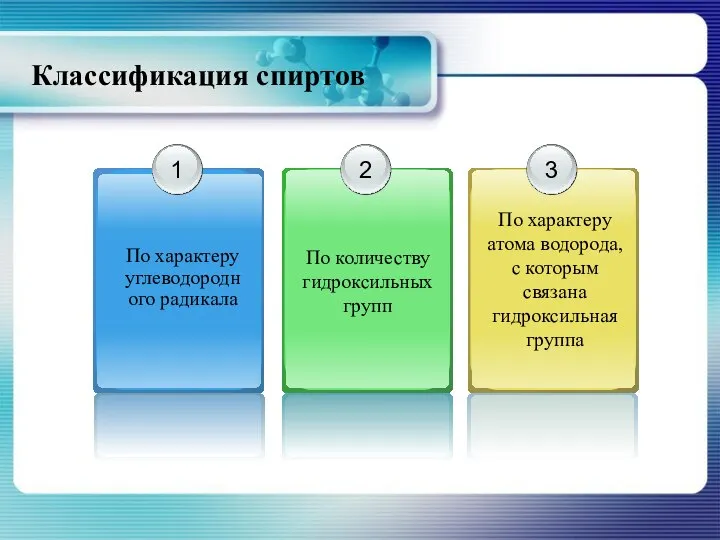
- 4. Классификация спиртов
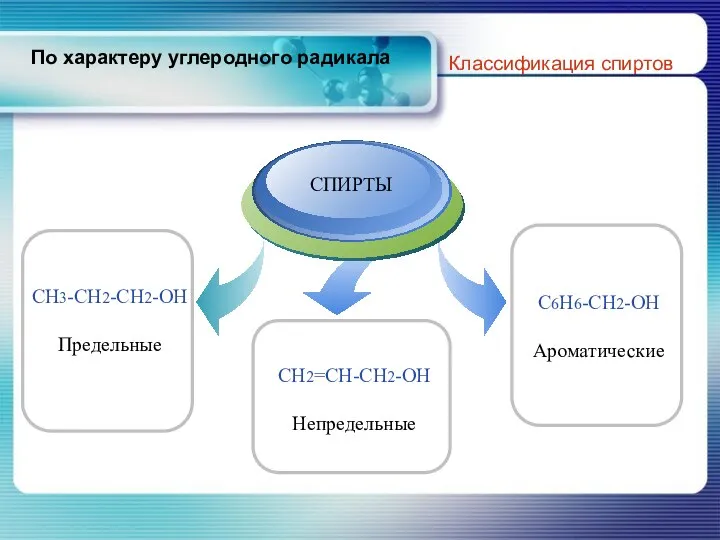
- 5. По характеру углеродного радикала Классификация спиртов
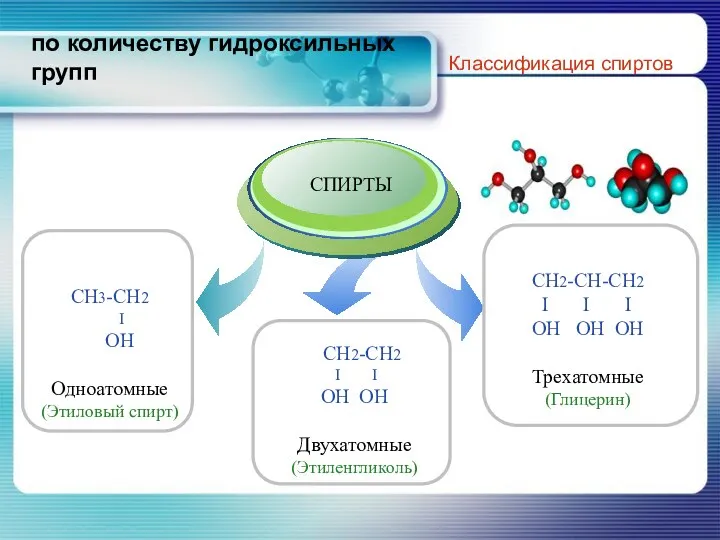
- 6. по количеству гидроксильных групп Классификация спиртов
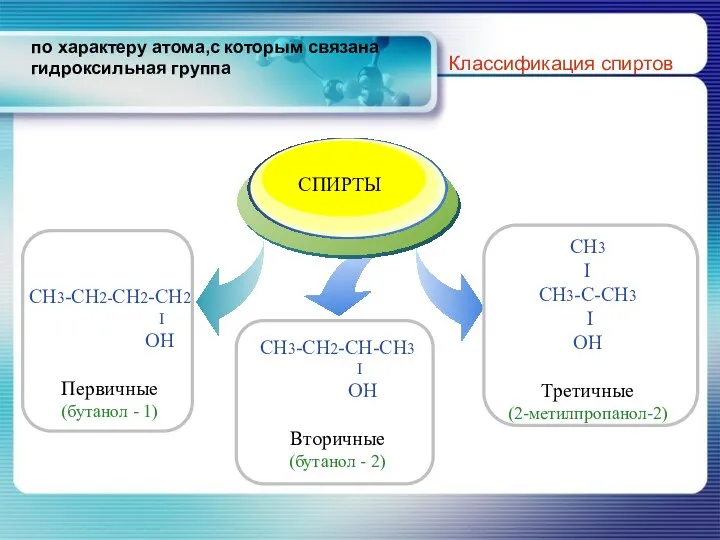
- 7. по характеру атома,с которым связана гидроксильная группа Классификация спиртов
- 8. Предельные одноатомные спирты Алканолы образуют гомологический ряд общей формулы CnH2n+1OH (n=1,2,3,…). Названия алканолов по систематичес-кой номенклатуре
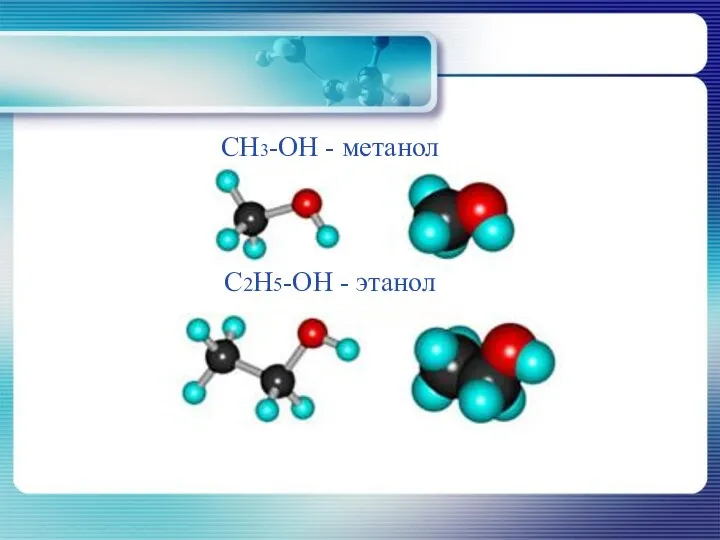
- 9. CH3-OH - метанол C2H5-OH - этанол
- 10. www.themegallery.com
- 11. Изомерия положения гидроксильной группы в углеродной цепи (с С3) CH3-CH2-CH2-OH пропанол-1 (пропиловый спирт) CH3-CH-CH3 l OH
- 12. CH3-CH2-CH2-CH2-OH бутанол-1 (бутиловый спирт) CH3-CH-CH2-OH l CH3 2-метилпропанол-1 (изобутиловый спирт) Первым из спиртов, для которого характерны
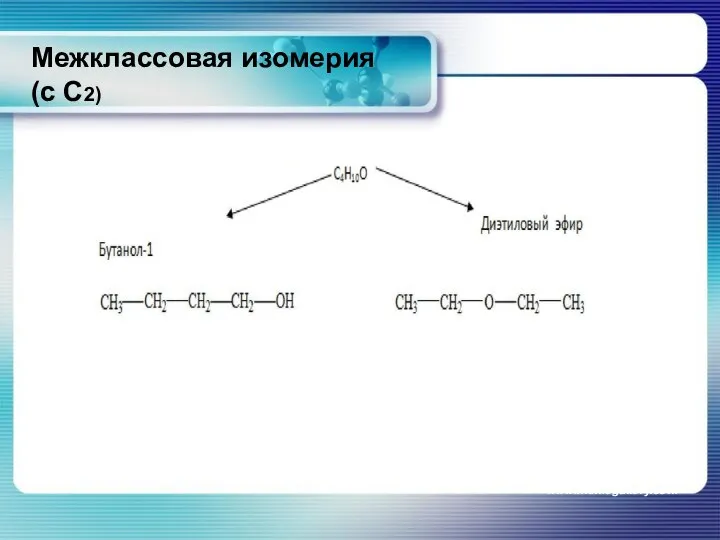
- 13. Межклассовая изомерия (с С2) www.themegallery.com
- 14. Физические свойства спиртов Алканолы являются бесцветными жидкостями или кристаллическими веществами с характерным запахом. Первые члены гомологического
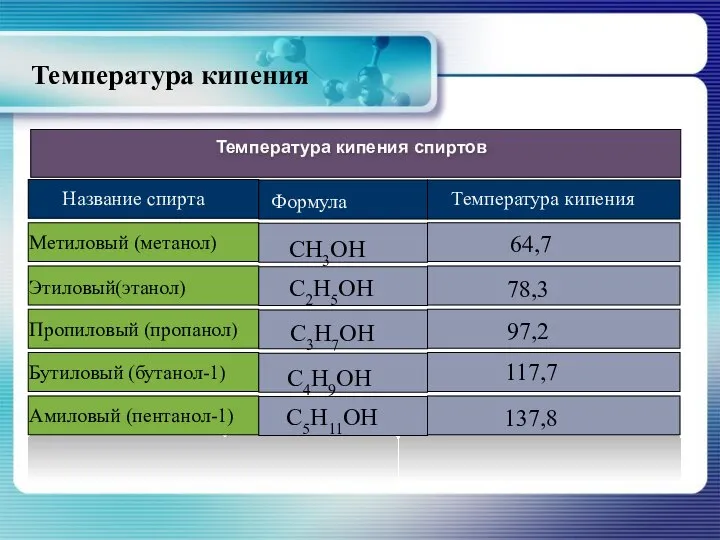
- 15. Температура кипения
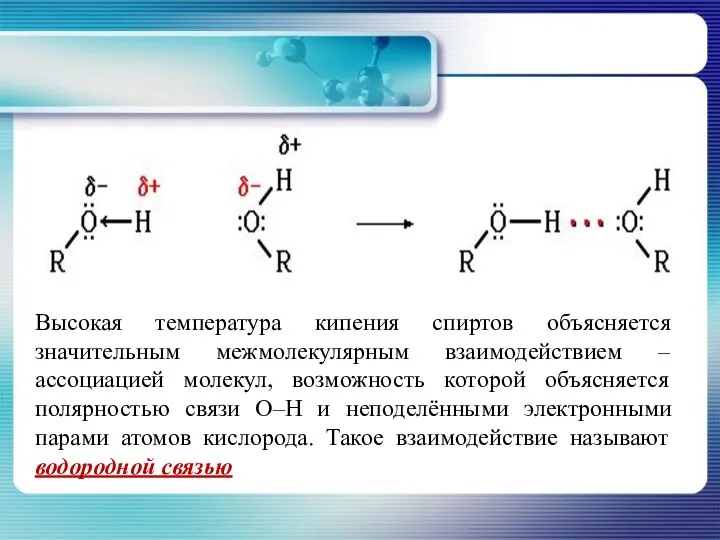
- 16. Высокая температура кипения спиртов объясняется значительным межмолекулярным взаимодействием – ассоциацией молекул, возможность которой объясняется полярностью связи
- 17. Строение молекулы этанола В молекуле этанола атомы углерода, водорода и кислорода связаны только одинарными - связями.
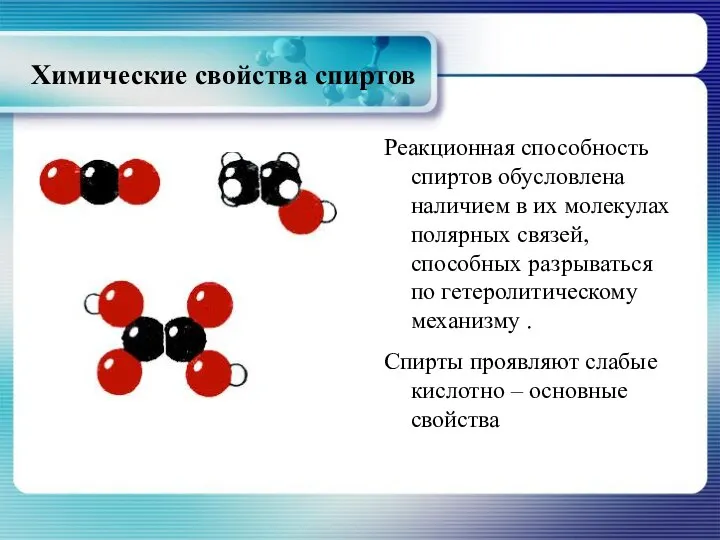
- 18. Химические свойства спиртов Реакционная способность спиртов обусловлена наличием в их молекулах полярных связей, способных разрываться по
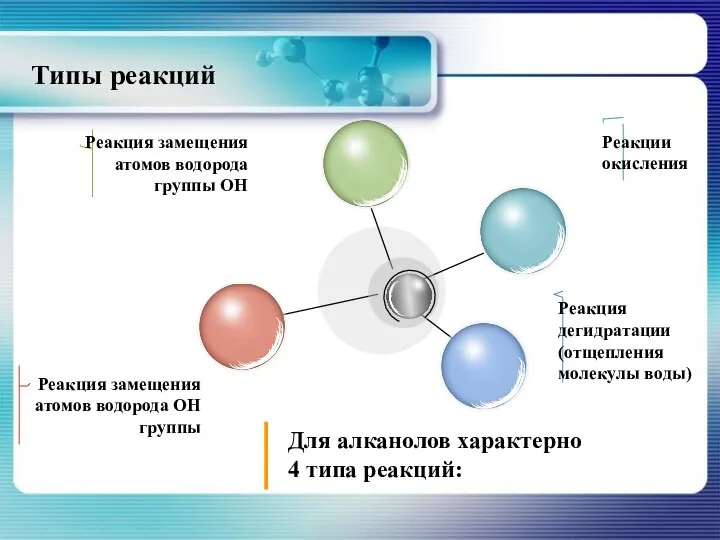
- 19. Типы реакций
- 20. Реакция замещения водорода -ОН группы 2С2Н5ОН + 2Na → 2C2H5ONa + H2 этилат Na Как слабые
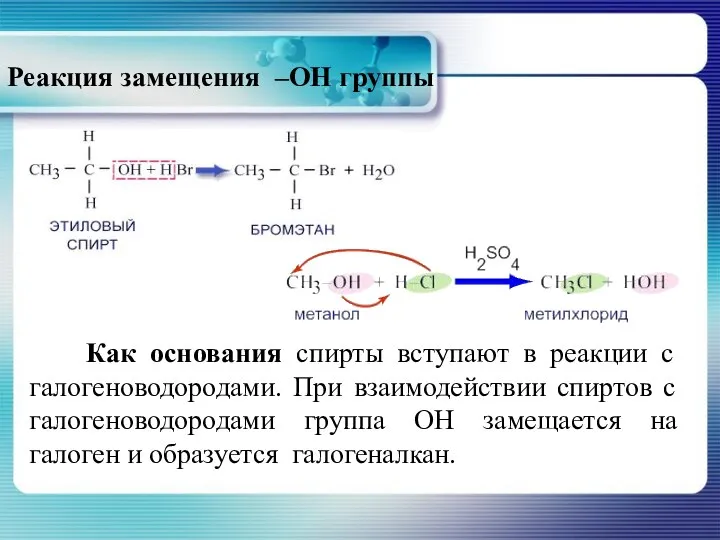
- 21. Реакция замещения –ОН группы Как основания спирты вступают в реакции с галогеноводородами. При взаимодействии спиртов с
- 22. Многоатомные спирты также, как и одноатомные спирты, реагируют с галогеноводородами. www.themegallery.com
- 23. Качественная реакция на многоатомные спирты Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи,
- 24. Реакция замещения –ОН группы Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на
- 25. Реакция дегидратации Для алканолов характерно два типа реакции дегидратации: - внутримолекулярная и - межмолекулярная При внутримолекулярной
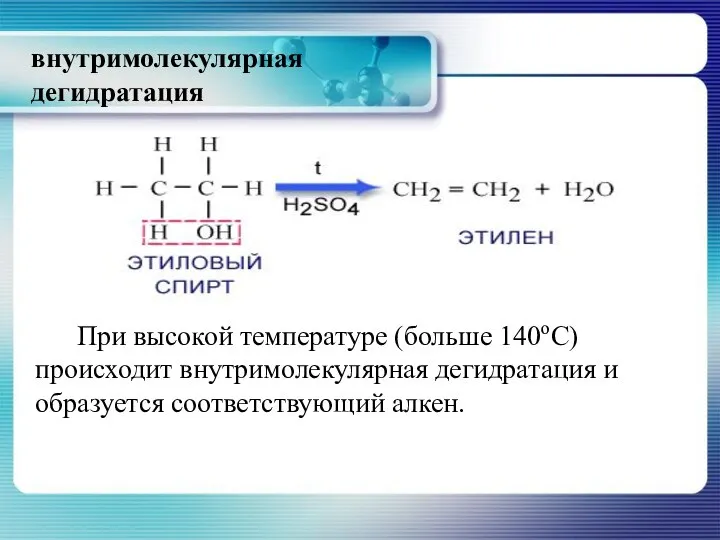
- 26. внутримолекулярная дегидратация При высокой температуре (больше 140оС) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
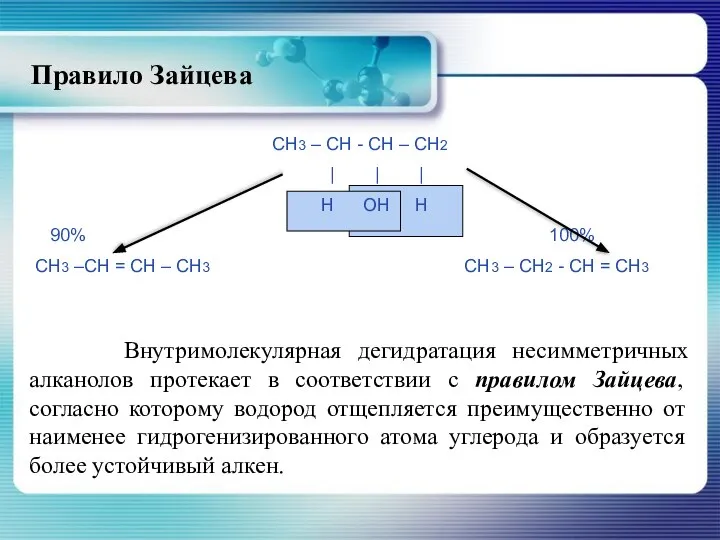
- 27. Правило Зайцева Внутримолекулярная дегидратация несимметричных алканолов протекает в соответствии с правилом Зайцева, согласно которому водород отщепляется
- 28. межмолекулярная дегидратация При низкой температуре (меньше 140оС) происходит межмолекулярная дегидратация. ОН-группа в одной молекуле спирта замещается
- 29. Дегидрирование спиртов При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола и
- 30. Этерификация (образование сложных эфиров) Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные
- 31. Реакции окисления Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого
- 33. ПОЛУЧЕНИЕ Метанол и этанол Метанол получают гидрированием оксида углерода (II) СО. В настоящее время разработан способ
- 34. Спиртовое брожение глюкозы . C6H12O6
- 35. Мировое производство метанола составляет около 10 миллионов тонн в год, этанола производится примерно на порядок больше.
- 37. Скачать презентацию





















 Термодинамика. Термодинамические потенциалы
Термодинамика. Термодинамические потенциалы Щелочноземельные металлы
Щелочноземельные металлы Смеси веществ
Смеси веществ История создания термометра: как придумали первый градусник?
История создания термометра: как придумали первый градусник? Стратегия обучения решению задач по химии
Стратегия обучения решению задач по химии Презентация на тему Уравнение Менделеева-Клапейрона
Презентация на тему Уравнение Менделеева-Клапейрона  Дисперсные системы. Гели
Дисперсные системы. Гели Щелочные металлы
Щелочные металлы Нефть и способы ее переработки. Октановое число - что это?
Нефть и способы ее переработки. Октановое число - что это? Электролитическая диссоциация
Электролитическая диссоциация Углеводы. Полисахариды. Важнейшие представители
Углеводы. Полисахариды. Важнейшие представители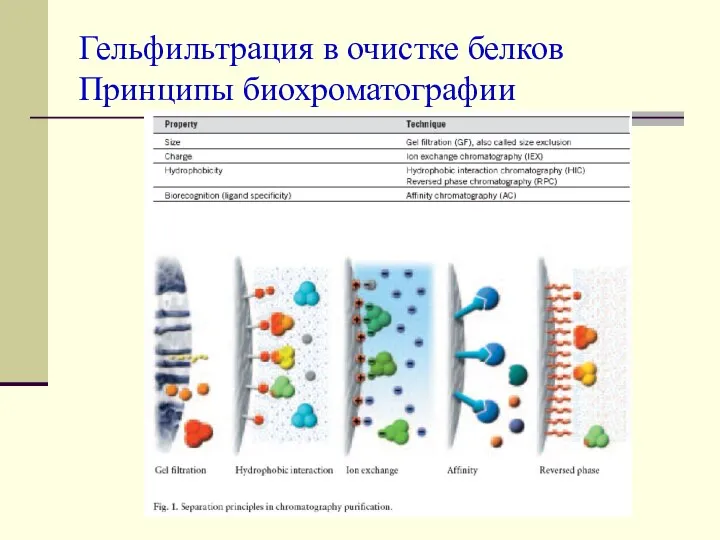 Гельфильтрация в очистке белков. Принципы биохроматографии
Гельфильтрация в очистке белков. Принципы биохроматографии Төртінші негізгі топша элементтері
Төртінші негізгі топша элементтері Серная кислота
Серная кислота Типичные реакции оснований
Типичные реакции оснований Строение электронных оболочек атомов. 8 класс
Строение электронных оболочек атомов. 8 класс Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Cиликат кальция
Cиликат кальция Кристаллические решетки
Кристаллические решетки Чистые вещества и смеси. Использование химического анализа
Чистые вещества и смеси. Использование химического анализа Бензол. Cвойства, реакции, применение
Бензол. Cвойства, реакции, применение 20140111_mineraly
20140111_mineraly Презентация на тему Химия в медицине
Презентация на тему Химия в медицине  Адсорбция и смачивание
Адсорбция и смачивание Природный и попутный газы, их состав и использование
Природный и попутный газы, их состав и использование Получение и применение кислорода. Круговорот кислорода в природе
Получение и применение кислорода. Круговорот кислорода в природе Простые эфиры и перекиси
Простые эфиры и перекиси Чистые вещества и смеси. Классификация веществ. Оксиды
Чистые вещества и смеси. Классификация веществ. Оксиды