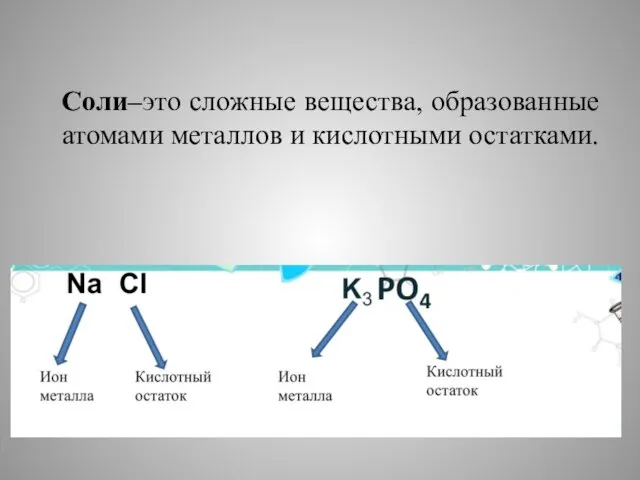
Слайд 2 Соли–это сложные вещества, образованные атомами металлов и кислотными остатками.
Слайд 3Диссоциация солей
Солями называются электролиты, при диссоциации которых образуются катионы металлов, а также катион аммония

(NH+4) и анионы кислотных остатков.
Например, диссоциация средних солей :
(NH4)2SO4 -> 2NH₄++ SO₄2-;
Na3PO 4 -> 3 Na + + PO₄3-
Слайд 4Номенклатура солей
Название Название Указание
Кислотного + металла (в Р.п.) + валентности
остатка (если она

переменная)
NaCl хлорид натрия
CaCO3 карбонат кальция
Са3(РО4)2 фосфат кальция
МgCI2 хлорид магния
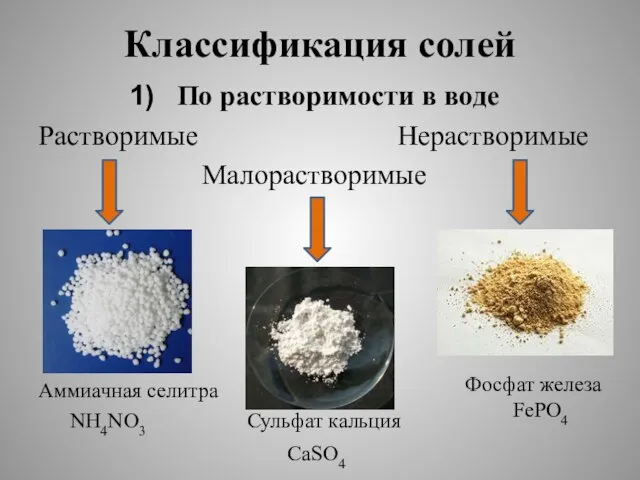
Слайд 5Классификация солей
По растворимости в воде
Растворимые Нерастворимые
Малорастворимые
Аммиачная селитра
NH4NO3 Сульфат кальция
Фосфат железа
Слайд 7Классификация солей
2) По наличию или отсутствию кислорода
Кислородсодержащие Бескислородные
Например: Например:
Na2SO4
(сульфат натрия) NaBr (бромид натрия)
KNO3 (нитрат калия) KY (иодид калия)
Ca(NO2)2 (нитрит кальция) CaCl2 (хлорид кальция)
Слайд 9Разновидности солей
Соли бывают:
Средние соли – это продукты полного замещения атомов водорода в

кислоте на металл.
Например: Na2CO3 (карбонат натрия)
CuSO4 (сульфат меди)
Слайд 10Разновидности солей
2) Кислые соли – это продукты неполного замещения атомов водорода

в кислоте на металл.
Например:
NaHCO3 (гидрокарбонат натрия)
Mg(HSO4)2 (гидросульфат магния)
Слайд 11Разновидности солей
3) Основные соли – это продукты неполного замещения гидроксогрупп в

основании на кислотный остаток.
Например:
(CuOH)2CO3 (гидроксокарбонат меди (II))
AlOHCl2 (гидроксохлорид алюминия)
Слайд 13Физические свойства:
Все соли твердые кристаллические вещества. Соли имеют различную окраску, и разную

растворимость в воде.
Слайд 14Химические свойства
Соль + кислота = другая соль + другая кислота
Например: H2SO4 +
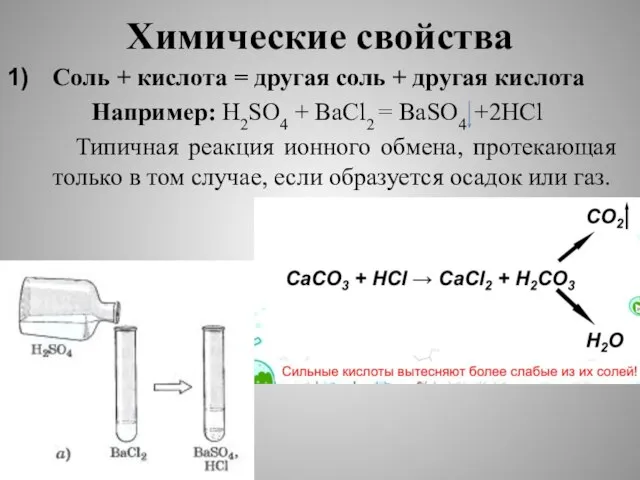
BaCl2 = BaSO4 +2HCl
Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок или газ.
Слайд 15Химические свойства
2) Соль + щелочь = другая соль + другое основание
Например: NaOH
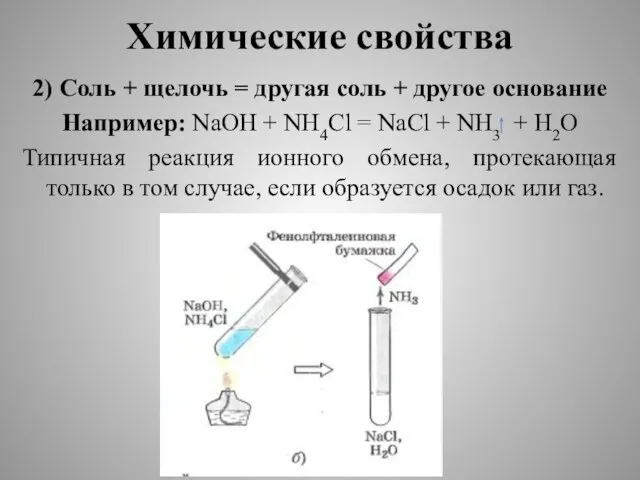
+ NH4Cl = NaCl + NH3 + H2O
Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок или газ.
Слайд 16Химические свойства
3) Соль1 + соль2 = соль3 + соль4
Например: Na2SO4

+ BaCl2 = BaSO4 +2NaCl
Типичная реакция ионного обмена, протекающая только в том случае, если образуется осадок.
Слайд 17Химические свойства
4) Соль + металл = другая соль + другой металл
Например: CuSO4(p-p)

+ Fe = FeSO4 (p-p) + Cu
Правила: а) Каждый металл вытесняет из растворов солей все другие металлы, расположенные правее его в ряду напряжений;
б) обе соли (и реагирующая, и образующаяся в результате реакции) должны быть растворимыми;
в) металлы не должны взаимодействовать с водой, поэтому металлы главных подгрупп I и II группы ПС Д.И.Менделеева не вытесняют другие металлы из растворов солей.


















 Азотная кислота
Азотная кислота Коллоидно-химическая теория схватывания и твердения вяжущих веществ
Коллоидно-химическая теория схватывания и твердения вяжущих веществ Ковалентная химическая связь
Ковалентная химическая связь Reactivi444
Reactivi444 Комлексті қосылыстардың кұрылысы мен қасиеттерін тусіндіретін теория, енгізген 1893 ж А. Вернер
Комлексті қосылыстардың кұрылысы мен қасиеттерін тусіндіретін теория, енгізген 1893 ж А. Вернер Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Арены. Бензол
Арены. Бензол Презентация на тему Амфотерные оксиды и гидроксиды
Презентация на тему Амфотерные оксиды и гидроксиды 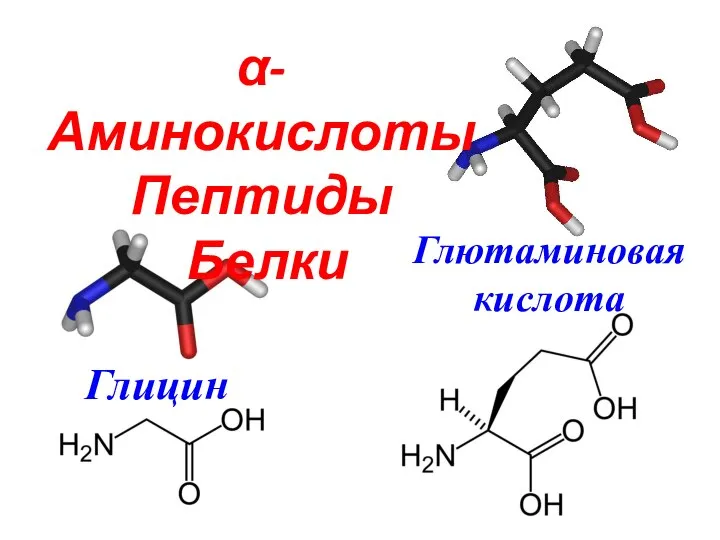 α-Аминокислоты
α-Аминокислоты Классификация и номенклатура аминов. 11 класс
Классификация и номенклатура аминов. 11 класс Получение аммиака и изучение его свойств. Практическая работа № 2
Получение аммиака и изучение его свойств. Практическая работа № 2 Викторина: А не химик ли ты?
Викторина: А не химик ли ты? Электрическая диссоциация
Электрическая диссоциация Щелочные металлы
Щелочные металлы Презентация на тему Движение электрона в атоме
Презентация на тему Движение электрона в атоме  Реакции ионного обмена
Реакции ионного обмена Химические вещества
Химические вещества Химическая связь
Химическая связь Цезий
Цезий Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Презентация на тему Химические свойства металлов
Презентация на тему Химические свойства металлов  Презентация на тему Войди в природу другом
Презентация на тему Войди в природу другом 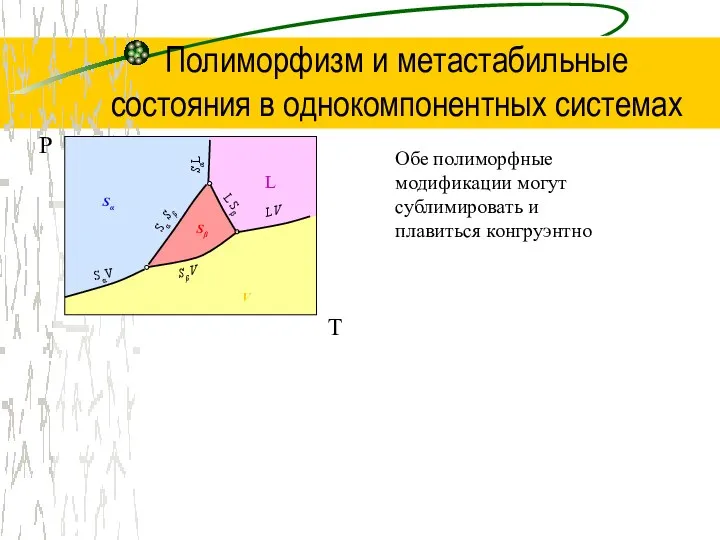 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Кислотність бджолиного обніжжя
Кислотність бджолиного обніжжя Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Кроссворд. Плотность
Кроссворд. Плотность Атом. Ядро и электронная оболочка. Изотопы. Строение электронных оболочек атома. Понятие об орбиталях
Атом. Ядро и электронная оболочка. Изотопы. Строение электронных оболочек атома. Понятие об орбиталях Svins. Iegūšana
Svins. Iegūšana