Содержание
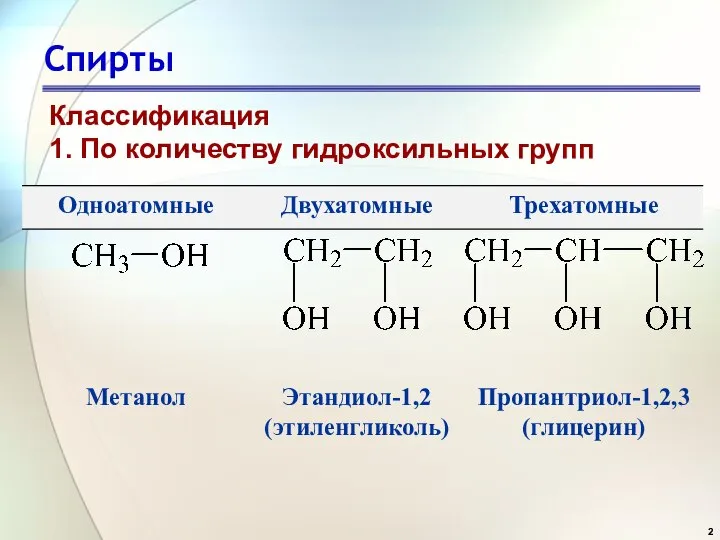
- 2. Спирты Классификация 1. По количеству гидроксильных групп
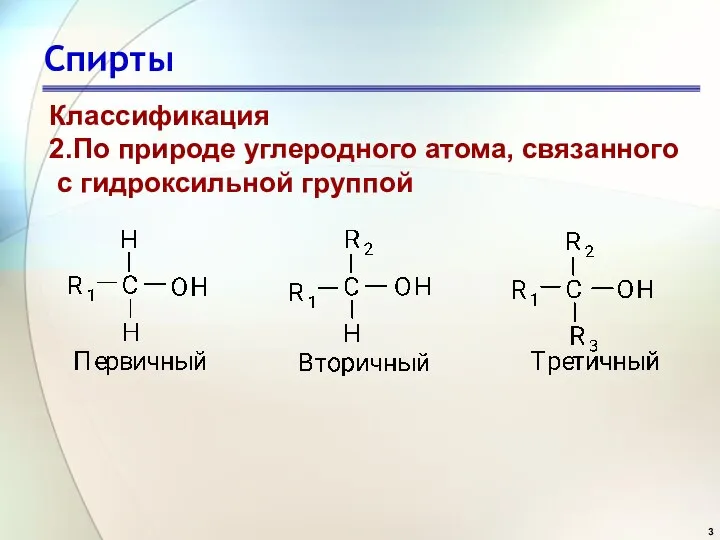
- 3. Спирты Классификация 2.По природе углеродного атома, связанного с гидроксильной группой
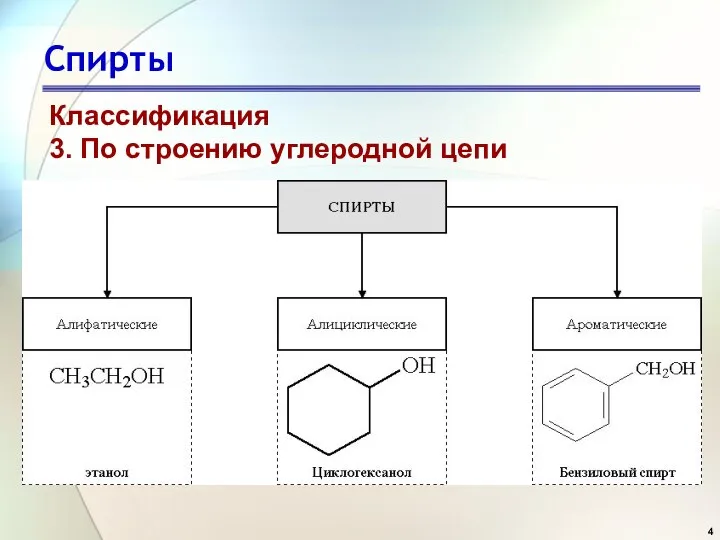
- 4. Спирты Классификация 3. По строению углеродной цепи
- 5. Спирты Изомерия 1. Измерия положения гидроксильной группы Пропанол-1 (н-пропиловый спирт) Пропанол-2 (изопропиловый спирт)
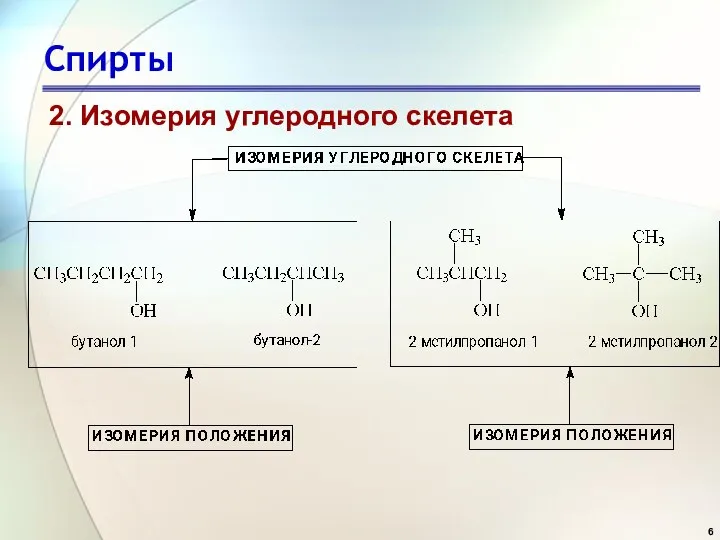
- 6. Спирты 2. Изомерия углеродного скелета
- 7. Спирты Номенклатура 1.Рациональная номенклатура 2.Радикально-функциональная номенклатура 3.Заместительная номенклатура
- 8. Спирты Номенклатура 1.По рациональной номенклатуре спирты называют как производные метанола (называется карбинол), у которого один или
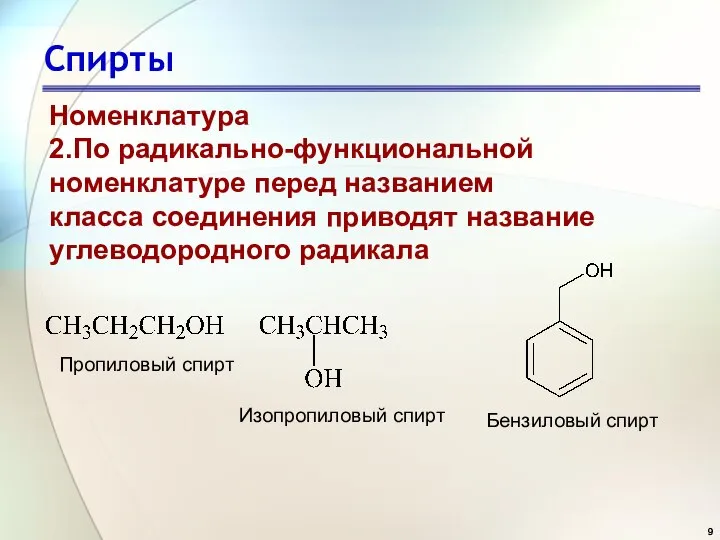
- 9. Спирты Номенклатура 2.По радикально-функциональной номенклатуре перед названием класса соединения приводят название углеводородного радикала Изопропиловый спирт Пропиловый
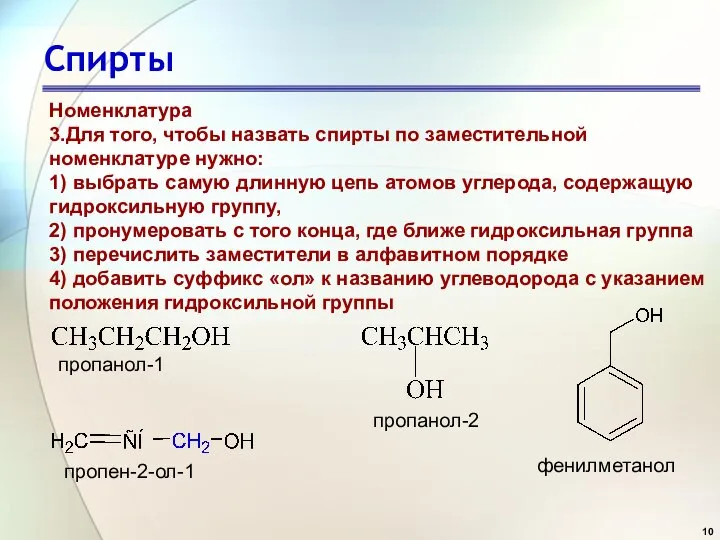
- 10. Спирты Номенклатура 3.Для того, чтобы назвать спирты по заместительной номенклатуре нужно: 1) выбрать самую длинную цепь
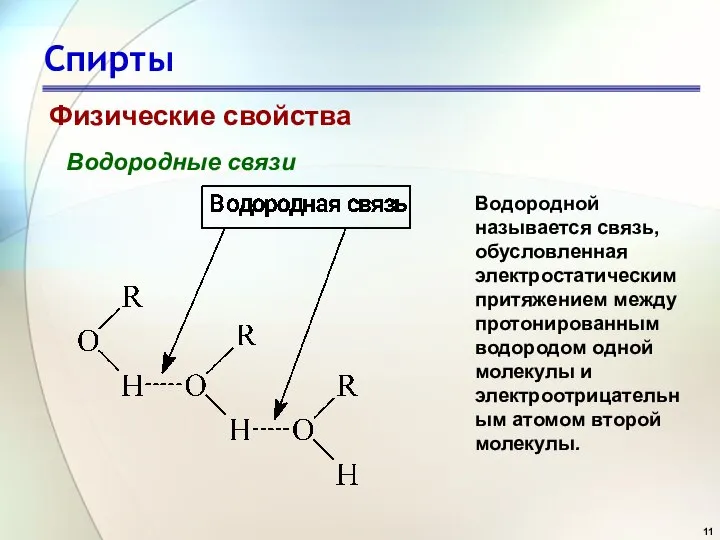
- 11. Спирты Физические свойства Водородные связи Водородной называется связь, обусловленная электростатическим притяжением между протонированным водородом одной молекулы
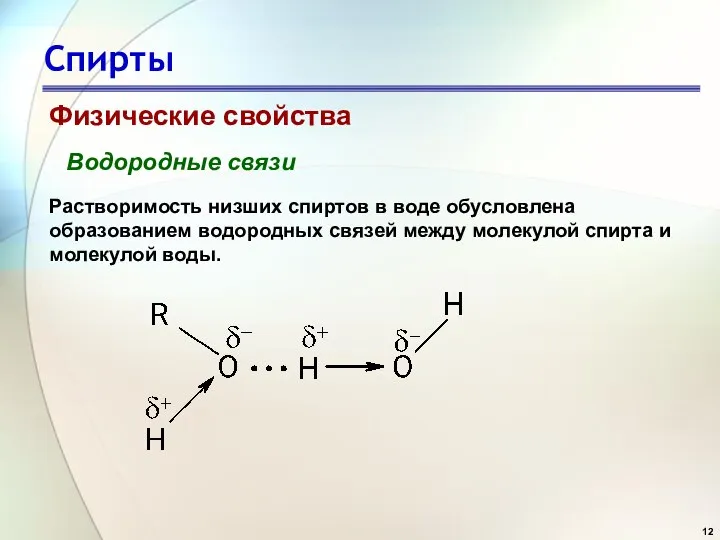
- 12. Спирты Физические свойства Водородные связи Растворимость низших спиртов в воде обусловлена образованием водородных связей между молекулой
- 13. Спирты Способы получения 1. Гидратация алкенов (промышленный метод) Присоединение воды к алкенам происходит в присутствии кислых
- 14. Спирты Способы получения 2. Брожение сахаров Дрожжи сбраживают некоторые виды сахаров. Это сложный каталитический многостадийный распад
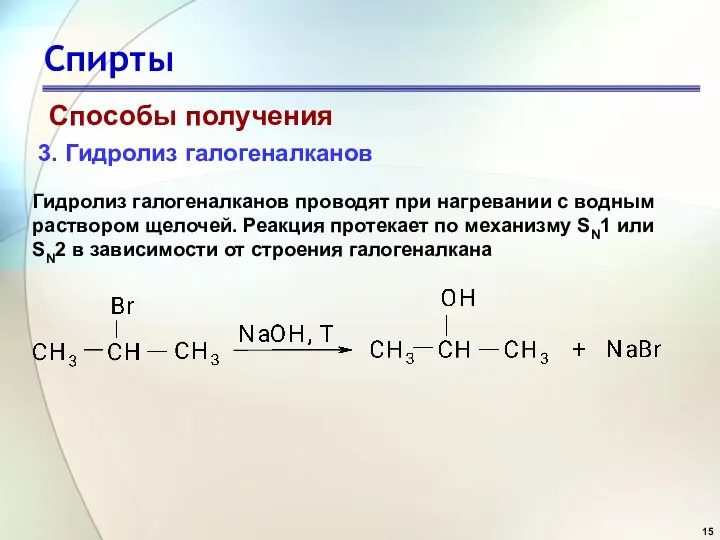
- 15. Спирты Способы получения 3. Гидролиз галогеналканов Гидролиз галогеналканов проводят при нагревании с водным раствором щелочей. Реакция
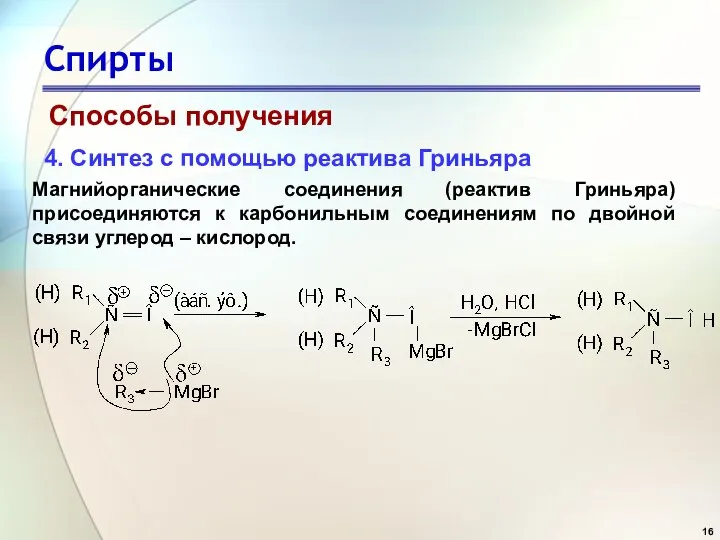
- 16. Спирты Способы получения 4. Синтез с помощью реактива Гриньяра Магнийорганические соединения (реактив Гриньяра) присоединяются к карбонильным
- 17. Спирты Способы получения 4. Синтез с помощью реактива Гриньяра Для синтеза первичных спиртов используют в качестве
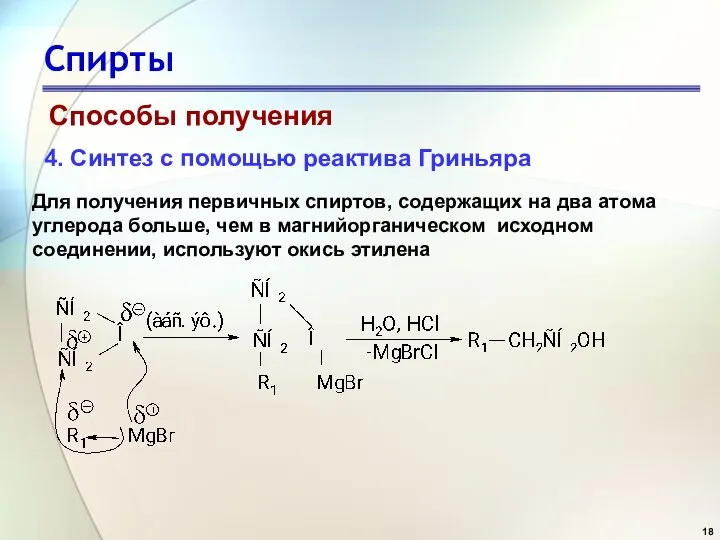
- 18. Спирты Способы получения 4. Синтез с помощью реактива Гриньяра Для получения первичных спиртов, содержащих на два
- 19. Спирты Способы получения 5. Гидроборирование-окисление алкенов Алкены взаимодействуют с дибораном В2Н6 с образованием алкилборана. Диборан -
- 20. Спирты Способы получения 6. Восстановление карбонильных соединений Альдегиды восстанавливаются в первичные спирты, кетоны – во вторичные
- 21. Спирты Способы получения 6. Восстановление карбонильных соединений Литийалюминийгидрид LiAlН4 – удобный, но дорогой восстанавливающий агент, используют
- 22. Спирты Способы получения 7. Восстановление сложных эфиров Первичные спирты также могут быть получены восстановлением сложного эфира,
- 23. Спирты Химические свойства 1. Кислотность спиртов В молекуле спирта содержится атом водорода, связанный с сильно электроотрицательным
- 24. Спирты Химические свойства 1. Кислотность спиртов
- 25. Спирты Химические свойства 1. Кислотность спиртов Алкоксиды (алкоголяты) нельзя получить реакцией спирта с гидроксидами металлов, их
- 26. Спирты Кислотность спиртов Кислотность спиртов в водных растворах pKa=-lgKa
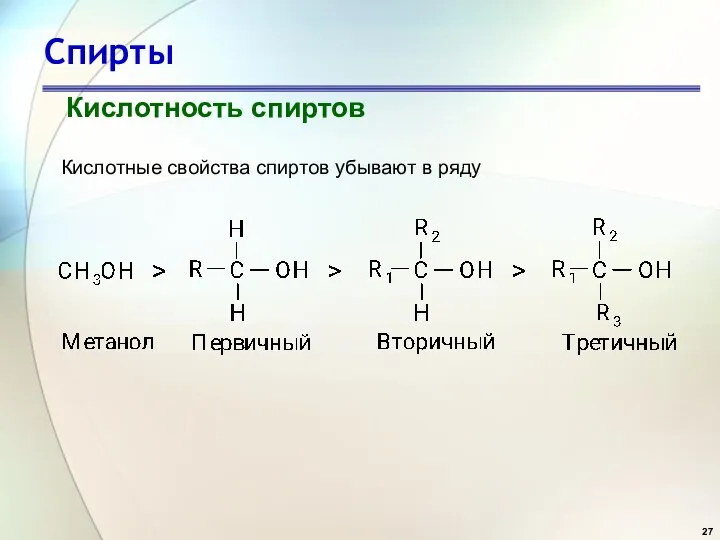
- 27. Спирты Кислотность спиртов Кислотные свойства спиртов убывают в ряду
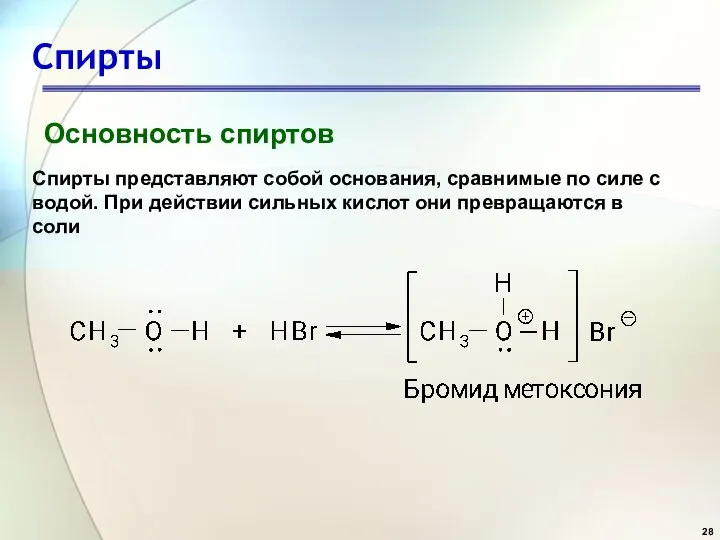
- 28. Спирты Основность спиртов Спирты представляют собой основания, сравнимые по силе с водой. При действии сильных кислот
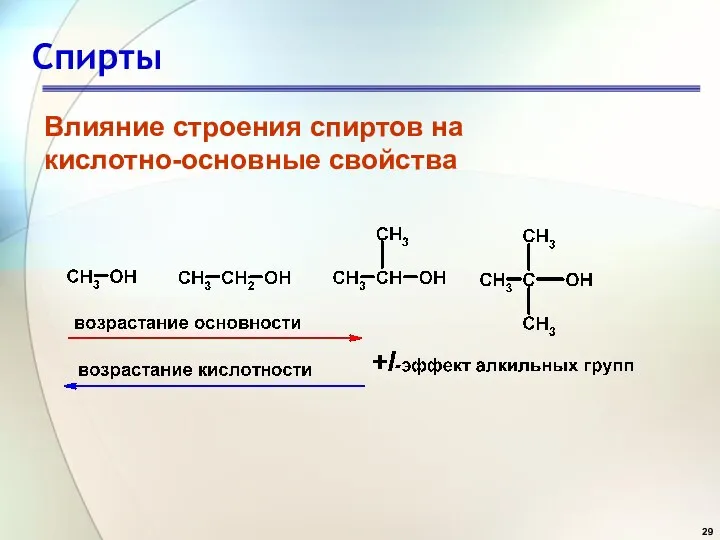
- 29. Спирты Влияние строения спиртов на кислотно-основные свойства
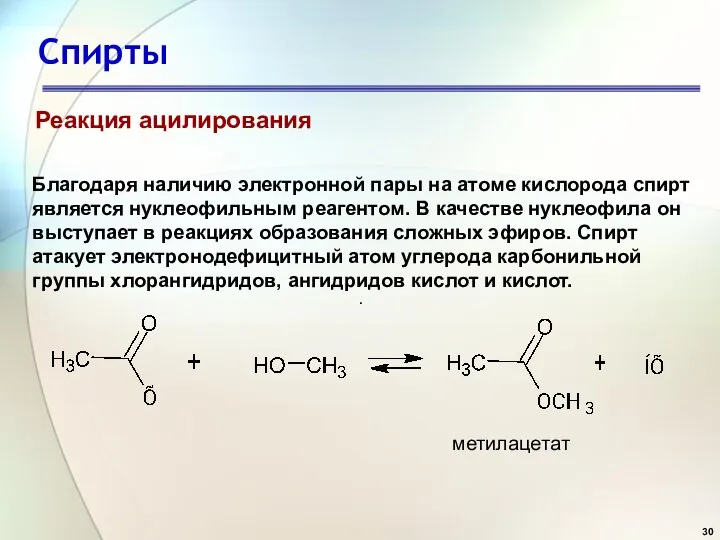
- 30. Спирты . Реакция ацилирования Благодаря наличию электронной пары на атоме кислорода спирт является нуклеофильным реагентом. В
- 31. Спирты . Реакция ацилирования С карбоновыми кислотами спирты реагируют в присутствии кислотных катализаторов, которые увеличивают поляризацию,
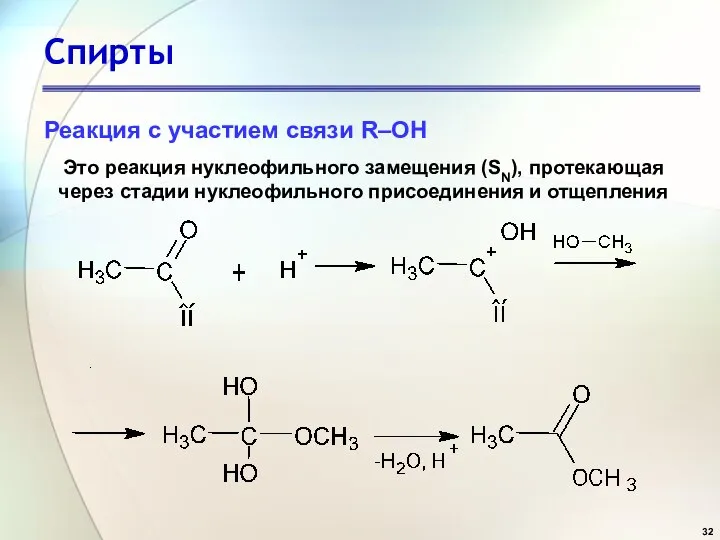
- 32. Спирты Реакция с участием связи R–OH . Это реакция нуклеофильного замещения (SN), протекающая через стадии нуклеофильного
- 33. Спирты Реакции нуклеофильного замещения Реакции с галогеноводородами, образование алкилгалогенидов Спирты легко реагируют с галогеноводородами (HCl, HBr,
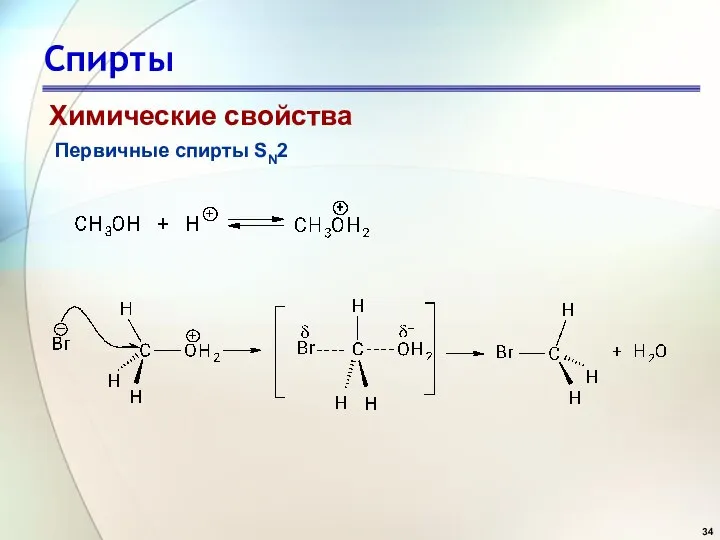
- 34. Спирты Химические свойства Первичные спирты SN2
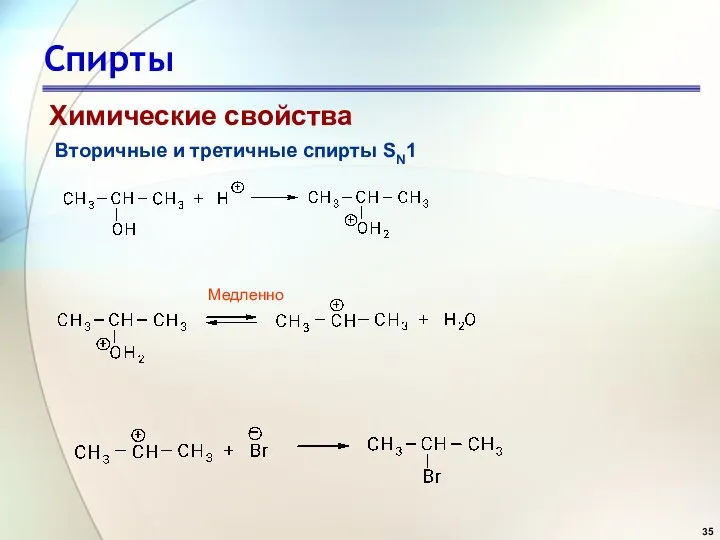
- 35. Спирты Химические свойства Вторичные и третичные спирты SN1 Медленно
- 36. Спирты Химические свойства Вторичные и третичные спирты SN1 Поскольку реакции замещения у вторичных и третичных спиртов
- 37. Спирты Химические свойства Реакционная способность спиртов по отношению к галогенводородам изменяется следующим образом: Бензиловый, аллиловый >
- 38. Спирты Реакции нуклеофильного замещения Реакция с галогенидами фосфора PCl5, PCl3, PBr3, PI3, тионилхлоридом SOCl2. Для получения
- 39. Спирты Реакции нуклеофильного замещения Межмолекулярная дегидратация спиртов. Получение простых эфиров Межмолекулярная дегидратация спиртов в присутствии каталитических
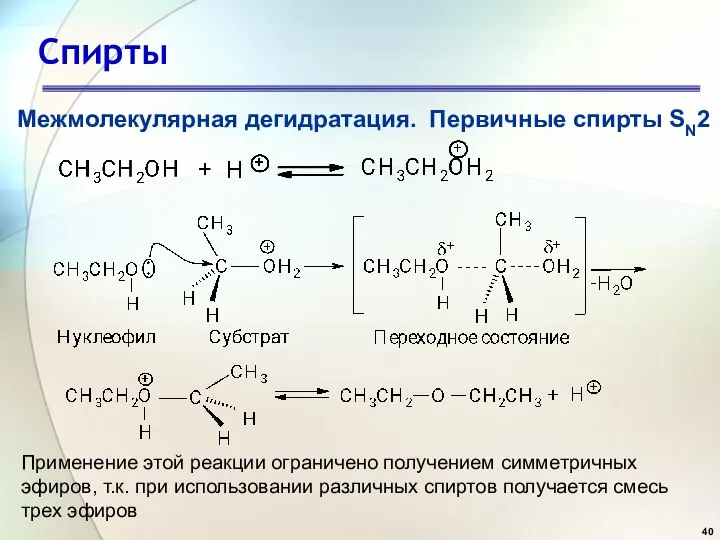
- 40. Спирты Межмолекулярная дегидратация. Первичные спирты SN2 Применение этой реакции ограничено получением симметричных эфиров, т.к. при использовании
- 41. Спирты Получение простых эфиров. Синтез А.Вильямсона. Важным методом получения простых эфиров является реакция алкоголятов с алкилгалогенидами
- 42. Спирты Образование алкенов – внутримолекулярная дегидратация . Спирт превращается в алкен при температуре ~ 200 оС
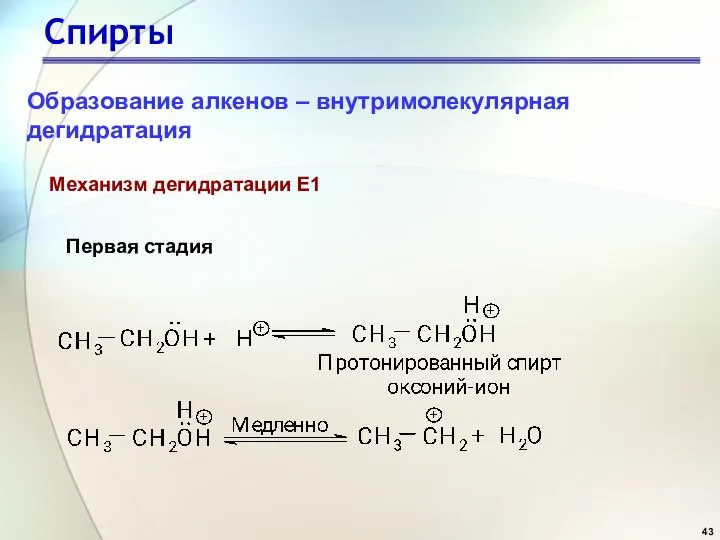
- 43. Спирты Механизм дегидратации Е1 Первая стадия Образование алкенов – внутримолекулярная дегидратация
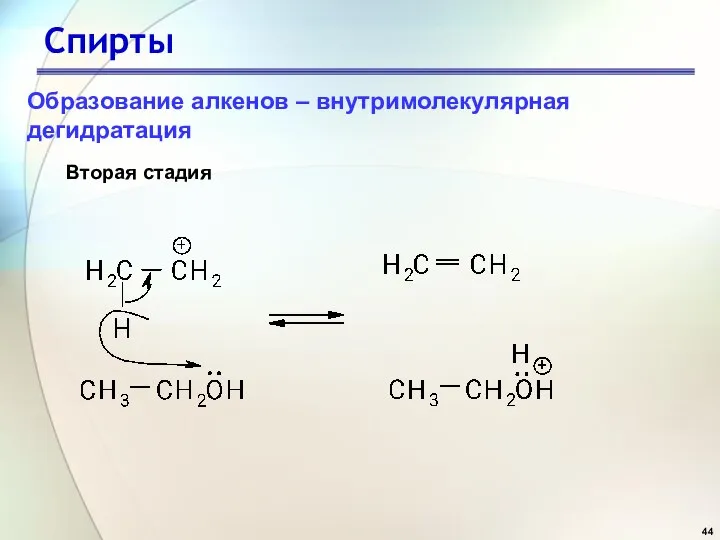
- 44. Спирты Вторая стадия Образование алкенов – внутримолекулярная дегидратация
- 45. Спирты В отличие от галогеналканов, которые подвергаются элиминированию в основном по Е2-механизму, спирты реагируют только по
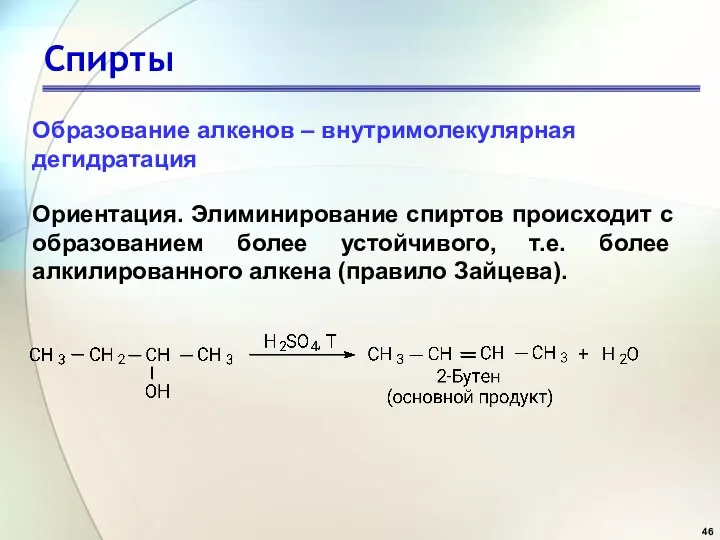
- 46. Спирты Ориентация. Элиминирование спиртов происходит с образованием более устойчивого, т.е. более алкилированного алкена (правило Зайцева). Образование
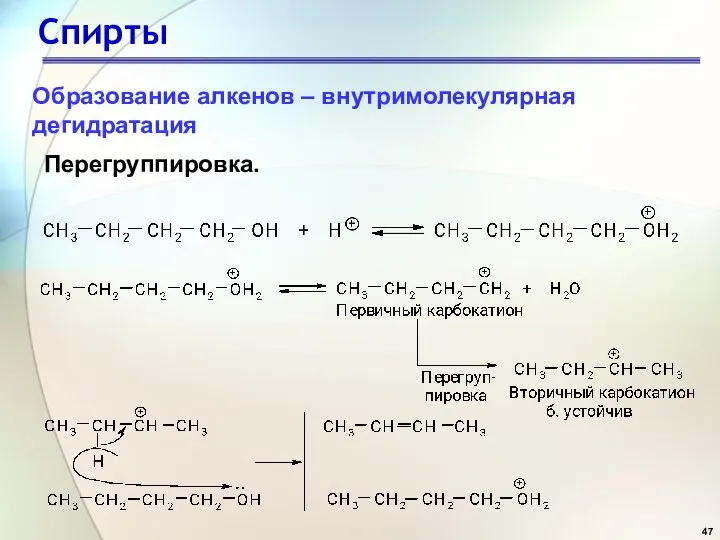
- 47. Спирты Перегруппировка. Образование алкенов – внутримолекулярная дегидратация
- 48. Спирты Реакции окисления Первичные спирты можно окислить до альдегидов действием К2Сr2О7, если одновременно с окислением вести
- 49. Спирты Реакции окисления Вторичные спирты окисляются до кетонов действием перманганата калия или хромовой кислотой. Дальнейшее окисление
- 50. Спирты Реакции окисления Третичные спирты в присутствии кислот превращаются в алкены, которые далее легко окисляются. В
- 51. Спирты Дегидрирование Превращение первичных спиртов в альдегиды, вторичных – в кетоны можно осуществлять, нагревая пары спирта
- 52. Спирты Замещение гидроксигруппы на водород Спирты устойчивы к действию химических восстановителей. Они не восстанавливаются и водородом
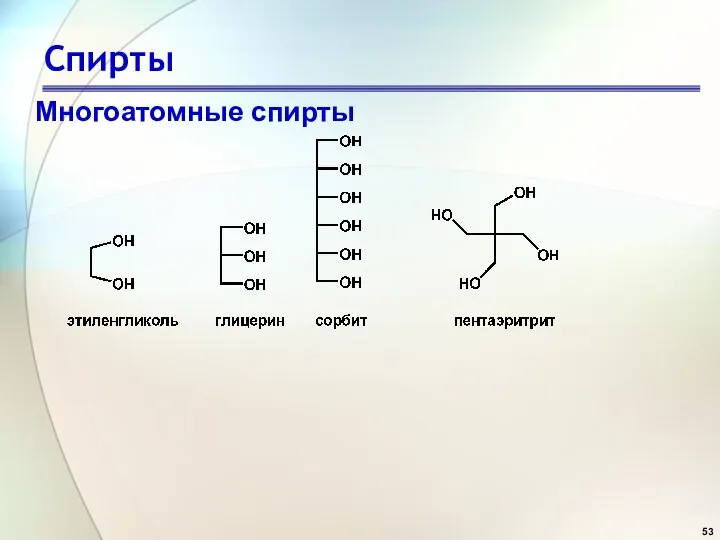
- 53. Спирты Многоатомные спирты
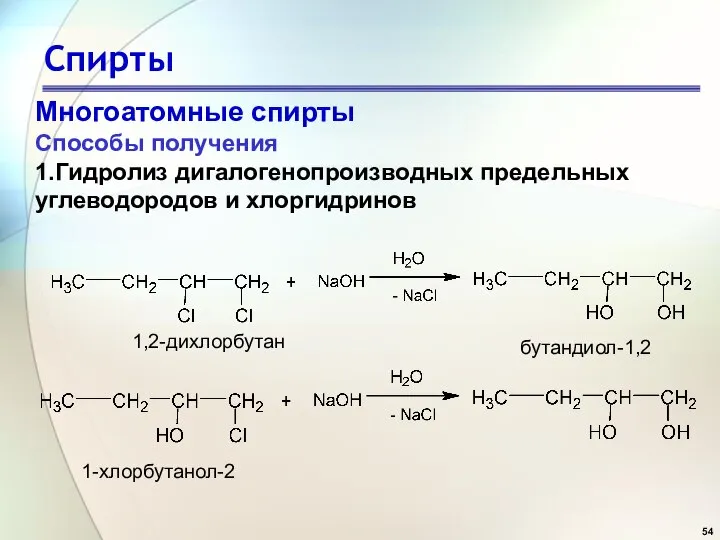
- 54. Спирты Многоатомные спирты Способы получения 1.Гидролиз дигалогенопроизводных предельных углеводородов и хлоргидринов 1,2-дихлорбутан бутандиол-1,2 1-хлорбутанол-2
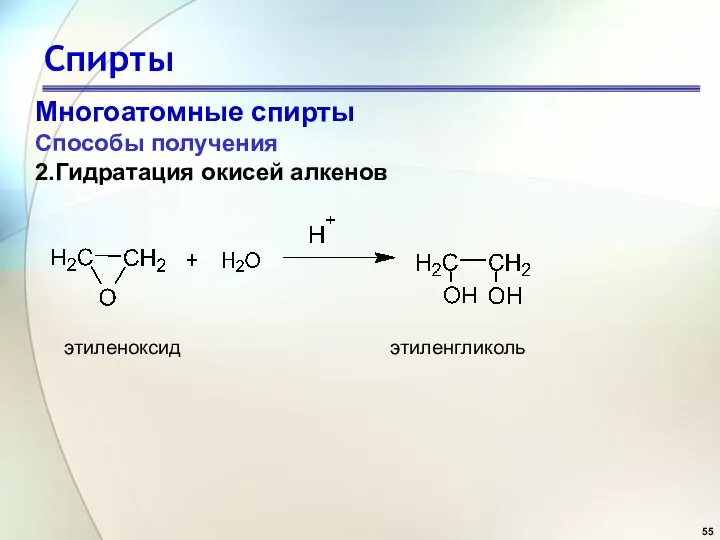
- 55. Спирты Многоатомные спирты Способы получения 2.Гидратация окисей алкенов этиленоксид этиленгликоль
- 56. Спирты Многоатомные спирты Способы получения 3.Окисление алкенов по Вагнеру Под действием холодного разбавленного раствора (5-10%) перманганата
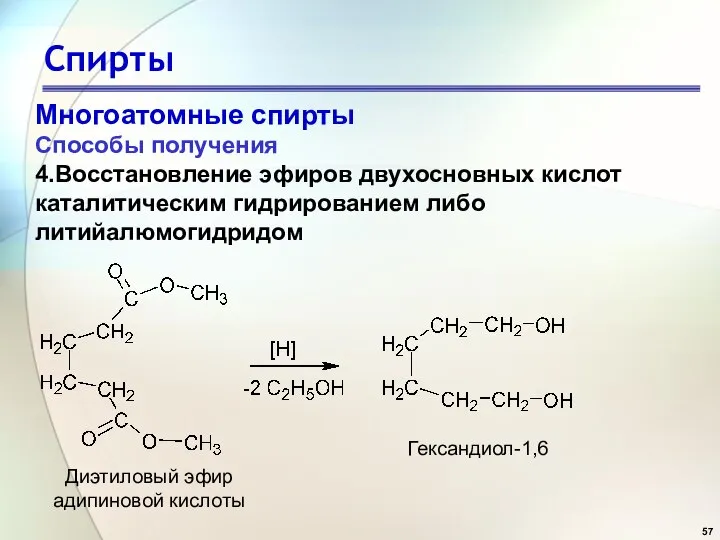
- 57. Спирты Многоатомные спирты Способы получения 4.Восстановление эфиров двухосновных кислот каталитическим гидрированием либо литийалюмогидридом Гександиол-1,6 Диэтиловый эфир
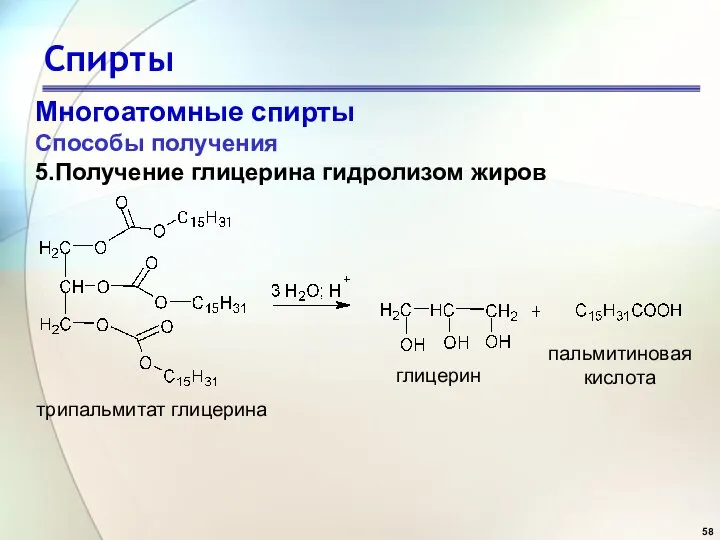
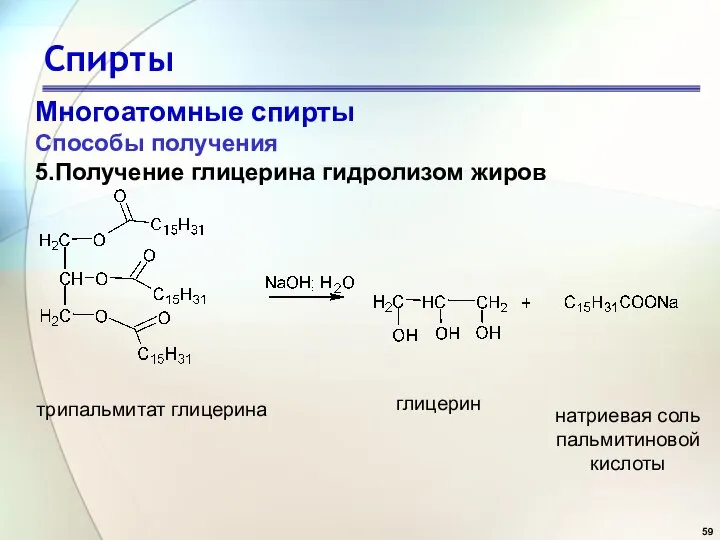
- 58. Спирты Многоатомные спирты Способы получения 5.Получение глицерина гидролизом жиров глицерин пальмитиновая кислота трипальмитат глицерина
- 59. Спирты Многоатомные спирты Способы получения 5.Получение глицерина гидролизом жиров глицерин натриевая соль пальмитиновой кислоты трипальмитат глицерина
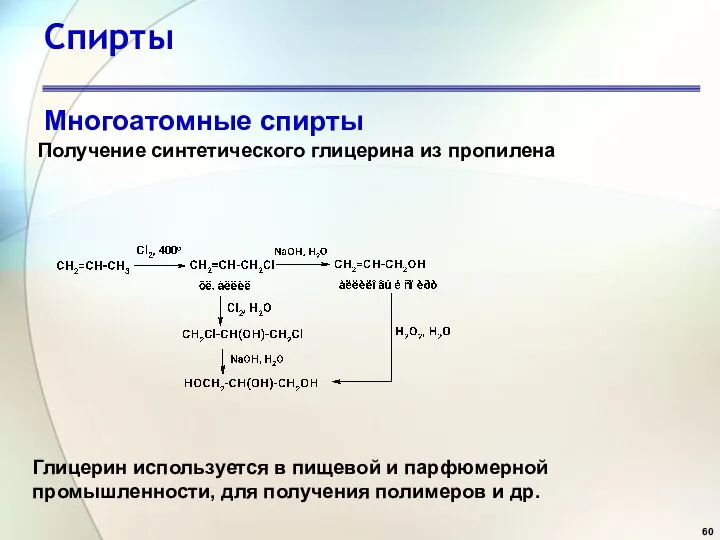
- 60. Спирты Многоатомные спирты Получение синтетического глицерина из пропилена Глицерин используется в пищевой и парфюмерной промышленности, для
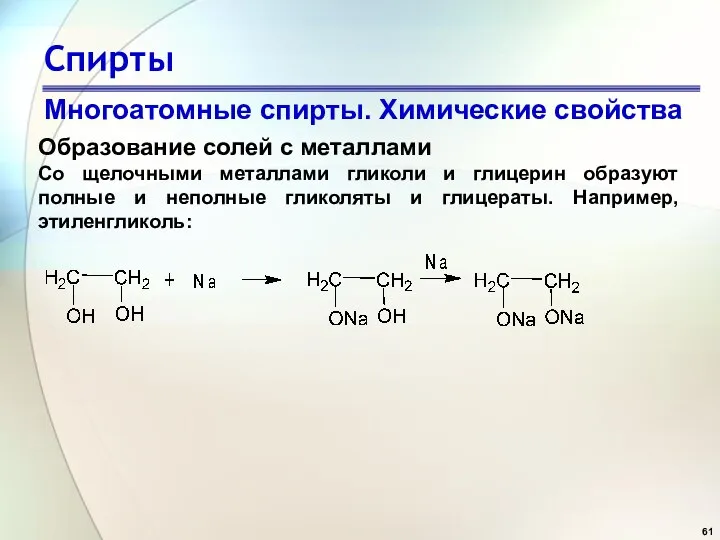
- 61. Спирты Многоатомные спирты. Химические свойства Образование солей с металлами Со щелочными металлами гликоли и глицерин образуют
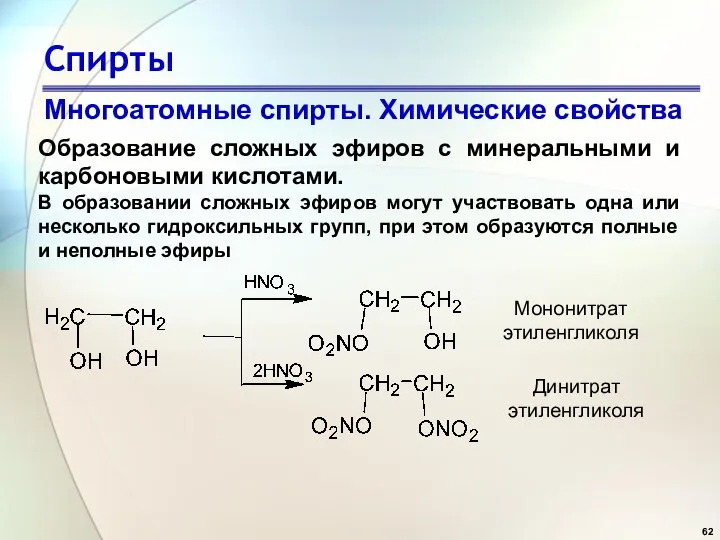
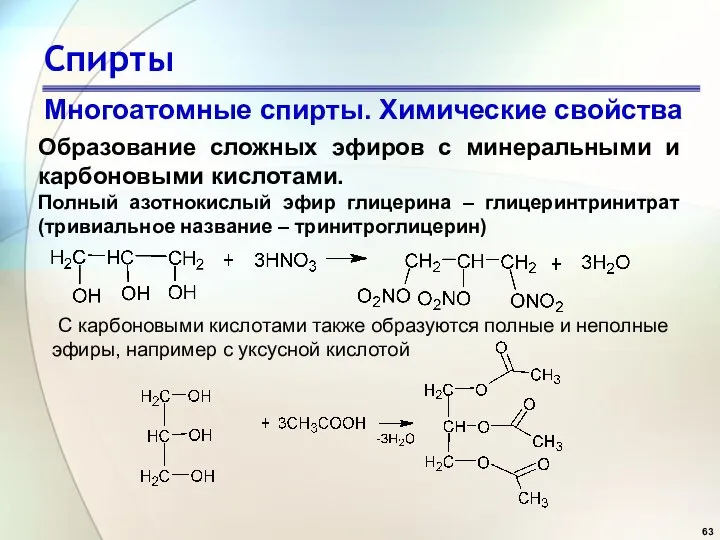
- 62. Спирты Многоатомные спирты. Химические свойства Образование сложных эфиров с минеральными и карбоновыми кислотами. В образовании сложных
- 63. Спирты Многоатомные спирты. Химические свойства Образование сложных эфиров с минеральными и карбоновыми кислотами. Полный азотнокислый эфир
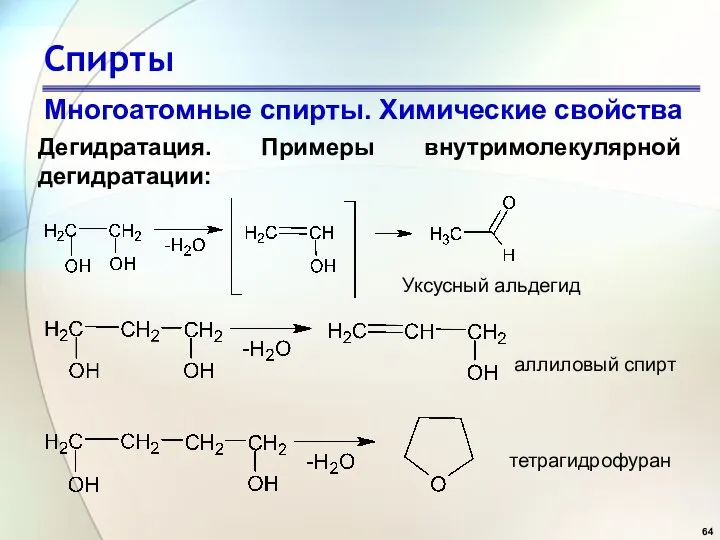
- 64. Спирты Многоатомные спирты. Химические свойства Дегидратация. Примеры внутримолекулярной дегидратации: Уксусный альдегид аллиловый спирт тетрагидрофуран
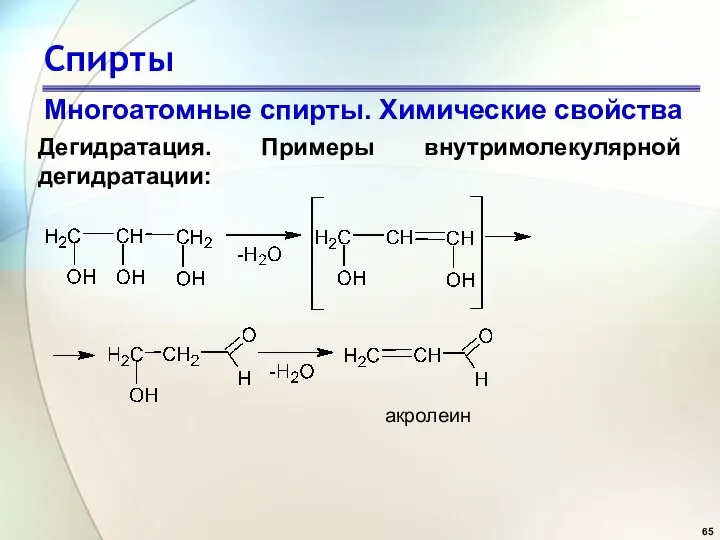
- 65. Спирты Многоатомные спирты. Химические свойства Дегидратация. Примеры внутримолекулярной дегидратации: акролеин
- 67. Скачать презентацию





























 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)