Содержание
- 5. Свойства соединений цинка, бериллия, алюминия, железа и хрома с точки зрения амфотерности Основные свойства при взаимодействии
- 6. Кислотные свойства при взаимодействии со щелочами Реакции при сплавлении Формулу гидроксида цинка записывают в кислотной форме
- 7. Реакции в растворе происходят с образованием комплексных солей Следует отметить, что при взаимодействии соединений алюминия со
- 8. Соединения бериллия (ВеО и Ве(ОН)2) взаимодействуют со щелочами аналогично соединениям цинка, соединения хрома(III) и железа(III) (Cr2O3,
- 9. При взаимодействии гидроксидов этих металлов со щелочами в растворе получаются комплексные соли с координационным числом 6
- 10. Металлические бериллий, цинк и алюминий взаимодействуют с растворами щелочей, вытесняя из них водород Железо и хром
- 11. Способы разрушения гидроксокомплексов 1. При действии избытка сильной кислоты получаются две средних соли и вода: Na[Al(OH)4]
- 12. Способы разрушения гидроксокомплексов 3. При действии слабой кислоты получаются кислая соль активного металла, амфотерный гидроксид и
- 13. Способы разрушения гидроксокомплексов При действии солей, образованных сильными кислотами и катионами Fe3+, Al3+ и Cr3+, происходит
- 14. Составьте уравнения четырех возможных реакций между растворами следующих соединений: гексагидроксохромат(III) калия, хлорид алюминия, сероводород, соляная кислота
- 16. Скачать презентацию













 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 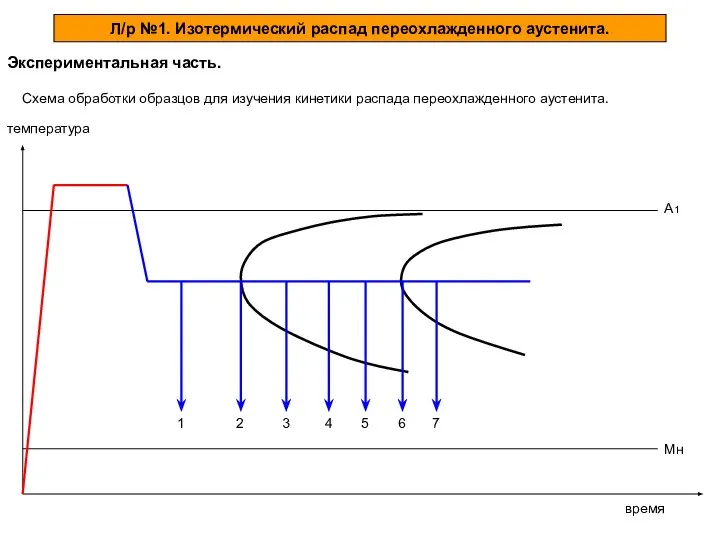 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций