Слайд 2План урока:
Строение молекулы серной кислоты
Физические свойства
Химические свойства
Получение
Применение

Слайд 3Строение молекулы серной кислоты
H2SO4 - молекулярная формула
Вопросы:
Простое или сложное вещество?
Какова валентность атомов:

H, S, O?
Какой тип химических связей в веществе?
Какой атом более электроотрицательный?
К какому атому смещена электронная плотность?
Слайд 4Физические свойства серной кислоты
H2SO4
Ответьте на вопросы:
Каково агрегатное состояние серной кислоты?
Хорошо ли она

смешивается с водой?
Серная кислота легче, или тяжелее воды?
Что произойдет, если прилить воду к кислоте?
5. Какие правила техники безопасности нужно помнить при работе с серной кислотой?
Слайд 5Химические свойства разбавленной кислоты
Дописать уравнения реакций:
Взаимодействие с металлами:
H2SO4+Mg->
Взаимодействие с основными и

амфотерными оксидами:
H2SO4+Na2O->
Взаимодействие с основаниями:
H2SO4+KOH->
Взаимодействие с солями:
H2SO4+BaCL2->
Слайд 6Химические свойства концентрированной кислоты:
1.Сильный окислитель. Обугливает органические вещества .
С12Н22О11------>12С+11Н2О
2. С

водой образует гидраты:
H2SO4+nH2O?H2SO4*nH2O
3.Регирует почти со всеми металлами:
Cu+2H2SO4?CuSO4+SO2+2H2O
Слайд 7Взаимодействие концентрированной
серной кислоты с металлами

Слайд 8Соли серной кислоты
Предложите названия следующим веществам .
Каково их применение?

Слайд 9Получение серной кислоты в промышленности
Осуществить цепочку превращения:
FeS2?SO2?SO3?H2SO4
По учебнику самостоятельно
изучить получение

серной
кислоты в промышленности.
Обсудите полученные знания
с соседом по парте.
Демонстрация эксперимента
получения серной кислоты в
лаборатории.








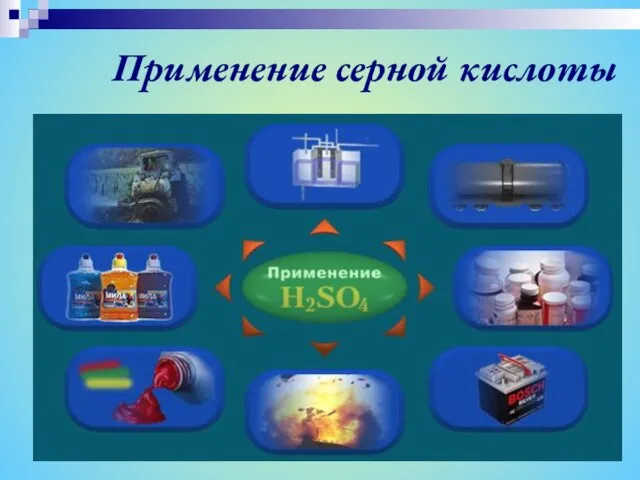
 Производство серной кислоты
Производство серной кислоты Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Вода. Растворы
Вода. Растворы Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Соли
Соли Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Металлы побочных подгрупп
Металлы побочных подгрупп Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Химический элемент кислород
Химический элемент кислород Химическая география чудес природы
Химическая география чудес природы Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1) Презентация по Химии "Схема получения моноизотопного кремния"
Презентация по Химии "Схема получения моноизотопного кремния"  Посвящение в химики
Посвящение в химики Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты)
Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты) Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Общая характеристика оксидов
Общая характеристика оксидов Серная кислота
Серная кислота Основные понятия химии
Основные понятия химии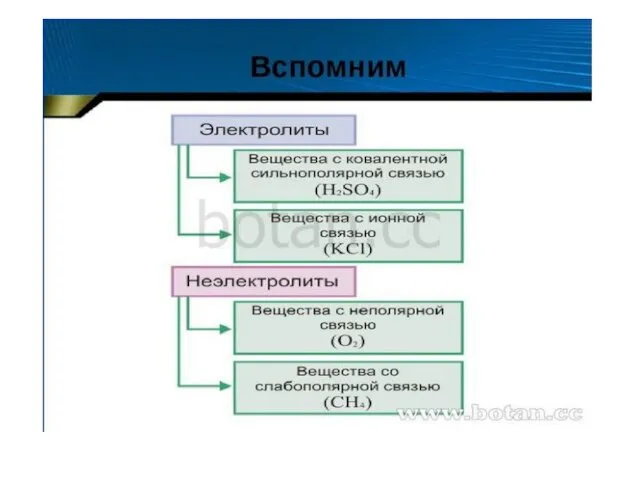 Диссоциация веществ
Диссоциация веществ Химическая связь и ее типы
Химическая связь и ее типы Соли. Химические свойства
Соли. Химические свойства Соль. Добыча соли
Соль. Добыча соли Металлы. Атомы металлов
Металлы. Атомы металлов Природные источники углеводорода
Природные источники углеводорода Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас