Содержание
- 2. Гидролизующиеся соли ГИДРОЛИЗ – реакция взаимодействия солей с водой
- 3. Соль, которая подвергается гидролизу и по аниону и по катиону: (CH3COO) NH4 Соль, образованная слабой кислотой
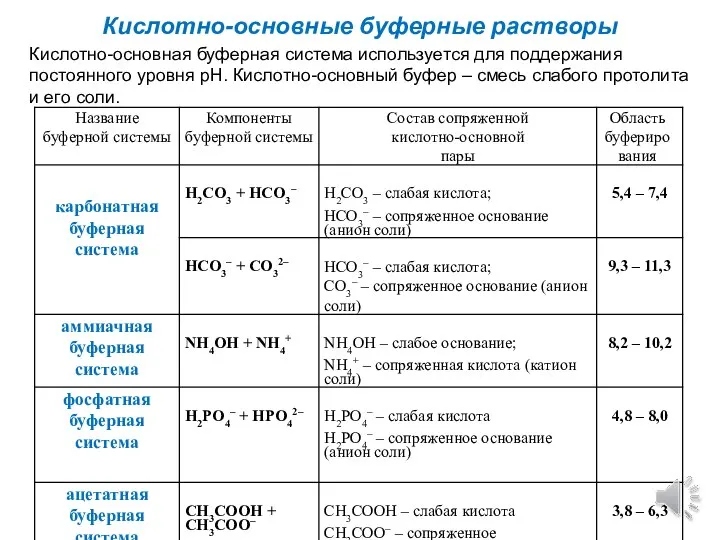
- 4. Кислотно-основные буферные растворы Кислотно-основная буферная система используется для поддержания постоянного уровня рН. Кислотно-основный буфер – смесь
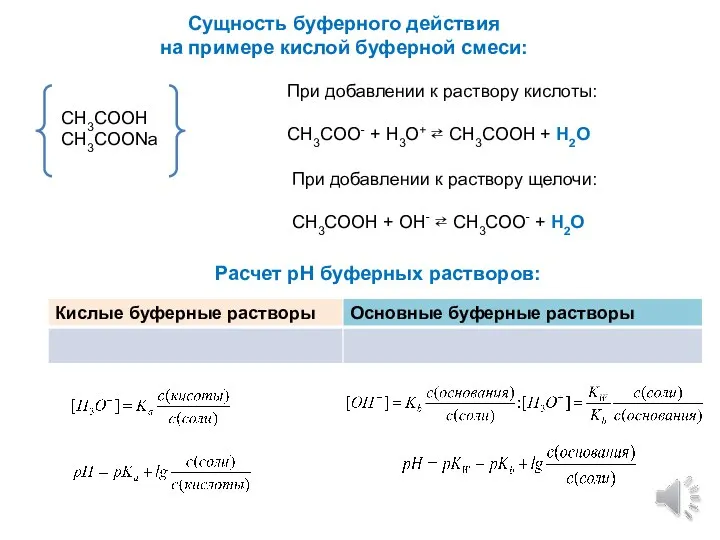
- 5. Сущность буферного действия на примере кислой буферной смеси: CH3COOH CH3COONa При добавлении к раствору кислоты: CH3COO-
- 6. Вычислить рН раствора, полученного сливанием 20 мл 0,015 М раствора нитрита натрия и 15 мл раствора
- 7. Свойства буферных растворов Значение рН буферного раствора остается неизменным при разбавлении; При добавлении кислот или щелочей
- 8. Формулы для расчета концентрации ионов H+ в растворах протолитов
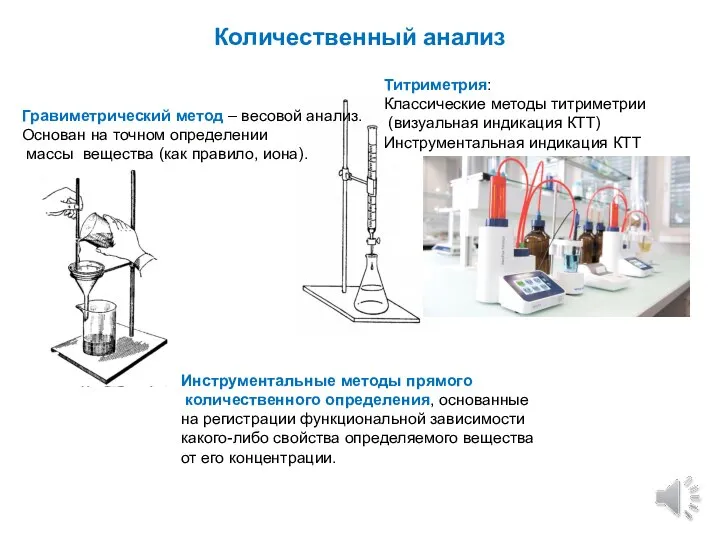
- 9. Количественный анализ Гравиметрический метод – весовой анализ. Основан на точном определении массы вещества (как правило, иона).
- 11. Скачать презентацию





 Сложные эфиры. Жиры
Сложные эфиры. Жиры Кинетика катодного выделения водорода на дисилициде хрома в щелочном и кислом электролитах
Кинетика катодного выделения водорода на дисилициде хрома в щелочном и кислом электролитах Электролиз расплавов и растворов электролитов
Электролиз расплавов и растворов электролитов Презентация на тему Гормоны
Презентация на тему Гормоны  Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Альдегиды, строение и свойства
Альдегиды, строение и свойства Водородная химическая связь
Водородная химическая связь Природный и попутный газы, их состав и использование
Природный и попутный газы, их состав и использование Описание молекул
Описание молекул Роль металлов в искусстве
Роль металлов в искусстве Диаграмма состояния BaO-Al2O3-SiO2
Диаграмма состояния BaO-Al2O3-SiO2 Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы
Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы Приключение кислорода
Приключение кислорода Презентация на тему Самородки
Презентация на тему Самородки  Мышьяк. Висмут. Сурьма
Мышьяк. Висмут. Сурьма Лекарственные растения содержащие флавоноиды
Лекарственные растения содержащие флавоноиды Алкины. Строение
Алкины. Строение Химия вокруг нас и для нас
Химия вокруг нас и для нас Алюминий
Алюминий Строение, свойства и функции аминокислот и белков
Строение, свойства и функции аминокислот и белков Сода. Что я знаю о ней!?
Сода. Что я знаю о ней!? Равновесия в растворах электролитов. Окислительно-восстановительные реакции
Равновесия в растворах электролитов. Окислительно-восстановительные реакции Кислотные оксиды
Кислотные оксиды Презентация на тему Анализ качества питьевой воды
Презентация на тему Анализ качества питьевой воды  Презентация на тему Алхимики
Презентация на тему Алхимики  Растворение. Экспериментальная работа с веществами
Растворение. Экспериментальная работа с веществами Презентация на тему Основные законы науки химии
Презентация на тему Основные законы науки химии  Химическая связь
Химическая связь