Содержание
- 2. НЕМЕТАЛЛЫ- ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ ,У КОТОРЫХ НА ПОСЛЕДНЕМ ЭНЕРГИТИЧЕСКОМ УРОВНЕ НАХОДИТСЯ ОТ 4 ДО 8 ЭЛЕКТРОНОВ
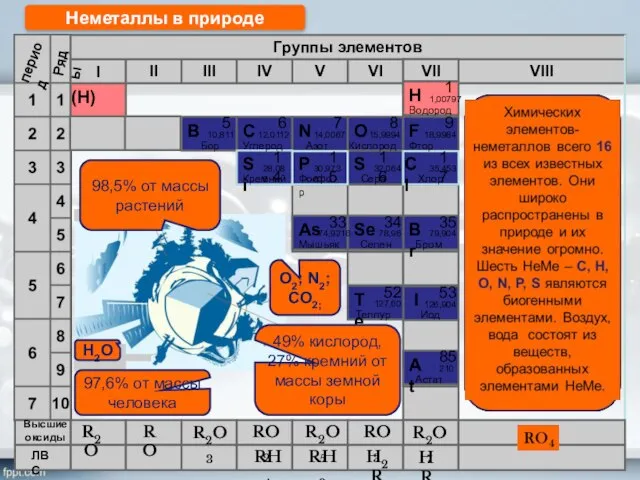
- 3. R2O RO R2O3 RO2 R2O5 RO3 R2O7 RH4 RH3 H2R HR Высшие оксиды ЛВС Неметаллы в
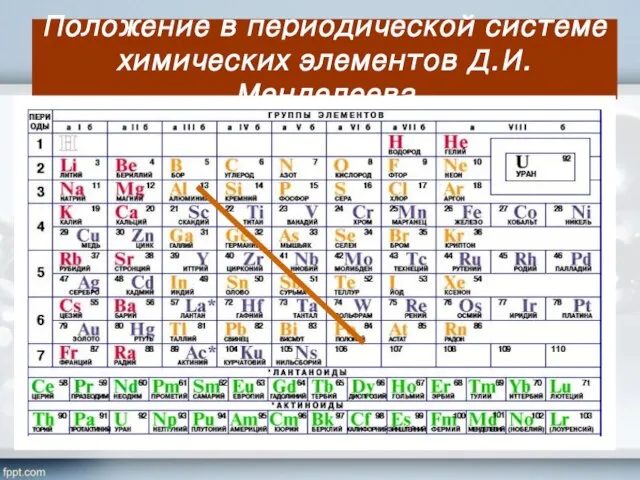
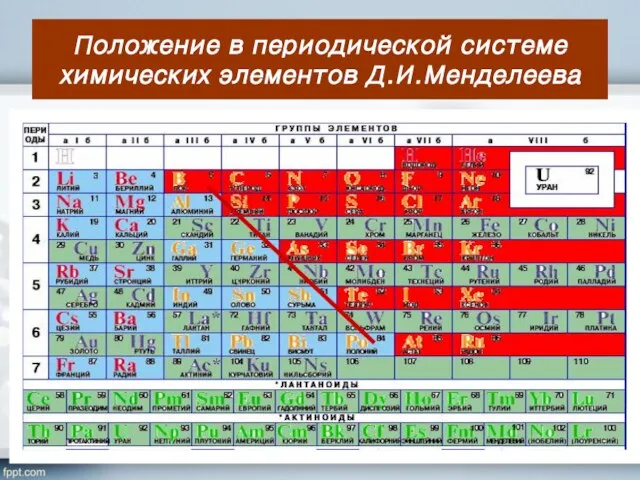
- 4. Положение в периодической системе химических элементов Д.И.Менделеева
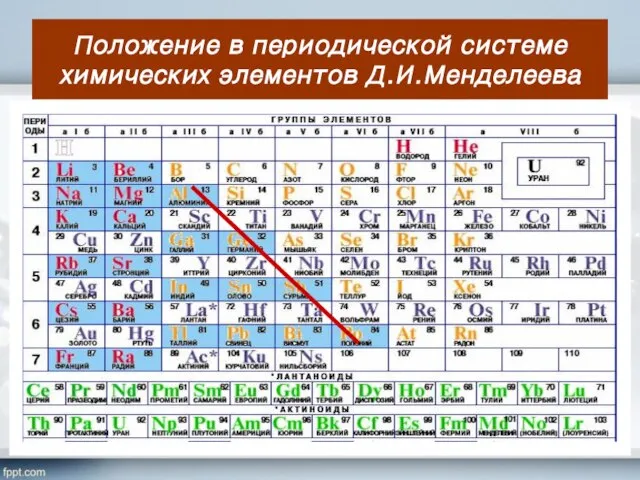
- 5. Положение в периодической системе химических элементов Д.И.Менделеева
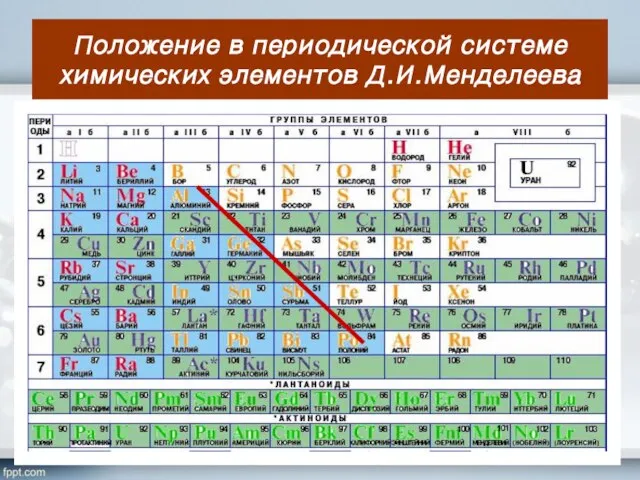
- 6. Положение в периодической системе химических элементов Д.И.Менделеева
- 7. Положение в периодической системе химических элементов Д.И.Менделеева
- 8. Особенности атомного строения неметаллов Небольшой атомный радиус На внешнем уровне 4-8 электронов Располагаются только в главных
- 9. Электроотрицательность – это свойство атомов химических элементов поляризовать химическую связь, оттягивать к себе общие электронные пары
- 10. ФИЗИЧЕСКИЕ СВОЙСТВА ПРОСТЫХ ВЕЩЕСТВ
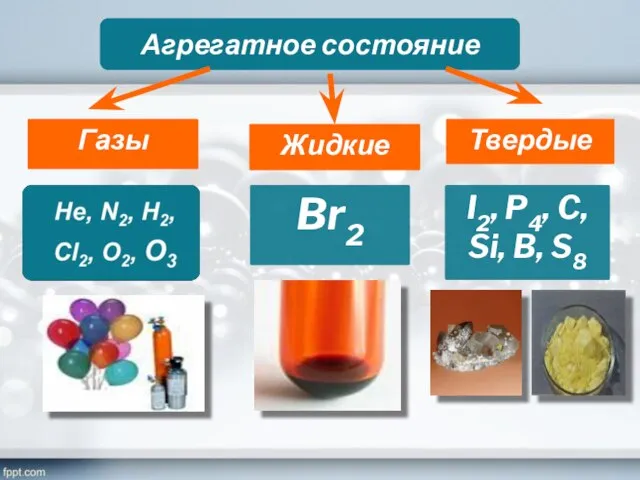
- 11. Агрегатное состояние Газы Жидкие Твердые Br2 I2, P4, C, Si, B, S8
- 12. Цвет неметаллов КРАСНЫЙ ЖЕЛТЫЙ ФИОЛЕТОВЫЙ ФОСФОР СЕРА ЙОД БЕСЦВЕТНЫЙ УГЛЕРОД
- 13. В чем причина разнообразия физических свойств у неметаллов ?
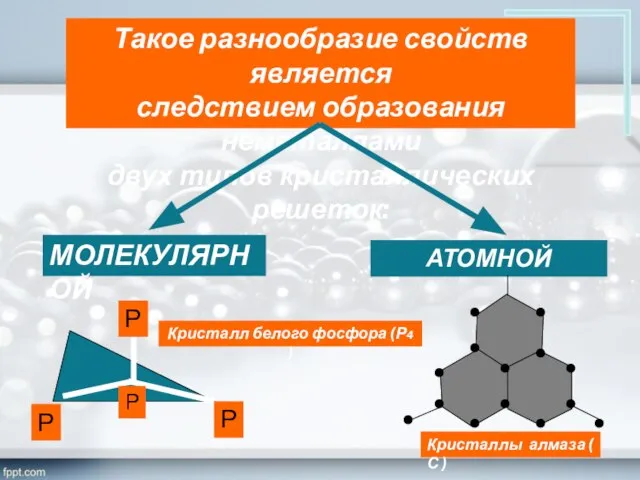
- 14. Такое разнообразие свойств является следствием образования неметаллами двух типов кристаллических решеток: МОЛЕКУЛЯРНОЙ АТОМНОЙ Р Р Р
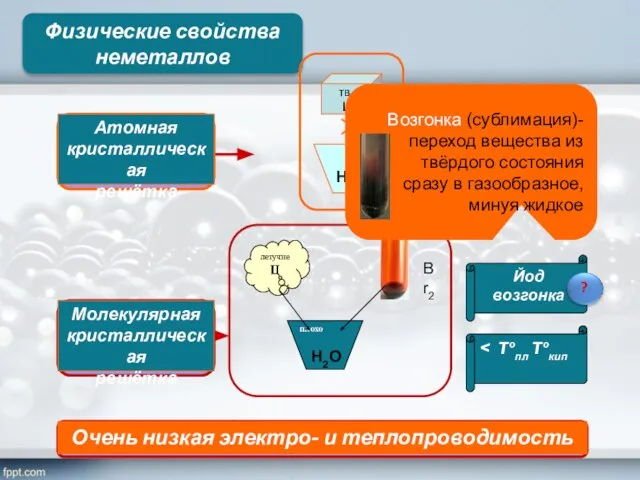
- 15. Физические свойства неметаллов > Tºпл Tºкип Йод возгонка Н2О Н2О
- 16. Аллотро́пия (от др-греч. αλλος — «другой», τροπος — «поворот, свойство») — существование одного и того же
- 17. Причины аллотропии: Разные типы кристаллических решеток (белый фосфор Р4 – молекулярная, красный фосфор Р – атомная).
- 18. Элементарный фосфор в обычных условиях представляет собой несколько устойчивых аллотропных модификаций; вопрос аллотропии фосфора сложен и
- 19. Ромбическая (a - сера) - S8 t°пл. = 113°C; ρ = 2,07 г/см3. Наиболее устойчивая модификация.
- 21. Скачать презентацию










 Фуллерены (шары Бакминстера)
Фуллерены (шары Бакминстера) Алюминий и его органические производные
Алюминий и его органические производные Презентация на тему Кристаллические решетки 9 класс
Презентация на тему Кристаллические решетки 9 класс  Энергетический обмен
Энергетический обмен Ионная связь
Ионная связь Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+
Генетические ряды Fe2+ и Fе3+. Качественные реакции на Fе2+ и Fе3+ Презентация на тему Йод
Презентация на тему Йод  Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов
Роль Хеуорса, Фишера, Лемье в изучении структуры углеводов Конструкционные и специальные материалы холодильной техники
Конструкционные и специальные материалы холодильной техники Перициклические реакции
Перициклические реакции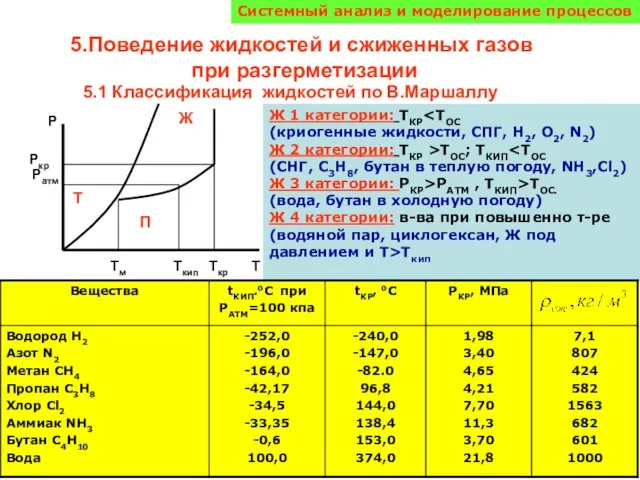 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот
Контроль качества лекарственных средств, производных карбоновых кислот и аминокислот Получение армированных фотополимерных композиций
Получение армированных фотополимерных композиций Group 6 Cations
Group 6 Cations Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева
Русские ученые и топонимы в периодической системе химических элементов Д.И. Менделеева Пищевые кислоты
Пищевые кислоты Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы Полиамиды (ПА)
Полиамиды (ПА) Окислители в пиросоставах
Окислители в пиросоставах Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Совместимость материалов
Совместимость материалов Молярная масса вещества
Молярная масса вещества Композитные материалы
Композитные материалы Типы химической связи
Типы химической связи Презентация на тему Законы газового состояния вещества
Презентация на тему Законы газового состояния вещества  Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry
Development of the system of concepts on the topic redox reactions in the school course of inorganic chemistry Аммиак: состав, строение, свойства, применение
Аммиак: состав, строение, свойства, применение