декларации 1948 г., Хельсинской декларации 1964 г., которая в дальнейшем многократно пересматривалась и дополнялась по результатам различных международных конгрессов врачей. Еще одним определяющим документом стал подготовленный американской Комиссией по защите человеческих субъектов биомедицинских и поведенческих исследований Бельмонтский отчет «Этические принципы и рекомендации по защите человека при проведении исследований» (1979 г.), посвященной использованию людей в научных исследованиях, которая проходила в Центре Бельмонта (Елкридж, Мэриленд, США) в феврале 1976 г.
Юридическая необходимость получения информированного согласия основывается на ряде основополагающих международных документов: Женевской декларации 1948 г., Хельсинской декларации 1964 г., которая в дальнейшем многократно пересматривалась и дополнялась по результатам различных международных конгрессов врачей. Еще одним определяющим документом стал подготовленный американской Комиссией по защите человеческих субъектов биомедицинских и поведенческих исследований Бельмонтский отчет «Этические принципы и рекомендации по защите человека при проведении исследований» (1979 г
Международные документы, регулирующие необходимость получения информированного согласия:
Нюрнбергский кодекс 1947 г.,
Женевская декларация 1948 г.,
Хельсинская декларация 1964.,
Лиссабонская декларация о правах пациента 1981 г., Декларация о политике в области обеспечения прав пациента в Европе 1994 г.,
Конвенция о защите прав человека и достоинства человеческого существа в связи с использованием достижений биологии и медицины 1997 г.,
Конвенция о защите прав и достоинства человека в области биомедицины: конвенция о биомедицине и правах человека 1997 г.,
Европейская хартия прав пациентов 2002 г.,










 Значение анатомо-физиологических особенностей детского организма при организации ухода за детьми
Значение анатомо-физиологических особенностей детского организма при организации ухода за детьми Методика Child–Pugh score.MELD
Методика Child–Pugh score.MELD Artificial heart
Artificial heart Хламидиоз
Хламидиоз Патофизиология почек
Патофизиология почек Гипофиздің аденомасы
Гипофиздің аденомасы Средства и формы ЛФК
Средства и формы ЛФК Celtra Press. Клиническое образование
Celtra Press. Клиническое образование Имплантация в стоматологии
Имплантация в стоматологии БД Факторы риска онкология
БД Факторы риска онкология Ишемический колит
Ишемический колит Гностические зрительные расстройства
Гностические зрительные расстройства Антигены
Антигены Железодефицитная анемия
Железодефицитная анемия Инфузионная терапия и применение инотропных препаратов в неонатологии
Инфузионная терапия и применение инотропных препаратов в неонатологии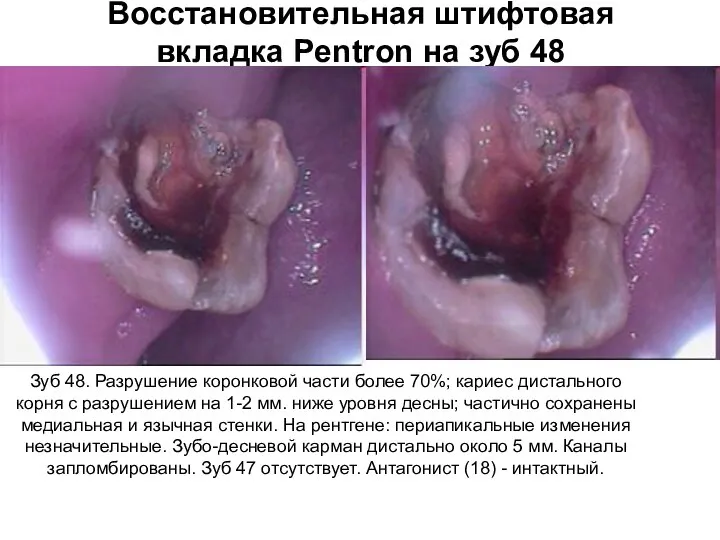 Восстановительная штифтовая вкладка Pentron на зуб 48
Восстановительная штифтовая вкладка Pentron на зуб 48 Анатомо-физиологические особенности сердечно-сосудистой системы у детей
Анатомо-физиологические особенности сердечно-сосудистой системы у детей Плевра куысына сұйықтық жиналу синдромы. Тыныс жетіспеушілігі синдромы
Плевра куысына сұйықтық жиналу синдромы. Тыныс жетіспеушілігі синдромы Хроническая патология органов пищеварения у детей
Хроническая патология органов пищеварения у детей Патогенез и методы диагностики острых нарушений мозгового кровообращения
Патогенез и методы диагностики острых нарушений мозгового кровообращения Инфекции
Инфекции Методы диагностики беременности и бесплодия
Методы диагностики беременности и бесплодия Фармакогенетика. Фармакогенетикадағы дәрілік заттың генетикалық факторға қатысы
Фармакогенетика. Фармакогенетикадағы дәрілік заттың генетикалық факторға қатысы Болезни нервной системы
Болезни нервной системы Экрадент. Возрождение космических технологий в стоматологии
Экрадент. Возрождение космических технологий в стоматологии Ревматизм
Ревматизм Лекарственные средства, применяемые при недостаточности коронарного кровообращения (антиангинальные средства)
Лекарственные средства, применяемые при недостаточности коронарного кровообращения (антиангинальные средства) ЖШС Амиран шаруашылығындағы сауын қондырғыларын санитариялық өңдеу шараларының тиімділігін бағалау
ЖШС Амиран шаруашылығындағы сауын қондырғыларын санитариялық өңдеу шараларының тиімділігін бағалау