Содержание
- 2. Актуальность Инфаркт головного мозга (ИМ) остается одной из основных причин инвалидности и смертности населения несмотря на
- 3. Актуальность Согласно данным международных статистических исследований отмечается рост заболеваемости ИМ лиц молодого возраста (МВ) на 23%-53%
- 4. Актуальность Несмотря на профилактику, в среднем в течение 2-х лет у 21% лиц, развивается повторный ИМ*.
- 5. ИМ часто считают болезнью пожилого человека, однако по данным исследования INTERSTROKE около 14% составляют пациенты моложе
- 6. Прогноз инфаркта мозга у молодых vs пожилых пациентов ниже смертность ниже частота рецидивов лучше функциональное восстановление*
- 7. Не уточнена долгосрочность периода использования антитромботической, гиполипидемической, антигипертензивной терапии, если у лиц пожилого возраста после инсульта
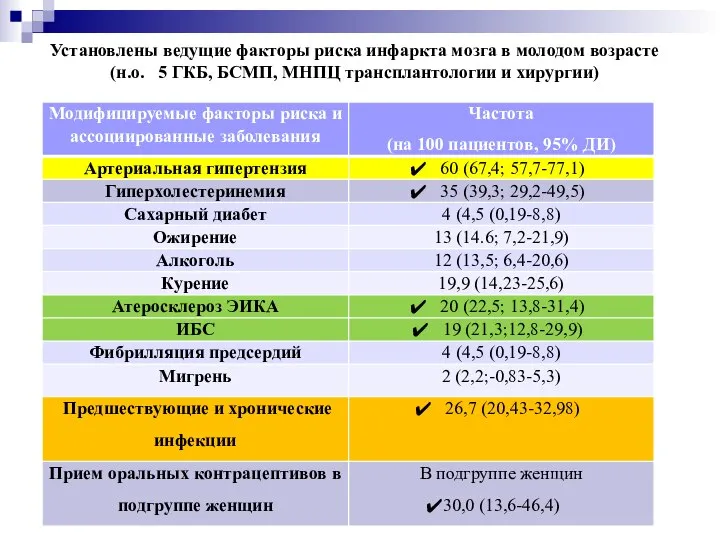
- 8. Установление факторов риска* Объектом исследования откуда 406 , ведь инсульт=356 , а 235 это что ?????
- 10. Стратегия вторичной профилактики инфаркта мозга в молодом возрасте (не позднее 48 часов) Определение этиопатогенетического подтипа Коррекция
- 11. Классификация инсультов на основе патофизиологических признаков по критериям TOAST: Атеросклероз крупных артерий: инфаркт в бассейне внечерепных
- 12. Варфарин Клопидогрел Статины Настоящий доклад посвящен особенностям фармако… статинов у лиц молодого возраста
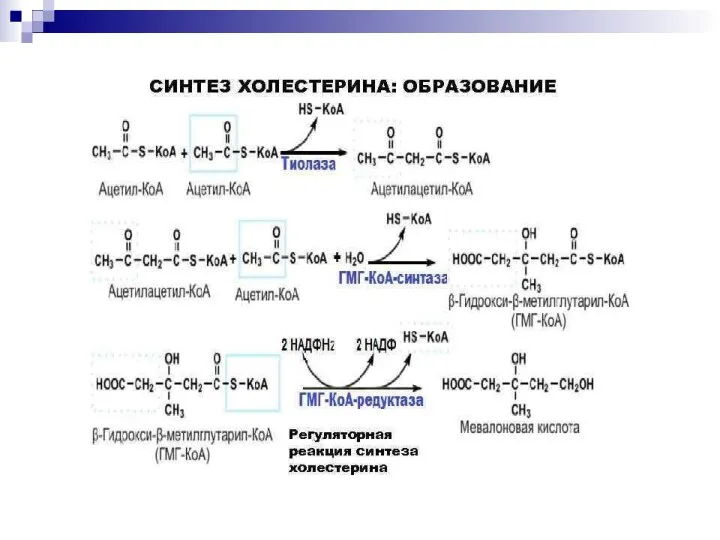
- 13. Статины Статины или ингибиторы 3-гидрокси-3- метилглутарил-коэнзим А редуктазы (ГМГ-КoA – редуктаза) - основная группа препаратов, снижающих
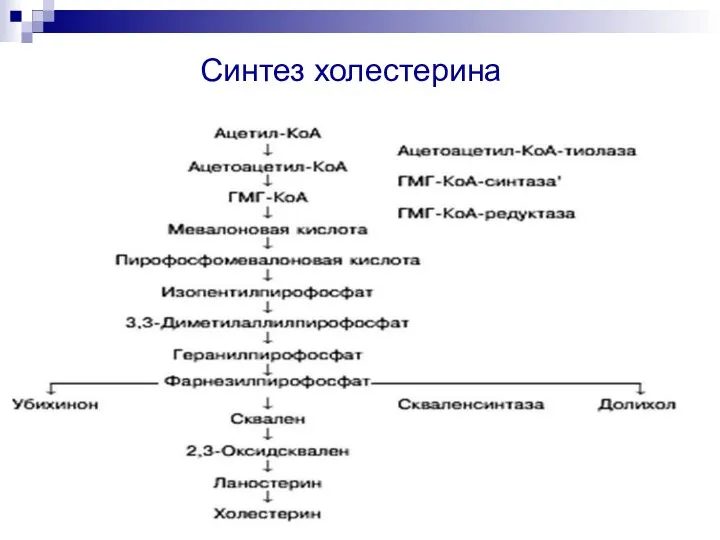
- 14. Синтез холестерина
- 16. Цель исследования: Изучить частоту полиморфных аллелей генов SLCO1B1, ABCB1, ABCG2 , ассоциированных с биотрансформацией и механизмом
- 17. Цель исследования: Данное исследование направлено на выполнение трех практических целей: Обеспечить выбор лекарственного средства и его
- 18. Побочные эффекты статинов «Непереносимость статинов» - EAS (10-15%)* 1. Статин-индуцированная миопатия (СИМ): (7-29%)** -Миалгия -Миопатия -Миозит
- 19. Побочные эффекты статинов 2. Новые случаи сахарного диабета и инсулинорезистентность (Food and drug administration, США; European
- 20. Объект исследования: Основная группа ИМ − 148 пациентов (92 мужчина, 56 женщины), обследованных на клинических базах
- 21. Материалы и методы Для генотипирования пациентов были использованы методы ПЦР-ПДРФ анализа и аллель-специфичной ПЦР с линейными
- 22. Вариабельность фармакологического ответа при применении статинов зависит от полиморфизма генов, продукты которых ответственны за процессы фармакокинетики
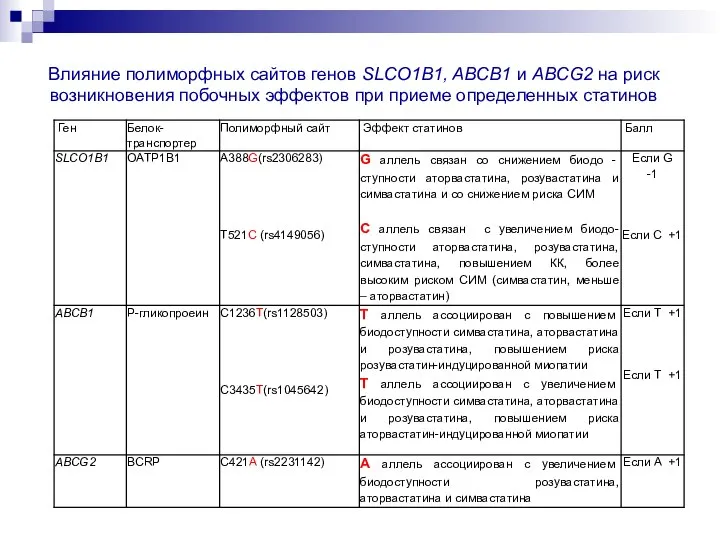
- 23. Влияние полиморфных сайтов генов SLCO1B1, ABCB1 и ABCG2 на риск возникновения побочных эффектов при приеме определенных
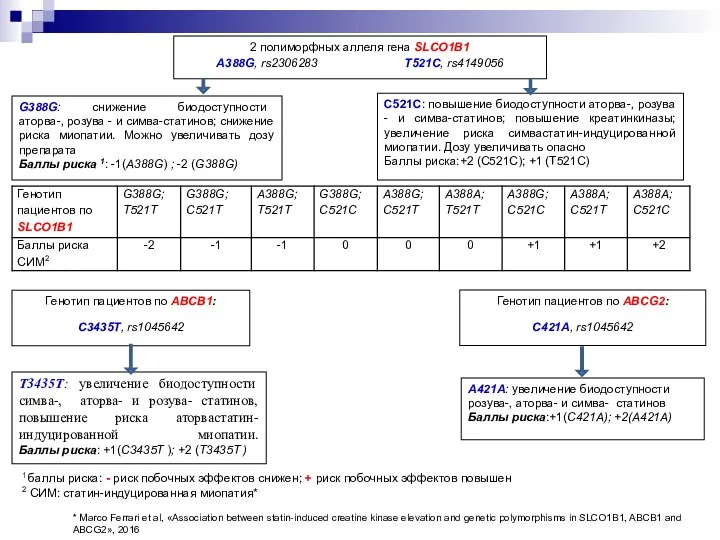
- 24. 2 полиморфных аллеля гена SLCO1B1 A388G, rs2306283 Т521C, rs4149056 G388G: снижение биодоступности аторва-, розува - и
- 25. Влияние полиморфных сайтов генов SLCO1B1, ABCB1 и ABCG2 на риск возникновения побочных эффектов при приеме определенных
- 26. Результаты Аллель А388G гена SLCO1B1, как показано в обзоре литературы, является благоприятным для его носителей при
- 27. Результаты У пациентов, несущих аллель риска T521C, значительно медленнее снижается титр липопротеинов низкой плотности, такие пациенты
- 28. Результаты 1.В зависимости от различия пациентов по полиморфным аллелям гена SLCOB1 у 56 пациентов (40,9%) выявлен
- 29. У скольких пациентов применялось знание фармакогенетики Хотя бы знать, как ответить, если кто то спросит Надо
- 30. Выводы Знание генетического статуса конкретного пациента по определенным генам, определяющим во многом течение заболевания и эффективность
- 32. Скачать презентацию
























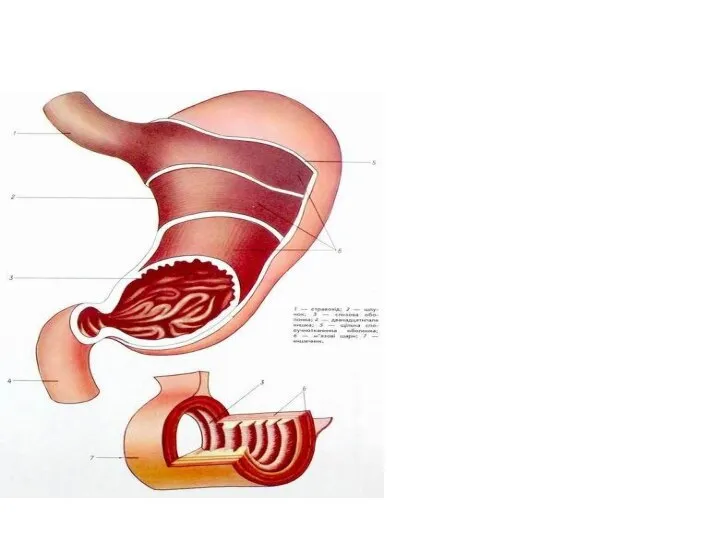 Пищеварение в желудке
Пищеварение в желудке Правильное питание и последствия его нарушения
Правильное питание и последствия его нарушения Соединения костей плечевого пояса. Локтевой и лучезапястные суставы. Соединения кисти
Соединения костей плечевого пояса. Локтевой и лучезапястные суставы. Соединения кисти Размер прибыли в структуре цены. Взаиморасчеты между организациями
Размер прибыли в структуре цены. Взаиморасчеты между организациями Medications
Medications Методы стапедопластики
Методы стапедопластики Зачетная работа. МРТ брюшной полости
Зачетная работа. МРТ брюшной полости ЖИВАЯ МАТЕРИЯ ПРИ НИЗКИХ И СВЕРХНИЗКИХ ТЕМПЕРАТУРАХ И. В. Артюхов
ЖИВАЯ МАТЕРИЯ ПРИ НИЗКИХ И СВЕРХНИЗКИХ ТЕМПЕРАТУРАХ И. В. Артюхов Phylogentic disorders of skeletal system
Phylogentic disorders of skeletal system Вакцинопрофилактика у ВИЧ-инфецированых и ВИЧ-экспонированых детей
Вакцинопрофилактика у ВИЧ-инфецированых и ВИЧ-экспонированых детей Техника инъекций
Техника инъекций Нарушения жирового, минерального и пигментного обмена
Нарушения жирового, минерального и пигментного обмена Заболевания молочной железы
Заболевания молочной железы Регуляция дыхания
Регуляция дыхания Методы обследования ребёнка в практике врача детского стоматолога
Методы обследования ребёнка в практике врача детского стоматолога Значение пищи и ее состав
Значение пищи и ее состав Техника упражнений на формирование правильной осанки
Техника упражнений на формирование правильной осанки Наркомания. Стадии наркомании. Принципы лечения
Наркомания. Стадии наркомании. Принципы лечения 3_glotka
3_glotka Раны. Определение. Классификация. Общие и местныесимптомы
Раны. Определение. Классификация. Общие и местныесимптомы Профилактические осмотры женского населения
Профилактические осмотры женского населения Факторы, влияющие на качество занятия иппотерапией, РВЕ и ОВЕ
Факторы, влияющие на качество занятия иппотерапией, РВЕ и ОВЕ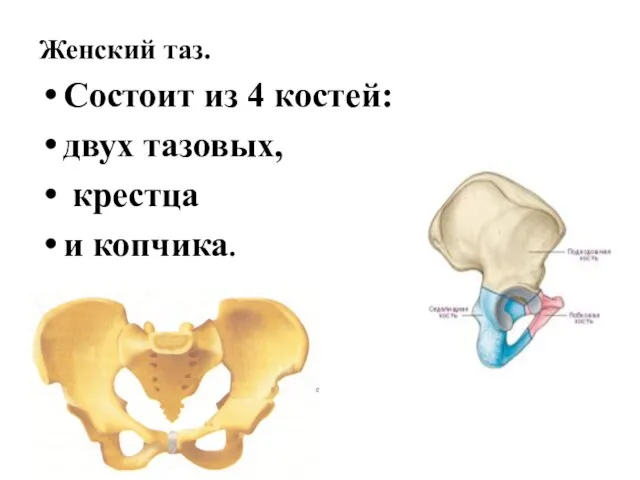 Женский таз
Женский таз Пневмония, воспаление лёгких. Классификация пневмоний
Пневмония, воспаление лёгких. Классификация пневмоний Предимплантационная генетическая диагностика
Предимплантационная генетическая диагностика Травянистое растение цикорий
Травянистое растение цикорий Рентгенологическая картина некоторых, редко встречающихся патологий
Рентгенологическая картина некоторых, редко встречающихся патологий Стандартизация стоматологической продукции
Стандартизация стоматологической продукции