Слайд 2Актуальность
Все уже слышали о пандемии коронавируса COVID-19. Количество стран, где есть заболевшие,

с каждым днем увеличивается, также растет и количество больных. Статистика обновляется и публикуется ежедневно многими СМИ, информации о вирусе много.
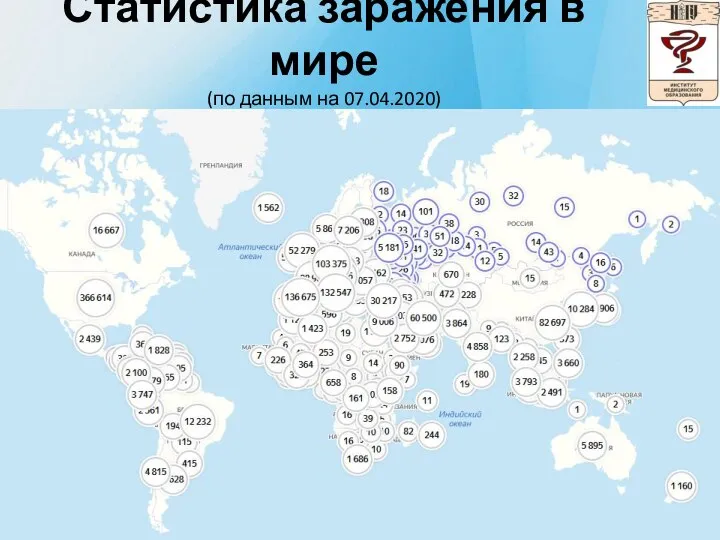
Всего в мире, по данным Всемирной организации здравоохранения, заразились около 1,15 миллиона человек, почти 63 тысячи больных скончались.
Слайд 3Статистика заражения в мире
(по данным на 07.04.2020)
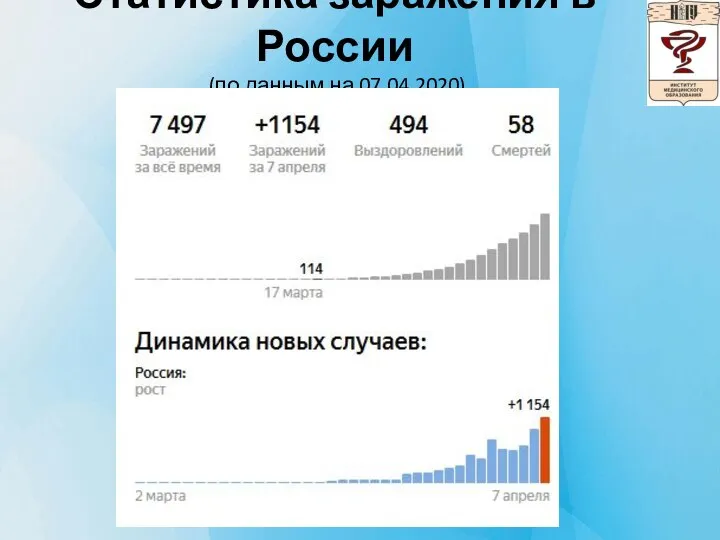
Слайд 4Статистика заражения в России
(по данным на 07.04.2020)
Слайд 5Диагностика
В качестве диагностики COVID-19 применяют методы лабораторной и инструментальной диагностики.

Слайд 6Лабораторная диагностика
Используются такие методы как:
Забор материала (мазки/смывы из носа и зева, мокрота)
Обнаружение

нуклеиновой кислоты SARS-CoV-2
Выделение и культивирование вируса
Обнаружение сывороточного антитела
Выявление индикаторов воспалительной реакции
Обнаружение вторичных бактериальных или грибковых инфекций
Слайд 7Обнаружение нуклеиновой кислоты SARS-CoV-2
Образцы подвергаются предварительной обработке, и вирус подвергается лизису для

вычленения нуклеиновых кислот. Три специфических гена SARS-CoV-2, а именно:
открытая рамка считывания 1a/b (ORF1a/b),
гены нуклеокапсидного белка (N) и
белка оболочки (E) —затем амплифицируются по методике количественной ПЦР в реальном времени. Амплифицированные гены обнаруживаются интенсивности флуоресценции.
Назовем критерии положительных результатов анализа на нуклеиновые кислоты: Положительный тест на ген ORF1a/b и (или) ген N (ген E).
Слайд 8Выделение и культивирование вируса
У пациента берутся свежие образцы мокроты, кала и другие

пробы, после чего они инокулируются в клетках Vero-E6 для культивирования вируса. Цитопатический эффект наблюдается через 96 часов. Обнаружение вирусной нуклеиновой кислоты в культуральной среде свидетельствует об успешном культивировании.
Определение титра вируса: После последовательного растворения вирусного посевного материала в 10 раз TCID50 определяется микроцитопатическим методом. В противном случае жизнеспособность вируса определяется бляшкообразующей единицей.
Слайд 9Обнаружение сывороточного антитела
После заражения SARS-CoV-2 образуются специфические антитела.
К методам определения сывороточных

антител относятся иммунохроматография с использованием коллоидного золота, твёрдофазный иммуноферментный анализ, иммунохемилюминесценция и др. Положительный результат анализа на антигенспецифичный сывороточный титр класса IgM —или если титр специфических антител класса IgG в фазе выздоровления в≥4 раза выше по сравнению с острой фазой —можно использовать в качестве диагностических критериев у пациентов с подозрением на COVID-19 и отрицательным результатом обнаружения нуклеиновых кислот.
Во время диспансерного наблюдения IgM обнаруживается через10 дней после появления симптомов, IgG —через 12. Вирусная нагрузка постепенно уменьшается по мере увеличения уровня сывороточных антител.
Слайд 10Выявление индикаторов воспалительной реакции
Рекомендуется сдавать анализы на C-реактивный белок, прокальцитонин, ферритин, D-димер,

общее содержание и субпопуляции лимфоцитов, интерлейкинов IL-4, IL-6, IL-10, TNF-α, INF-у и другие индикаторы воспаления и иммунного статуса, которые могут помочь оценить клиническое течение болезни, оповещать о тяжелых и критических состояниях, а также служить основой для формирования стратегий лечения.
У большинства пациентов с COVID-19 нормальный уровень прокальцитонина и существенно повышенный уровень C-реактивного белка. Быстрое и существенное повышение уровня C-реактивного белка указывает на возможность вторичной инфекции. В тяжелых случаях уровень D-димера существенно возрастает, что потенциально служит фактором риска для неблагоприятного прогноза. У пациентов с общим низким количеством лимфоцитов в начале болезни обычно неблагоприятный прогноз. У пациентов в тяжелом состоянии неуклонно уменьшается количество лимфоцитов периферической крови. Уровень экспрессии IL-6 и IL-10 у пациентов в тяжелом состоянии значительно повышается. Контроль уровня IL-6 и IL-10 помогает оценить риск развития тяжелого состояния.
Слайд 11Обнаружение вторичных бактериальных или грибковых инфекций
Пациенты в тяжелом или критическом состоянии

подвержены риску развития вторичных бактериальных или грибковых инфекций. При подозрении на вторичную легочную инфекцию следует брать образцы мокроты, выделяемой из глубины лёгких, трахейных аспиратов, бронхоальвеолярного лаважа и щёточные образцы для культивирования.
У пациентов с высокой температурой следует своевременно брать посев крови.
У пациентов с подозрением на сепсис, которым был установлен постоянный катетер, следует брать посевы крови из периферических внутривенных катетеров. Рекомендуется брать у них анализ крови класса G и GM не реже двух раз в неделю, помимо посева на грибы.
Слайд 12Инструментальная диагностика
В качестве инструментальных методов исследования выделим компьютерную томографию и бронхоскопию.
Слайд 13Компьютерная томография
Торакальная томография чрезвычайно важна в диагностике COVID-19, контроле терапевтической эффективности и

оценки готовности пациента к выписке. На ранних стадиях COVID-19 часто обнаруживаются многоочаговые тени или субплевральные фокусы уплотнения по типу «матового стекла», расположенные на периферии лёгких, в субплевральной зоне и обеих нижних долях на снимках КТ грудной клетки. Длинная ось поражённого участка по большей части параллельна плевре. В некоторых случаях субплевральных фокусов уплотнения по типу «матового стекла» наблюдаются междольковые септальные утолщения и внутридольковые интерстициальные утолщения, которые выглядят как субплевральный сетчатый узор, а именно: рисунок «булыжной мостовой». В небольшом числе случаев могут наблюдаться одиночные, локальные поражения или узелковое (очаговое) поражение, распределенное в соответствии с бронхом, с периферийными изменениями в виде субплевральных фокусов уплотнения по типу «матового стекла». Прогрессирование заболевания наблюдается по большей части в течение 7—10 дней, при этом нарастает и увеличивается плотность поражённых участков по сравнению с предыдущими снимками, а также наблюдаются уплотнённые поражённые участки с признаком воздушной бронхограммы. В критических случаях может наблюдаться дальнейшее разрастание уплотнения, когда плотность всего лёгкого в целом демонстрирует повышенную замутнённость, иногда это называется «белое лёгкое».
Слайд 14Компьютерная томография
(Продолжение)
После того, как состояние пациента улучшится, субплевральные фокусы уплотнения по типу

«матового стекла» могут полностью рассосаться, а некоторые уплотнённые поражённые участки оставят после себя фиброзные полоски или субплевральный сетчатый узор. Пациенты с несколькими дольковыми поражениями, особенно с обширными поражёнными участками, должны оставаться под наблюдением на предмет обострения заболевания. Пациенты с характерными лёгочными проявлениями заболевания на снимках КТ должны быть изолированы и постоянно сдавать анализы на нуклеиновую кислоту, даже если анализ на нуклеиновую кислоту SAR-CoV-2 показал отрицательный результат.
Слайд 151,2 - очаговые субплевральные фокусы уплотнения по типу «матового стекла»;
3 - :
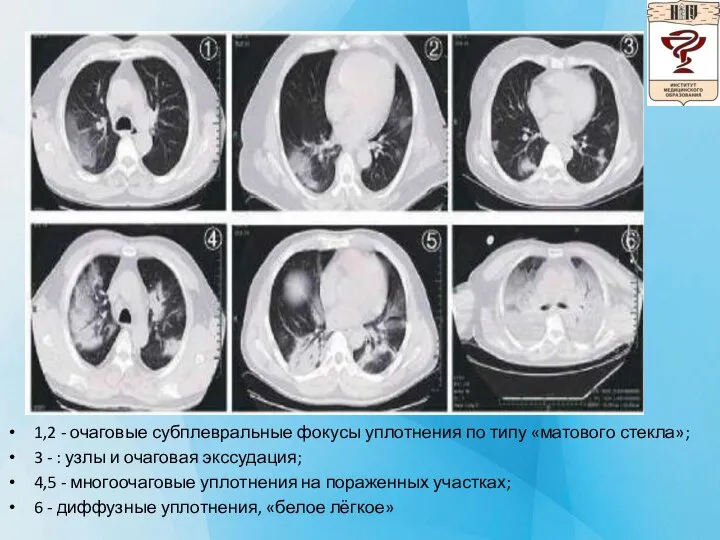
узлы и очаговая экссудация;
4,5 - многоочаговые уплотнения на пораженных участках;
6 - диффузные уплотнения, «белое лёгкое»
Слайд 16Бронхоскопия
Бронхоскопия с гибким видеоэндоскопом является универсальным методом, который прост в использовании и

хорошо переносится у пациентов, инфицированных COVID-19, находящихся на искусственной вентиляции. Его применение включает в себя:
Сбор образцов из нижних дыхательных путей (т.е. мокроты, эндотрахеального аспирата, бронхоальвеолярного лаважа) для выявления SARS-CoV-2 или других возбудителей помогает определить выбор соответствующих антимикробных препаратов, что может привести к благоприятным клиническим результатам. Наш опыт показывает, что образцы из нижних дыхательных путей с большей вероятностью могут быть положительными при анализе на SAR-CoV-2, чем образцы верхних дыхательных путей.
Возможно использование этого метода для локализации очага кровотечения, купирования кровохарканья, удаления мокроты или сгустков крови; если очаг кровотечения выявлен с помощью бронхоскопии, то с помощью бронхоскопа можно проводить местную инъекцию холодного физиологического раствора, эпинефрина, вазопрессина или фибрина, а также лазерное лечение.
Помощь в создании искусственных дыхательных путей; контроль интубации трахеи или чрескожной трахеотомии.
Такие препараты, как α-интерферон и N-ацетилцистеин, можно вводить через бронхоскоп.
Слайд 17Бронхоскопические проявления COVID-19
Отек и застойные явления на слизистой оболочки бронхов; большое количество
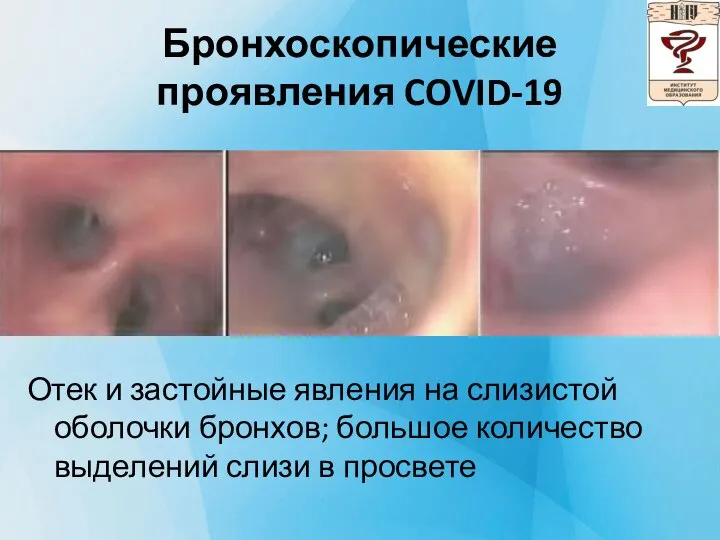
выделений слизи в просвете
Слайд 18Лечение
Противовирусное лечение
Противоударное и анти-гипоксемийное лечение
Слайд 19Противовирусное лечение
Лопинавир/ритонавир (2 капсулы, каждые12 ч) в сочетании с арбидолом (200 мг

каждые 12 ч). Из опыта лечения 49 пациентов до получения отрицательного результата теста на вирусную нуклеиновую кислоту в первый раз составило 12 дней (95% (8-15 дней)). Длительность отрицательного результата теста на нуклеиновую кислоту (отрицательного более 2 раз подряд с интервалами ≥24 ч) составила 13,5 суток (95% (9.5-17.5 дней)). Если основной режим не эффективен, то хлорохинфосфат можно применять у взрослых в возрасте от 18 до 65 лет (вес ≥50 кг: 500 мг ставки; вес ≤50 кг: 500 мг ставки в течение первых двух дней, 500 мг в сутки в течение следующих пяти дней).
Интерфероновая ингаляция рекомендуется в протоколах диагностики и лечения COVlD-19. Рекомендуется проводить его в палатах с отрицательным давлением, а не в палатах общего назначения из-за возможности передачи аэрозоля. Дарунавир / кобицистат обладает определенной степенью противовирусной активности в месте подавления вирусов in vitro, основанном на опыте лечения больных СПИДом, и побочные эффекты относительно слабы.
Для пациентов, которые имеют непереносимость лопинавира/ритонавира, дарунавира/ кобицистата (1 таблетка в сутки) или фавипиравира (начальная доза 1600 мг с последующим 600 мг 2 р/с) является альтернативным вариантом после этического рассмотрения. Одновременное применение трех и более противовирусных препаратов не рекомендуется.
Слайд 20Противоударное и анти-гипоксемийное лечение
Применение глюкокортикоидов при необходимости
Лечение искусственной поддержкой печени для подавления

цитокинового каскада
Кислородная терапия для гипоксемии
Слайд 21Применение глюкокортикоидов
Рекомендуется начальный рутинный прием метилпреднизолона в дозе 0,75~1,5 мг/кг внутривенно

один раз в день (почти 40 мг один или два раза в день). Однако метилпреднизолон в дозе 40 мг каждые 12ч можно рассматривать для пациентовс понижающейся температурой тела или для пациентов со значительно повышенными цитокинами при рутинных дозах стероида. Даже метилпреднизолон в дозе 40 мг-80 мг каждые 2 ч можно рассматривать в критических случаях. Внимательно контролируйте температуру тела, насыщение крови кислородом, режим работы крови, С-реактивный белок, цитокины, биохимический профиль и КТ легких каждые 2-3 дня во время лечения по мере необходимости. Дозировка метилпреднизолона должна быть уменьшена вдвое каждые 3-5 дней, если состояниездоровья пациентов улучшается, температура тела нормализуется или вовлеченные поражения на КТ значительно всасываются. Пероральный метилпреднизолон (Медрол) рекомендуется принимать один раз в сутки при снижении внутривенной дозы до 20 мг в сутки. Курс лечения кортикостероидами не определен; некоторые специалисты предлагают прекратить лечение кортикостероидами, когда пациенты почти выздоровели.
Слайд 22Лечение искусственной поддержкой печени
Искусственная система поддержки печени (ALSS) может проводить плазмообмен, адсорбцию,

перфузию и фильтрацию медиаторов воспаления, таких как эндотоксины и вредные метаболические вещества малой или средней молекулярной массы. Он также может обеспечить сывороточный альбумин, факторы свертывания крови, сбалансированный объем жидкости, электролиты и кислотно-щелочное соотношение, а также проявлять антицитокиновые бури, шок, воспаление легких и др. При этом он также может помочь улучшить функции многих органов, включая печень и почки. Таким образом, он может повысить успех лечения и снизить смертность тяжелых пациентов.
Слайд 23Кислородная терапия
Гипоксемия может возникнуть из-за нарушения дыхательных функций COVID-19. Лечение кислородными добавками

может исправить гипоксемию, снимая вторичное повреждение органов, вызванное дыхательным расстройством и гипоксемией.
Слайд 24ЭКМО-поддержка для пациентов с COVID-19
COVID-19- это новое, высокоинфекционное заболевание, нацеленное в первую

очередь на легочные альвеолы, которое повреждает главным образом легкие тяжелобольных пациентов и приводит к тяжелой дыхательной недостаточности.
Для применения экстракорпоральной мембранной оксигенации (ЭКМО) в лечении COVID-19 медицинским работникам необходимо уделять пристальное внимание следующим аспектам: время и способ вмешательства, антикоагулянты и кровотечения, координация с искусственной вентиляцией легких, ЭКМО в сознании и ранняя реабилитационная подготовка, стратегия лечения осложнений.
Слайд 25«Человечеству объявлена беспрецедентная глобальная «война», и наш враг –это новое заболевание -

коронавирус. «Полем битвы» являются больницы, а наши «солдаты» -это медицинские работники.»
Профессор Тинбо Лян
























 Генетика и здоровье человека
Генетика и здоровье человека Санитарно-микробиологический контроль качества воздушной среды
Санитарно-микробиологический контроль качества воздушной среды Вольфатриоз
Вольфатриоз hernia6r
hernia6r Атеросклероз. Лекция № 6
Атеросклероз. Лекция № 6 Риногенные орбитальные осложнения
Риногенные орбитальные осложнения Клинический случай
Клинический случай Афазии
Афазии Алкоголометрия. Расчеты концентраций спирта по алкоголометрической таблице
Алкоголометрия. Расчеты концентраций спирта по алкоголометрической таблице Бронхиальная астма (БА)
Бронхиальная астма (БА) ГЕМОДИАЛИЗ: ОТВЕТЫ НА ВОПРОСЫ ДИАЛИЗНЫХ ПАЦИЕНТОВ Е.А.Стецюк, д.м.н.
ГЕМОДИАЛИЗ: ОТВЕТЫ НА ВОПРОСЫ ДИАЛИЗНЫХ ПАЦИЕНТОВ Е.А.Стецюк, д.м.н. Догляд за кінцівками великої рогатої худоби
Догляд за кінцівками великої рогатої худоби Туберкулез вчера и сегодня
Туберкулез вчера и сегодня Соціальна політика охорони здоров'я в Італії
Соціальна політика охорони здоров'я в Італії Психосоматика невроза
Психосоматика невроза Студенческий научный кружок кафедры детских болезней
Студенческий научный кружок кафедры детских болезней Холелитолитиктер. Өттас ауруын емдеу
Холелитолитиктер. Өттас ауруын емдеу Токсикомания. Виды токсикомании в зависимости от употребляемых веществ
Токсикомания. Виды токсикомании в зависимости от употребляемых веществ Центр комплексной реабилитации инвалидов Семь Ступеней
Центр комплексной реабилитации инвалидов Семь Ступеней Өз ойын
Өз ойын Неотложные состояния при ОНМК
Неотложные состояния при ОНМК Накопление βA и р-тау
Накопление βA и р-тау Ведение пациентов с сахарным диабетом 2 типа на амбулаторном этапе
Ведение пациентов с сахарным диабетом 2 типа на амбулаторном этапе Психопатологическая семиотика
Психопатологическая семиотика Физиология пирамидной и непирамидной систем. Физиология базальных ганглиев и ретикулярной формации. (Лекция 10)
Физиология пирамидной и непирамидной систем. Физиология базальных ганглиев и ретикулярной формации. (Лекция 10) Аборт. Прерывание беременности
Аборт. Прерывание беременности Фитотерапия хронического обструктивного бронхита
Фитотерапия хронического обструктивного бронхита 32 зуба
32 зуба