Слайд 2Гемостатические средства — лекарственные средства, способствующие остановке кровотечений. Все гемостатики, в зависимости

от механизма действия, подразделяются на три большие группы:
ингибиторы фибринолиза (антифибринолитики);
средства, усиливающие свертывание крови (коагулянты);
средства, понижающие сосудистую проницаемость.
Слайд 3Гемостатик должен: остановить кровотечение (тромбообразование) в течение 2 минут или менее; действовать

в широком диапазоне температур; не повреждать окружающие ткани, не вызывать болевых ощущений от сдавления или термического повреждения; быть готовым к использованию и легко наносится, в т.ч. в экстремальных условиях, для сложных ран, а также деградировать или легко удаляться из раны; иметь длительный срок хранения; быть бактерицидным; применимым при нарушениях функции свертывания крови, быть экономически эффективным
Слайд 4Аппликационные МГС представлены различными формами выпуска: гели, клеи, порошки, тканные и нетканые
материалы, гемостатические губки, растворы и пудры. Цель всех известных на сегодня МГС состоит в имитации специфических процессов естественного гемостаза, их ускорении или в быстром формировании фибринового сгустка с использованием иного механизма. При этом, гемостатик, не способный предотвратить диффузное кровотечение в течение двух минут, следует считать не эффективным
Слайд 5По механизму активности местные гемостатики принято делить на:
• сосудосуживающие и проагрегационные;
• плазменные

факторы свертывания;
• ингибиторы фибринолиза;
• стимуляторы агрегации и адгезии;
• способствующие денатурациибелков;
• комбинированные
Слайд 6МГС, внесенные в Регистр лекарственных средств в России на 2018 г

Слайд 7Препараты колагена
Коллаген ускоряет естественный путь коагуляции и запускает процесс свертывания крови
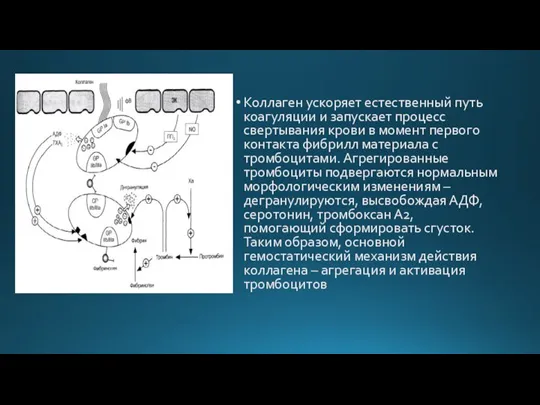
в момент первого контакта фибрилл материала с тромбоцитами. Агрегированные тромбоциты подвергаются нормальным морфологическим изменениям – дегранулируются, высвобождая АДФ, серотонин, тромбоксан А2, помогающий сформировать сгусток. Таким образом, основной гемостатический механизм действия коллагена – агрегация и активация тромбоцитов
Слайд 8Большинство современных МГС на основе коллагена содержат вещества, влияющие на отдельные стадии

свертывания крови : тромбоциты («Тромбокол»), тромбин, фибриноген («ТахоКомб»), эпсилон-аминокапроновую кислоту, гидроксиаппатит и др. При взаимодействии коллагена с растворами, содержащими кальций, катионы прочно связываются, входя внутрь тройной спирали. В результате, ее конформация изменяется таким образом, что молекулы воды перестают удерживаться данным участком тройной спирали, это приводит к локальной потере воды и «сшивке» структуры – образуется болеежесткий губчатый материал. Органические катионы – алкалоиды, так же как и ионы тяжелых металлов стереохимически связываются коллагеном, а мало- и неионизированные вещества не образуют прочных связей. Это свойство позволяет регулировать активность лекарственных средств в составе коллаген-содержащих форм.
Слайд 10Желатин – продукт частичной деструкции коллагена. Так же как коллаген, он обеспечивает
физическую матрицу для инициирования свертывания крови. Желатин эффективно контролирует кровотечения малых сосудов, рекомендуется к использованию в качестве гемостатической пробки, обернутой в окисленную целлюлозу. pH желатиновых пенопластов близок к 7 и поэтому они могут использоваться в сочетании с тромбином или другими веществами для усиления гемостатического действия. Гранулы желатина позволяют сконцентрированному тромбину быстро реагировать с фибриногеном пациента и формировать механически устойчивый фибриновый сгусток. По мере того, как кровь просачивается через желатиновый матрикс, гранулы гемостатика разбухают примерно на 20% за 10 минут, ограничивая течение крови и обеспечивая мягкую тампонаду, конформно подходящую по форме раны
Слайд 11Эффективность данных МГС достигается благодаря сорбционным (поглощение жидкости и концентрирование факторов тромбообразования)

и адгезионным (инициирование свертывания) свойствам
Главный недостаток желатина в его бактериоемкости, то есть, он может стать очагом инфекции.
Слайд 12Полисахариды Высокомолекулярные углеводы представляют собой длинные линейные или разветвлённые цепочки моносахаридных остатков,

соединённых гликозидной связью. В качестве гемостатиков применяются целлюлоза, хитин (в природе выполняют структурные функции), а также крахмал (резервные функции) и др.
Преимуществом целлюлозных волокнистых материалов является наличие различных форм: тканей (марли), нетканых и трикотажных полотен, ваты и т.п. Марля обладает высокой адгезией к ране, в то же время нельзя отрицать высокие гигиенические, сорбционные и физикомеханические свойства повязок на основе целлюлозных волокон. Тканые и нетканые материалы являются наиболее распространённым носителем гемостатических средств, относящихся к группам: плазменные факторы свертывания, сосудосуживающие и проагрегационные, ингибиторы фибринолиза и т.д.
Слайд 13После химической модификации целлюлоза приобретает собственную физиологическую активность, что позволяет ее использовать

в качестве лечебной формы без присоединения лекарственных веществ. Так, карбоксиметилцеллюлоза, содержащая функциональные группы кислотного типа, способна связывать в раневой среде пептиды, в частности эластазу, и таким образом подавлять ее активность. Хорошо известно применение монокарбоксилцеллюлозы в качестве кровоостанавливающей марли. Высокая биоинертность карбоксиметилцеллюлозы позволяет использовать ее в качестве барьерного средства, например, в форме гидрогеля («Мезогель») для профилактики спаечного процесса брюшной полости. Na-карбоксиметилцеллюлоза обладает выраженным стимулирующим действием на репаративные процессы, ускоряет образование и созревание грануляционной ткани, активно влияет на процессы фибриллогенеза
Слайд 14МГС из окисленной регенерированной целлюлозы «Surgicel Fibrillar» представляет собой нетканый 7-слойный материал,
он не крошится при нарезании, обладает хорошей адгезией к ткани, волокнистая структура позволяет легко моделировать размер и форму фрагмента накладывается целиком, слоями, пучками и турундами и поэтому удобен для применения в труднодоступных местах. Среднее время остановки кровотечения 2–4 минуты
Слайд 15Алюмосиликатные минералы – цеолиты (каолин). Структурная пористость неоранического полимера AlSiO4 определяет применение

алюмосиликатов в качестве адсорбентов. Открытая каркаснополостная структура имеет отрицательный заряд, что позволяет им задерживать большое количество катионов, например кальция – кофактора в коагуляционном каскаде. На основе синтетического цеолита разработано несколько эффективных МГС. Препараты не растворимы, но биосовместимы. В армии США для остановки наружных массивных кровотечений был принят «QuikClot». Механизм гемостаза «QuikClot» включает адсорбирование порошком воды из крови, концентрирование факторов свертывания крови, активацию тромбоцитов и последующее продвижение ступеней в коагуляционном каскаде.














 Поперечно-полосатая мышечная ткань языка
Поперечно-полосатая мышечная ткань языка Сахарный диабет у детей
Сахарный диабет у детей Шалкова проба
Шалкова проба Аритмии сердца
Аритмии сердца Хирургиялық инфекция
Хирургиялық инфекция Оценка комплексного состояния здоровья ребенка, определение группы здоровья по форме 112/у
Оценка комплексного состояния здоровья ребенка, определение группы здоровья по форме 112/у Уақытша сауыттар
Уақытша сауыттар удаление зуба
удаление зуба Серодиагностика брюшного тифа
Серодиагностика брюшного тифа Препараты бария. Противопоказания и показания
Препараты бария. Противопоказания и показания Акушерство и его особенности
Акушерство и его особенности Иммунограмма в практике инфекциониста
Иммунограмма в практике инфекциониста Норма и патология органов забрюшинного пространства
Норма и патология органов забрюшинного пространства Метоика кормения тяжелобольного пациента
Метоика кормения тяжелобольного пациента Органическое поражение головного мозга
Органическое поражение головного мозга Чума. Определение
Чума. Определение Профессия врач
Профессия врач Грыжа пищеводного отверстия диафрагмы
Грыжа пищеводного отверстия диафрагмы История развития концепции реабилитации. Общие вопросы реабилитации. Основные методы реабилитации. Лекция №1
История развития концепции реабилитации. Общие вопросы реабилитации. Основные методы реабилитации. Лекция №1 Проблемы с кожей? Проверьте кишечник
Проблемы с кожей? Проверьте кишечник Аккредитация. Тесты 3
Аккредитация. Тесты 3 Основные проблемы и ошибки в оказании медицинской помощи пациентам реанимационных отделений с COVID-19 инфекцией
Основные проблемы и ошибки в оказании медицинской помощи пациентам реанимационных отделений с COVID-19 инфекцией Контроль качества на аналитическом этапе. Понятия, принципы организации. Алгоритмы оценки результатов
Контроль качества на аналитическом этапе. Понятия, принципы организации. Алгоритмы оценки результатов Основные типы кожи. Чистка лица
Основные типы кожи. Чистка лица Индивидуальная система привычек в повседневной жизни. Режим дня
Индивидуальная система привычек в повседневной жизни. Режим дня Заявка на иммунобиологические лекарственные препараты
Заявка на иммунобиологические лекарственные препараты Программа по восстановлению утраченных функций после мозговых катастроф
Программа по восстановлению утраченных функций после мозговых катастроф ВИЧ-инфекция и особенности В-клеточного иммунитета
ВИЧ-инфекция и особенности В-клеточного иммунитета