Слайд 2Качество дезинфекции зависит:
1. от правильности выбора дезинфицирующего средства для данной инфекции:

2. от концентрации примененного дезинфектанта;
3. от температуры дезинфицирующего раствора;
4. от количества раствора, израсходованного на 1 кв/м.
Слайд 3Кроме того, качество произведенной дезинфекции зависит от качества механической очистки объекта (помещения).

Для того чтобы убедиться - правильно-ли выбран дезинфектант, его концентрация и пр., существует бактериологическая методика контроля качества дезинфекции.
Слайд 4Прежде чем остановиться на методике, необходимо выяснить, надо ли при дезинфекции убивать

всех патогенных микроорганизмов или достаточно уничтожить только большую их часть.
Слайд 5Установлено, что не все и не всегда микробы погибают или теряют свою

вирулентность даже при взаимодействии с высокоэффективными дезинфицирующими веществами. Доказано, что часто вирулентность, оставшихся в живых микробов сохраняется, но количество их резко уменьшается.
Слайд 6Во многих случаях животное может преодолеть воздействие оставшихся после дезинфекции микроорганизмов, но

возможны случаи и заражения.
Все в данном случае зависит от числа оставшихся возбудителей, их вирулентности, состояния самого животного и условий его содержания. Это обязывает тщательно проводить дезинфекцию.
Слайд 7В последнее время принято считать, что при дезинфекции надо полностью уничтожать патогенных

возбудителей инфекции.
В 1954 году Минздрав СССР составил "Инструкцию по бактериологическому контролю качества дезинфекционной обработки очагов кишечных инфекций".
Слайд 8Критерием для оценки дезинфекции в этих очагах служит кишечная палочка (Eschericha coli),

как постоянно присутствующий микроб.
Поляков А.А., Тереньтьева К.И. в 1952-1955 годах провели исследования и разработали метод контроля качества дезинфекции животноводческих объектов.
Полученные данные показали, что кишечная палочка может быть использована для контроля качества дезинфекции.
Слайд 9Этот вид микроба наиболее распространен в животноводческих помещениях; как правило, кишечная палочка

выделяется до дезинфекции (после очистки и промывки) в 100% случаев из проб с пола и в подавляющем большинстве случаев из проб со стен.
После правильно проведенной дезинфекции ни в одном случае не было обнаружено роста кишечной палочки.
Слайд 10Кишечная палочка по своей устойчивости к химическим дезинфицирующим средствам не уступает многим

патогенным неспорообразующим и некокковым микроорганизмам или превосходит их.
Установлено, что если при дезинфекции будет уничтожена кишечная палочка, будут уничтожены и возбудители таких болезней, как бруцеллез, сальмонеллез, колибактериоз, рожа.
Исключением в этом отношении могут быть возбудители туберкулеза, мыта и спорообразующая микрофлора, устойчивость которой гораздо выше.
Слайд 11Е.С. Цой в 1969 году установил одинаковую устойчивость к химическим дезосредствам разных

патогенных возбудителей туберкулеза и стафилококков.
Стафилококки, как и кишечная палочка, присутствуют в 100% проб, взятых в помещениях для животных.
Это дало возможность использовать данные микроорганизмы в качестве контрольно-санитарных при бактериологическом контроле качества произведенной дезинфекции при туберкулезе.
Слайд 12Отбор проб для определения качества дезинфекции проводит ветеринарный врач хозяйства.
Пробы берут

через 2-3 часа после проведения профилактической дезинфекции или по истечению определенной экспозиции при текущей дезинфекции.
Пробы берут с пола, с двух стен в стойле, в месте расположения задних конечностей животного, из углов и кормушек.
Всего - с 10-ти различных участков.
Слайд 13Для этого намечают квадраты величиной 10 х 10 см и протирают их

в течение 1-2 минут стерильным ватным тампоном, пропитанным и хорошо отжатым в колбе (пробирке) с нейтрализующим раствором.
Тампон, каждый в отдельности, помещают в стерильный нейтрализующий раствор или стерильную воду (20 мл) и в таком виде доставляют в лабораторию.
Слайд 15Для нейтрализации:
хлорной извести используют 0,1% раствор тиосульфата натрия;
для щелочных растворов

- 0,01% раствор уксусной кислоты;
для формалина - 1-2% раствор нашатырного спирта.
Концентрация нейтрализующих растворов должна быть в 10 раз меньше концентрации растворов, применяющихся для дезинфекции.
Слайд 16При применении креолина, лизола, серно-карболовой смеси и других дезинфектантов, при которых нет

нейтрализаторов, тампоны промывают двукратно по 5-10 минут в стерильной воде.
Пробы доставляют в лабораторию не позднее чем через 2 часа после их отбора.
Слайд 17К пробам пишут сопроводительную, в которой указывают:
хозяйство;
2) тип постройки;
3)

дату и время дезинфекции;
4) дату и время отбора проб;
5) вид дезинфекции (профилактическая, текущая, заключительная);
6) качество механической очистки.
В лаборатории пробы исследуют в тот же день.
Слайд 18Тампоны отмывают во флаконе с 20 мл стерильной нейтрализующей жидкости или воды,
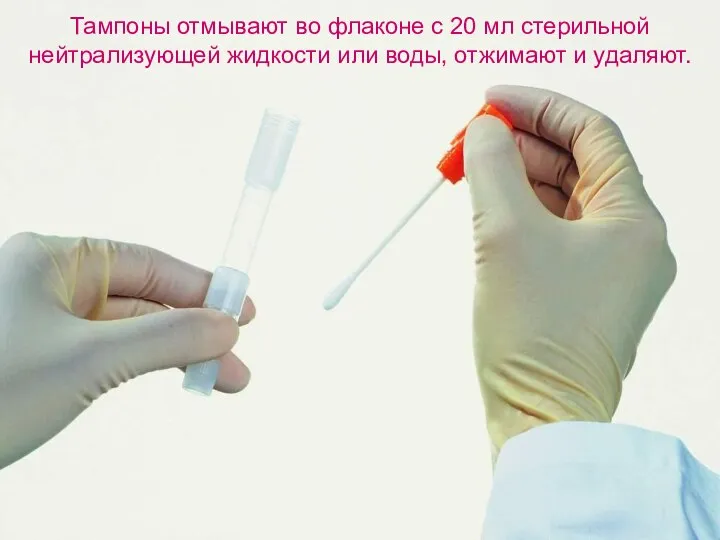
отжимают и удаляют.
Слайд 19Жидкость центрифугируют 20-30 минут при 3000-3500 об/мин.

Слайд 20В осадок добавляют равное количество стерильной воды, содержимое смешивают и вновь центрифугируют

20 минут.
Жидкость сливают, а с осадка делают посев на элективные питательные среды.
Слайд 21Для индикации кишечной палочки высев делают на модифицированную среду Хейфеца (индикаторами, в

которой служат розоловая кислота и метиленовая синька), по 0,5 мл центрифугата на 5 мл среды.
Культивируют при температуре 43°С в течение 12-18 часов.
Кишечная палочка изменяет цвет среды из малинового в зеленый или салатовый, среда становится мутной с пузырьками газа.
Слайд 22Высев на модифицированную среду Хейфеца.

Слайд 23Для индикации стафилококков 0,5 мл центрифугата высевают в 5 мл 50%-ного сахарозного

мясопептонного бульона (МПБ). Инкубируют 24 часа при температуре 37ºС, затем пересевают на 8,5%-ный солевой мясопептонный бульон (МПБ) и инкубируют 24 часа при 37°С. Полученную культуру исследуют под микроскопом.
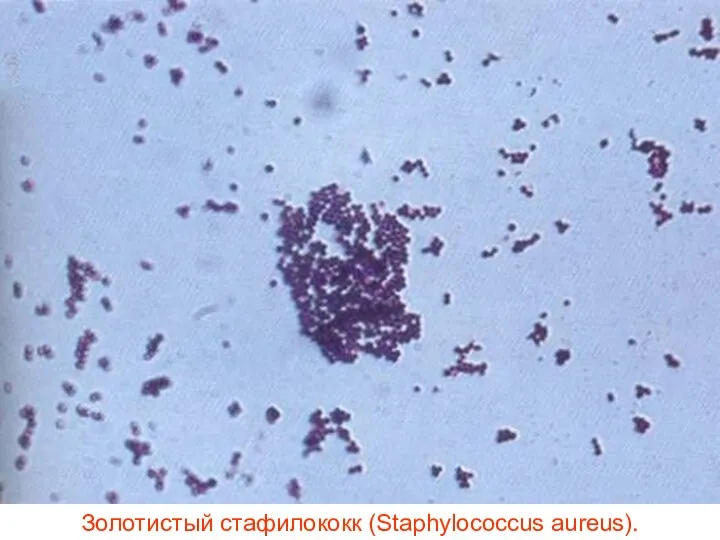
Слайд 24Золотистый стафилококк (Staphylococcus aureus).
Слайд 25Учет результатов:
Удовлетворительный результат означает, что при:
1) профилактической дезинфекции ни в

одной из проб не выделен контрольно-санитарный микроорганизм, или он установлен не более чем в 20% проб;
2) текущей дезинфекции - отрицательный результат не менее чем в 90% проб;
3) заключительной дезинфекции - во всех пробах отрицательный результат.
Контроль качества заключительной дезинфекции при туберкулезе проводят параллельно двумя методами: по выделению стафилококка и микобактерий.
Слайд 26Контроль качества дезинфекции по микобактериям.
Из кислотоупорных сапрофитов рода микобактерий готовят нефиксированные

мазки (тестобъекты) на предметных стеклах, которые раскладывают в различных местах помещения до дезинфекции. После окончания дезинфекции и срока экспозиции тестобъекты собирают обрабатывают в нейтрализующем растворе и помещают в микрокультиватор Н.М. Колычева, который заполняют жидкой средой Сотона и культивируют при 37ºС в течение 48 часов.
Слайд 27По окончании этого срока тестобъекты извлекают, промывают от среды, фиксируют над пламенем

горелки и окрашивают методом Циль Нильсона.
Если в процессе дезинфекции тестмикробы не погибли на стекле образуются микроколонии, которые можно обнаружить под микроскопом.
Слайд 28Изучение тестобъекта под микроскопом.



























 Антисептики, дезинфицирующие средства, антибиотики. Лекция 22
Антисептики, дезинфицирующие средства, антибиотики. Лекция 22 ГУЗ Липецкая ГБ № 4 Липецк-Мед
ГУЗ Липецкая ГБ № 4 Липецк-Мед Общие понятия о здоровье как основной ценности человека
Общие понятия о здоровье как основной ценности человека Классификация переломов
Классификация переломов Организация акушерско-гинекологической помощи в Республике Беларусь
Организация акушерско-гинекологической помощи в Республике Беларусь Ми – жұлын сұйықтығының құрамы мен диагностикалық маңызы
Ми – жұлын сұйықтығының құрамы мен диагностикалық маңызы Психопатологическая семиотика
Психопатологическая семиотика Гигиена зрения ребенка
Гигиена зрения ребенка Первичная артериальная гипертензия
Первичная артериальная гипертензия Гигиена ухода за животными. Санитарно-гигиеническое значение ухода за кожей
Гигиена ухода за животными. Санитарно-гигиеническое значение ухода за кожей Особенности лечебной тактики при экстрагенитальном эндометриозе
Особенности лечебной тактики при экстрагенитальном эндометриозе Острые респираторные заболевания и грипп
Острые респираторные заболевания и грипп Основы инфектологии
Основы инфектологии Противомикробные средства
Противомикробные средства Бронхиальды астма терапиясының фармакоэкономикасы
Бронхиальды астма терапиясының фармакоэкономикасы Нарушения речи, связанные с затруднениями в реализации моторной программы
Нарушения речи, связанные с затруднениями в реализации моторной программы Қарттар үйі
Қарттар үйі Сохранение здоровья ребенка до 1 года
Сохранение здоровья ребенка до 1 года Ресинхронизирующая терапия (устройства)
Ресинхронизирующая терапия (устройства) Тератомалар
Тератомалар Причины отклонений в развитии
Причины отклонений в развитии Гемопоэз и группы крови
Гемопоэз и группы крови Физиологические барьеры организма и их роль во врожденном иммунитете
Физиологические барьеры организма и их роль во врожденном иммунитете Aortic diseases
Aortic diseases Хронический насморк
Хронический насморк Здоровое питание
Здоровое питание Деменция - приобретённое слабоумие
Деменция - приобретённое слабоумие Нарушения сознания
Нарушения сознания