Слайд 2Тяжелый комбинированный иммунодефецит (ТКИД)
Наследственный дефект гена γ-цепи рецептора IL-2. Общая субъединица для

рецепторов IL-4, IL-7, IL-9, IL-15, IL-21.
Дефицит JAK3 киназы. Проводит внутриклеточный активационный сигнал от γ-цепи .
Дефицит α-субъединицы рецептора IL-7.
Нарушение функционирование только IL-7, стимулирующего Снижение количества Т-лф, но нормальные В-лф и NK-клетоксозревание предшественников лимфоцитов.
Слайд 3Нарушение в системе IL-12,IL-23,IFN-γ и их рецепторов
АПК представляет АГ + синтезирует цитокины
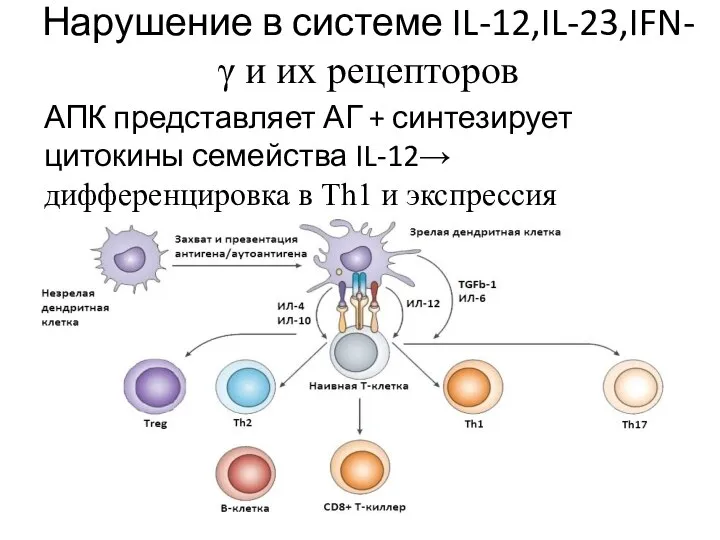
семейства IL-12→ дифференцировка в Th1 и экспрессия цитокинов(IFN-γ)
Слайд 5Обнаружены 5 мутаций, нарушающие данный каскад:
1) Ген субъединицы р40. Одна из двух субъединиц

гетеромерных цитокинов IL-12, IL-23
2) β1-цепи рецептора IL-12/IL-23R
3,4) Гены субъединиц 1 и 2 рецептора IFN-γ. Подразделяется на полные дефициты рецепторов, частично рецессивные и частично доминантные.
Ген внутриклеточной сигнальной молекулы STAT1
Клиника: Восприимчивость к инфекциям, вызываемыми микобактериями и сальмонеллами
Слайд 6Функциональный полиморфизм генов цитокинов как вариант развития наследственных нарушения цитокиновой регуляции
Мутации в

генах цитокинов достаточно редки у человека, что говорит об их значительной роли.
Однако обнаружены различные SNP, вызывающие количественные изменения функционирования соответствующих генов
Часть выявленных аллельных генов ассоциированы с увеличением/снижением биологической активности кодируемых ими белков
Слайд 7Ген TNF -308(G→A)
Однонуклеотидная замена располагается в промоторной области
Наличие аллеля (-308А) увеличивает эффиктивность

транскрипции гена, а следовательно и продукцию TNF в 2-5 раз, по сравнению с (-308G )
У африканцев аллель (-308А) ассоциирован с наиболее тяжелым протекании малярии (церебральная форма, последующие нарушения ЦНС). Более выражена системная воспалительная реакция.
У африканцев частота носительства данного аллеля составляет 5%, а у европейцев 30%
Следовательно определение SNP поможет скорректировать прогноз и подобрать адекватную терапию
Слайд 9Изменение синтеза цитокинов при сепсисе
Сепсис – это патологический процесс, в основе которого
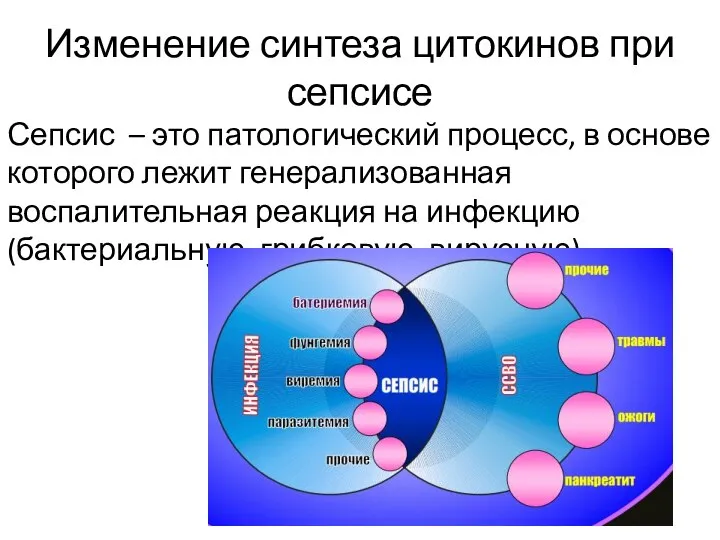
лежит генерализованная воспалительная реакция на инфекцию (бактериальную, грибковую, вирусную).
Слайд 10Лабораторные данные: Чем выше уровни цитокинов (про- и противовоспалительных) при поступление в

отделение интенсивной терапии больных с диагнозом «сепсис», тем выше уровень смертности.
В начале развития сепсиса происходит активация различных типов лейкоцитов и других, синтезирующих цитокины, клеток, а также индукция или увеличение уровня экспрессии генов цитокинов
В высоких концентрациях провоспалительные цитокины способны вызывать нейроэндокринные изменения, нарушения терморегуляции, отеки, коллапс, полиорганная недостаточность, смерть
Наибольшую корреляцию с течением сепсиса имеют: TNF, IL-6, IL-1, IL-10
Слайд 11Продукция цитокинов изолированными лейкоцитами больного сепсисом снижена по сравнению с уровнем продукции

лейкоцитов здоровых доноров.
Вероятно, связано с общим явлением анергии после интенсивного синтеза цитокинов (так происходит после травм, массовых ожогах)
Противовосполительные цитокины (IL-10,TGFβ) и растворимые рецепторы TNF и IL-6 тоже синтезируются в повышенных количествах при сепсисе. Наиболее высокие уровни IL-10 встречаются при наименее благоприятном исходе.
Эти данные привели к понятию «синдром компенсированного антивосполительного ответа». СКАО развивается вслед за ССВР, для его ограничения. Но иногда это приводит к иммуносупрессии
Слайд 12Роль цитокинов в развитии аутоиммуной паталогии
Хроническая несбалансированность активации Т-хелперных клонов (Th1, Th2,

Th17) приводит к развитию иммунопаталогических состояний
Главным образом развиваются при избыточной активации воспалительной реакции и клеточного иммунитета
При ряде аутоиммуных процессов в области поражения доминируют цитокины Th1 и симптомы аутоиммуного воспаления могут быть подавлены введением цитокинов Th2
В других аутоиммунных растройствах гиперактивируются как Th1 так и Th2
Слайд 13Ревматоидный артрит
РА – аутоиммунное заболевание, поражающее главным образом синовиальную оболочку, хрящевую и

костную ткань суставов
Цитокины – посредники между активацией иммуной системы, развитии хронического воспалительного процесса и деструкции сустава
Слайд 14В синовиальной оболочке обнаружены плазмацитоидные и миелоидные ДК, синовиальные макрофаги, выделяющие цитокины,
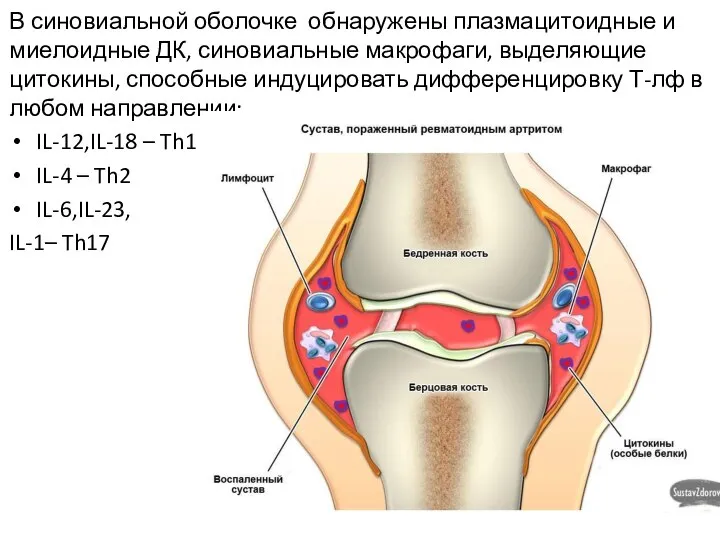
способные индуцировать дифференцировку Т-лф в любом направлении:
IL-12,IL-18 – Th1
IL-4 – Th2
IL-6,IL-23,
IL-1– Th17
Слайд 15Повышенная концентрация TNF и IL-1 вызывает активацию синовиальных фибробластов, эндотелиальных клеток и

привлеченных лейкоцитов, синтез медиаторов воспаления и ремоделирования ткани с развитием патологических осложнений
Все усугубляется тем фактом, что снижается продукция противовосполительных медиаторов и регуляторных цитокинов. Снижаетя концентрация raIL, IL-10, IL-4, IL-2. Но не снижается концентрация растворимых рецепторов для TNF и IL-1
Слайд 16Уровни провосполительных цитокинов в крови могут коррелировать с клиническими проявлениями заболевания и

могут быть диагностическими маркерами
Если они очень высоки, то будет системное проявление биологического действия: IL-6 стимулирует синтез острофазных белков в печени, TNF вызывает кахексию, остеопороз трубчатых костей
Слайд 17Цитокины и аллергия
Аллергические состояния – генетически детерминированная группа заболеваний, характеризующихся повышенной способностью

В-лф синтезировать IgE против аллергенов.
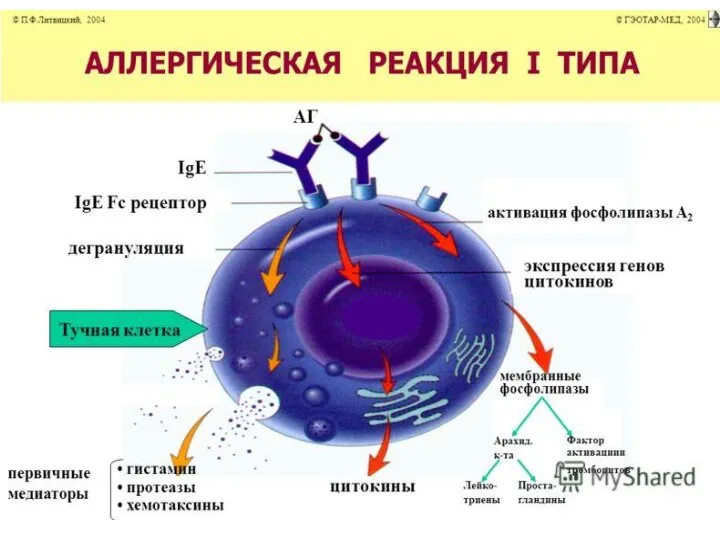
IgE взаимодействует с высокоафинным мембранным рецептором базофилоф и тучных клеток FcεR1→ выброс вазоактивных аминов, хемокинов, провосполительных цитокинов
Развитие ИО с преимущественным синтезом IgE регулируется Th2 через IL-4, IL-5, IL-13
Слайд 19Первый источник цитокинов – тучные клетки (IL-4, IL-13, TNF)
При дегрануляции попадают в

межклеточное пространство в первые минуты после опсонизации
Усиливается продукция хемокинов, молекул адгезии
Привлечение в ткани эозинофилов, базофилов, Т-лф
Дальнейший источник – базофилы, тучные клетки, др. лейкоциты, активация которых сопровождается секрецией IL-3, IL-4, IL-5, IL-6, TNF, GM-CSF
По мере развития заболевания аллерген-специфические Т-лф все более накапливаются в очаге аллергического воспаления















 Метод предупреждения развитие фокомелии, опираясь на теорию морфогенеза Тьюринга
Метод предупреждения развитие фокомелии, опираясь на теорию морфогенеза Тьюринга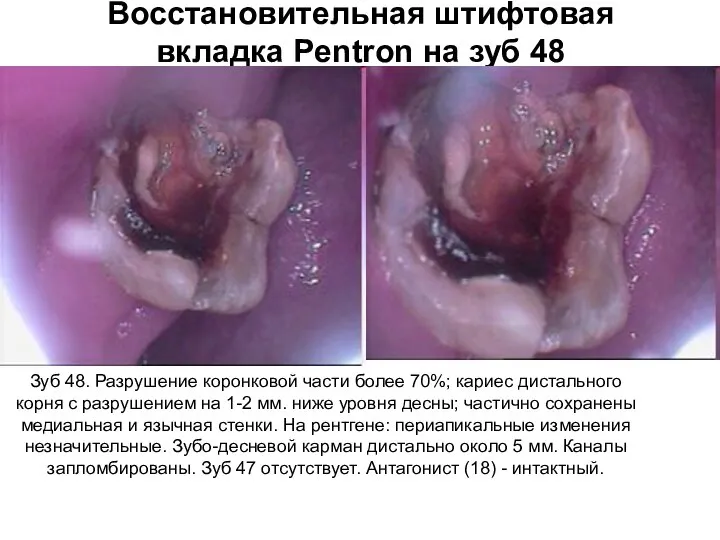 Восстановительная штифтовая вкладка Pentron на зуб 48
Восстановительная штифтовая вкладка Pentron на зуб 48 Интубация трахеи
Интубация трахеи Госпитальная эпидемиология
Госпитальная эпидемиология Методики исследования и травматические повреждения костно–суставного аппарата
Методики исследования и травматические повреждения костно–суставного аппарата Сыртқы белгілері бойынша адамды сәйкестендіру әдістемесін жетілдіру
Сыртқы белгілері бойынша адамды сәйкестендіру әдістемесін жетілдіру Наномедицина
Наномедицина Удаление глазных яблок среди взрослого населения Луганской Народной Республики за 2019 год
Удаление глазных яблок среди взрослого населения Луганской Народной Республики за 2019 год Беременность и роды у женщины при рубце на матке
Беременность и роды у женщины при рубце на матке О клинико-лабораторном обследовании детей, выезжающих в летние оздоровительные учреждения
О клинико-лабораторном обследовании детей, выезжающих в летние оздоровительные учреждения Профилактика ожирения среди взрослого населения
Профилактика ожирения среди взрослого населения Гастроэзофагеальная рефлюксная болезнь
Гастроэзофагеальная рефлюксная болезнь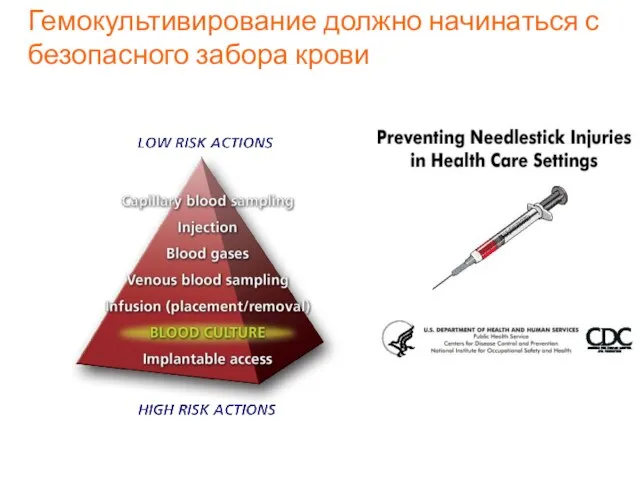 Гемокультивирование. Правила забора крови
Гемокультивирование. Правила забора крови Профилактика туберкулеза в современном обществе
Профилактика туберкулеза в современном обществе Жасалған операциялар тізімі
Жасалған операциялар тізімі Реставрация зубов после эндодонтического лечения
Реставрация зубов после эндодонтического лечения Дифтерия
Дифтерия Хвороба, яка супроводжується тяжким ураженням центральної нервової системи
Хвороба, яка супроводжується тяжким ураженням центральної нервової системи Возможности лечения БАС на современном этапе. Прогноз
Возможности лечения БАС на современном этапе. Прогноз Лабораторные, инструментальные, функциональные методы исследования органов дыхания
Лабораторные, инструментальные, функциональные методы исследования органов дыхания Бордетеллалар. Көкжөтел және паракөкжөтел
Бордетеллалар. Көкжөтел және паракөкжөтел Gender bound/sex bound inheritance
Gender bound/sex bound inheritance День здоровья. Победим диабет!
День здоровья. Победим диабет! Rofilaxia bolilor genetice
Rofilaxia bolilor genetice Математическое и программное обеспечение долгосрочного прогнозирования неблагоприятных сосудистых событий
Математическое и программное обеспечение долгосрочного прогнозирования неблагоприятных сосудистых событий Экзаменационный билет патан, препараты (пример) 5
Экзаменационный билет патан, препараты (пример) 5 Безболевая ишемия миокарда: патофизиология, диагностика, прогноз
Безболевая ишемия миокарда: патофизиология, диагностика, прогноз Первая помощь при преломах
Первая помощь при преломах