Содержание
- 2. Лекция 1. час 1. Введение. Содержание курса. 1.1. Цель и задачи курса. Определение понятия "физические свойства".
- 3. Цель и задачи курса Цель курса: Научить связывать физические свойства материалов с их структурой и фазовым
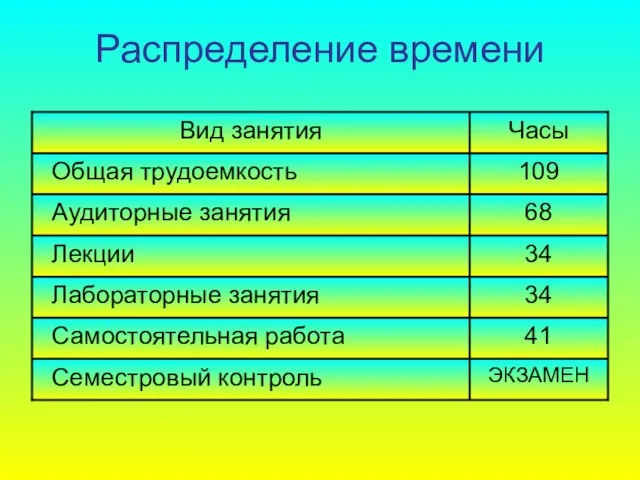
- 4. Распределение времени
- 5. РАСПРЕДЕЛЕНИЕ УЧЕБНОГО ВРЕМЕНИ Лекции – 34 ч 6 Лабораторных работ – 34 ч Самостоятельная работа –
- 6. Программа курса Тема 1. Введение (1 час) Тема 2. Тепловые свойства (теплоемкость и энтальпия), термическое расширение,
- 7. Литература Лившиц Б.Г., Крапошин В.С., Линецкий Я.Л. Физические свойства металлов и сплавов. М.: Металлургия, 1980, 318
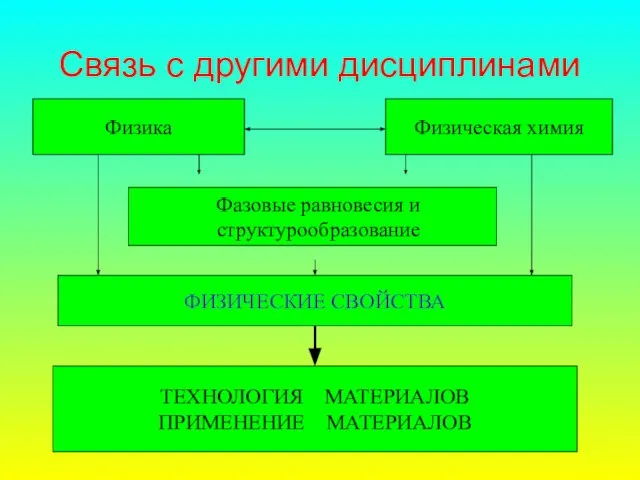
- 8. Связь с другими дисциплинами Физика Физическая химия Фазовые равновесия и структурообразование ФИЗИЧЕСКИЕ СВОЙСТВА ТЕХНОЛОГИЯ МАТЕРИАЛОВ ПРИМЕНЕНИЕ
- 9. Классификация физических свойств по влиянию микроструктуры и дефектов кристаллической решетки: 1. структурно-чувствительные свойства (ρ, λ, μ,
- 10. Влияние обработки на свойства стали У8 Отжиг Сфероидизирующий Закалка отжиг Bs=2,1 Тл Вs=2,1 Тл Вs=1,8 Тл
- 11. Классификация по виду физического эффекта Физический эффект, «порождающий» физическое свойство, может быть охарактеризован путем описания воздействия
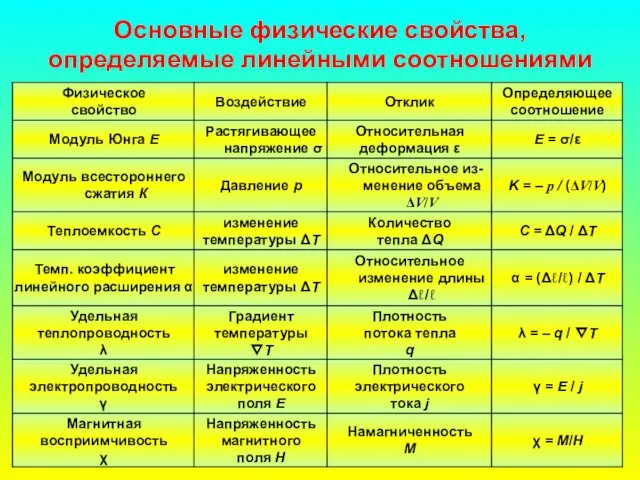
- 12. Основные физические свойства, определяемые линейными соотношениями
- 13. Комментарии Различие между воздействием и откликом иногда довольно условно. Под воздействием понимают физическую величину, значение которой
- 14. Некоторые особенности физических свойств наноматериалов. В наноструктурных материалах часто изменяются фундаментальные характеристики, такие как Точка Кюри,
- 15. Лекция 2. час 2. Тема 1. Тепловые свойства. 1. Общие понятия и определения (энтальпия, виды теплоемкости
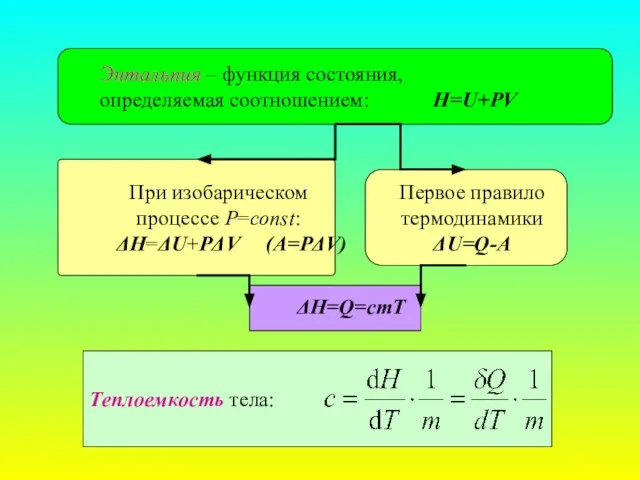
- 16. Энтальпия – функция состояния, определяемая соотношением: H=U+PV При изобарическом процессе P=const: ΔH=ΔU+PΔV (A=PΔV) Первое правило термодинамики
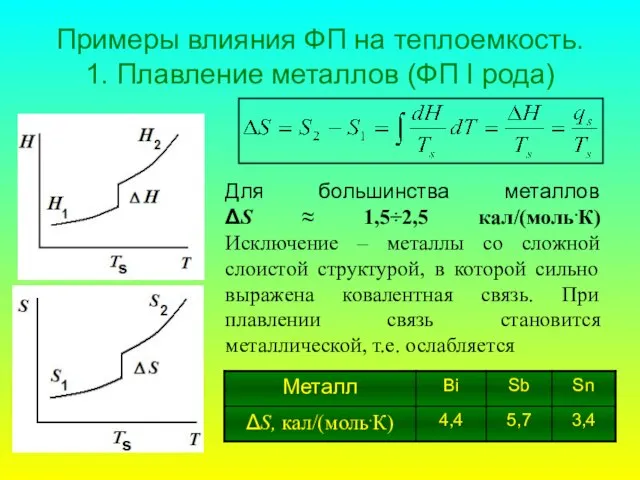
- 17. Виды теплоемкости Теплоемкость тела: C = δQ/dT [Дж/К]. Удельная теплоемкость: Суд = С/m [Дж/кг·К]. Молярная теплоемкость:
- 18. Теплоемкость для разных условий передачи тепла Теплоемкость при постоянном объеме: CV = (∂U/∂T)V=const. Теплоемкость при постоянном
- 19. Различие теплоемкостей Объемный коэффициент термического расширения Коэффициент всестороннего сжатия (сжимаемость)
- 20. Формула Нернста-Линдемана Причем a≠f(T) Для металлов ΔС очень мала: СP ≈ CV . (1+10-4T), НО Для
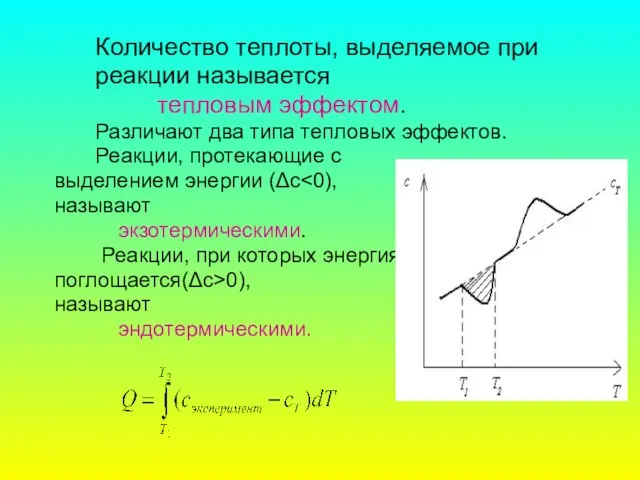
- 21. Количество теплоты, выделяемое при реакции называется тепловым эффектом. Различают два типа тепловых эффектов. Реакции, протекающие с
- 22. Составляющие теплоемкости Cp = Cрешетки + Сэл = = Сидеальной решетки + Сдефект + Сэл =
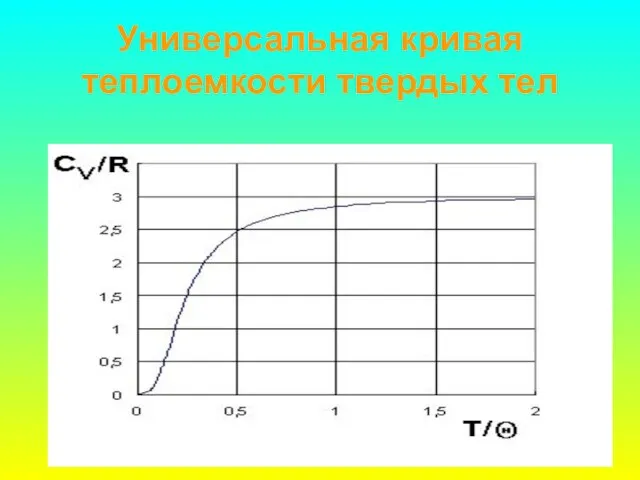
- 23. Универсальная кривая теплоемкости твердых тел
- 24. Решеточная теплоемкость 1 классическое приближение Средняя энергия классического осциллятора на 1 степень свободы: на 3 степени
- 25. Решеточная теплоемкость 2 классическое приближение Всего 6 степеней свободы – 3 - поступательное движение 3 -
- 26. Лекция 2. 2. Теории теплоемкости Эйнштейна и Дебая. Дебаевская температура как характеристика сил связи между атомами
- 27. Теория теплоемкости Эйнштейна Предположения: 1. Твердое тело – совокупность атомов, которые колеблются независимо друг от друга,
- 28. Достоинства и недостатки теории Эйнштейна Достоинства: Качественно верно описывает зависимость Cv(Т) и ее связь с жесткостью
- 29. Теория теплоемкости Дебая Основные положения: 1. При нагреве возникают связанные (коллективные) колебания атомов. Распространение колебаний в
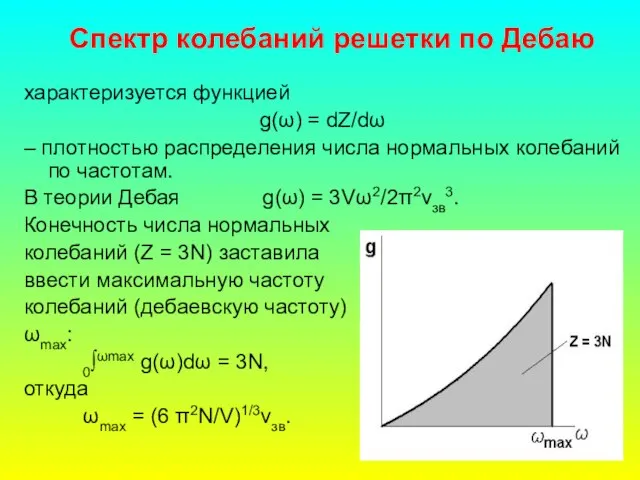
- 30. Спектр колебаний решетки по Дебаю характеризуется функцией g(ω) = dZ/dω – плотностью распределения числа нормальных колебаний
- 31. Расчет теплоемкости по Дебаю CV = ∂U/∂T = ∂/∂T 0∫ωmax g(ω) dω, CV = 9R (T/θ)3
- 32. Температура Дебая θ = ħωmax/k = (6 π2/Vат)1/3 vзв. При Т > θ возбуждены все частоты
- 33. Фононы Любую волну можно представить, как квазичастицу. Фонон – квазичастица, описывающая нормальные колебания кристаллической решетки. Энергия
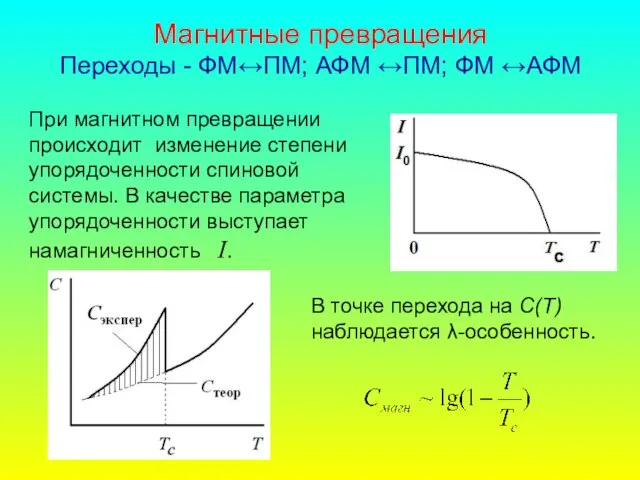
- 34. Число фононов Число фононов n = 1/[exp(1/x)-1], где x = ħω/kT. Общее число фононов Nфон =
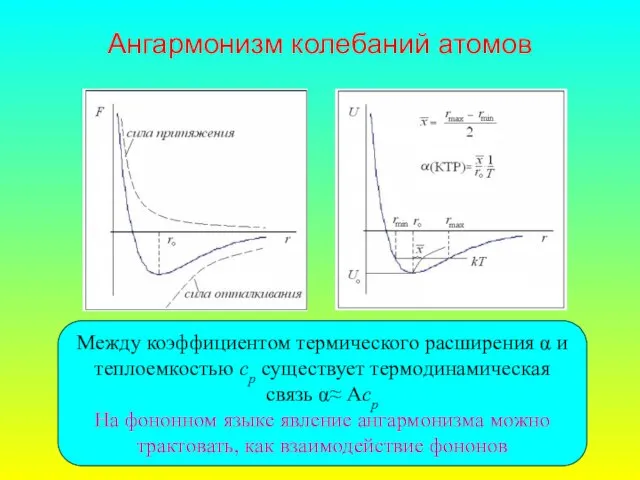
- 35. Ангармонизм колебаний атомов Между коэффициентом термического расширения α и теплоемкостью ср существует термодинамическая связь α≈ Аср
- 36. Влияние ангармонизма колебаний атомов на теплоемкость Решеточная теплоемкость с учетом ангармонизма равна: Здесь : g –
- 37. Вакансионный вклад в теплоемкость Равновесная концентрация вакансий: Появление вакансий приводит к росту энтальпии Вакансионный вклад в
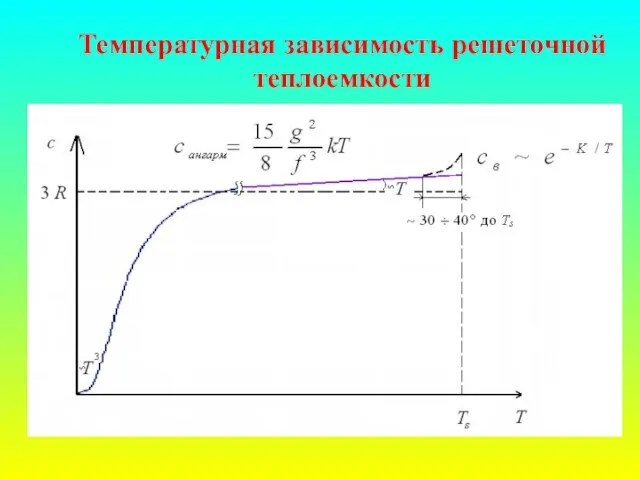
- 38. Температурная зависимость решеточной теплоемкости
- 39. Заключение Теплоемкость «скачет» - существует вклад, зависящий от положения в таблице Менделеева При высоких температурах реальная
- 40. Лекция 3. 1 час. Электронная составляющая теплоемкости 3.1 Электронная составляющая теплоемкости простых и переходных металлов. Общие
- 41. энергия Ферми Рассмотрим энергетический спектр одновалентного металла – в его зоне N-уровней, но занято N/2 Значение
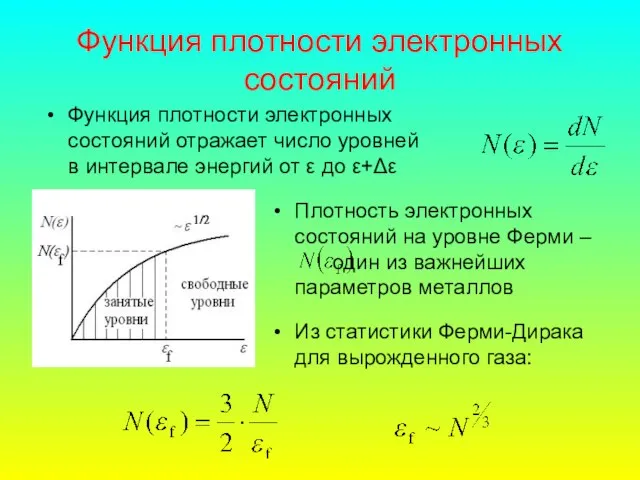
- 42. Функция плотности электронных состояний Функция плотности электронных состояний отражает число уровней в интервале энергий от ε
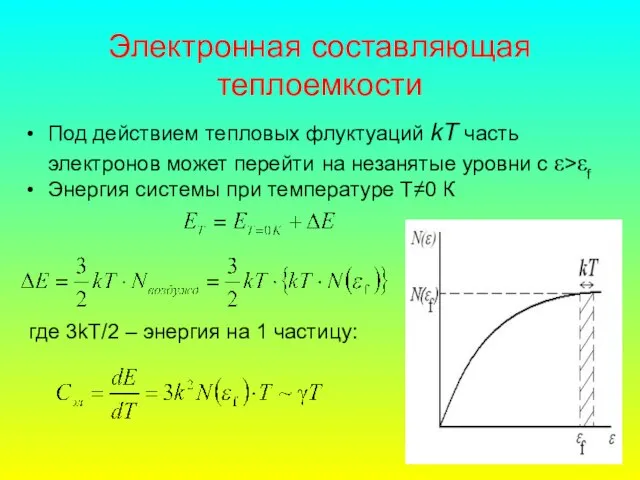
- 43. Электронная составляющая теплоемкости Под действием тепловых флуктуаций kT часть электронов может перейти на незанятые уровни с
- 44. Анализ электронной составляющей теплоемкости простых металлов Учет неидеальности, не одновалентности и квантовой статистики Оценка Сэл при
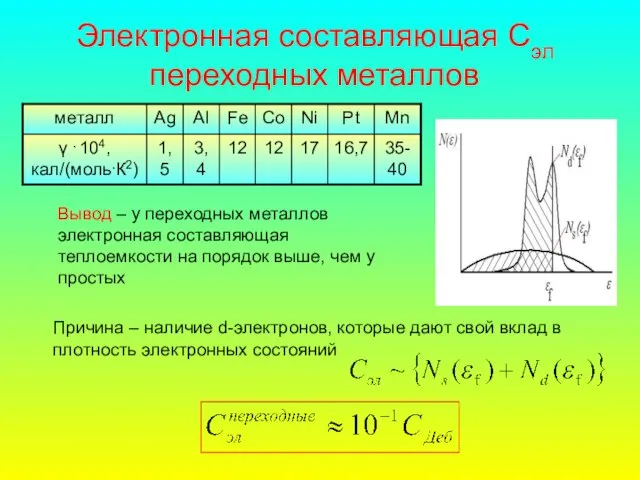
- 45. Электронная составляющая Сэл переходных металлов Вывод – у переходных металлов электронная составляющая теплоемкости на порядок выше,
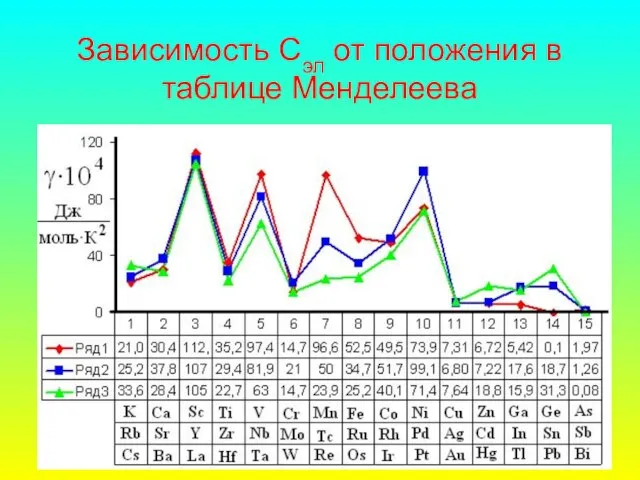
- 46. Зависимость Сэл от положения в таблице Менделеева
- 47. Магноны и их влияние на теплоемкость Магнон – квазичастица, описывающая магнитное возмущение спиновой системы ↑↑↑↑↑↑↑↑ -
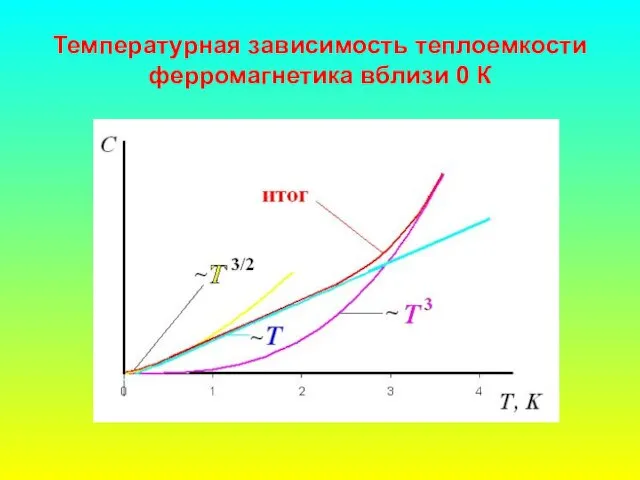
- 48. Температурная зависимость теплоемкости ферромагнетика вблизи 0 К
- 49. Лекция 3. Час 2 Поведение теплоемкости при фазовых переходах.
- 50. Связь теплоемкости с функциями термодинамического состояния и энергией Гиббса Фазовые переходы бывают 1 и 2 рода
- 51. Особенности ФП 1 и 2 рода
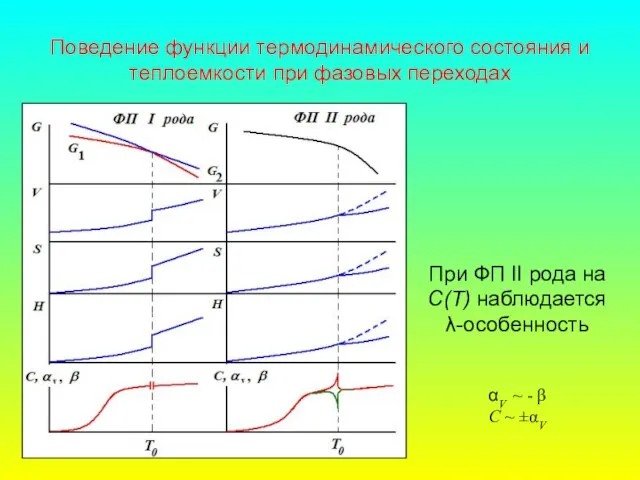
- 52. Поведение функции термодинамического состояния и теплоемкости при фазовых переходах При ФП II рода на С(Т) наблюдается
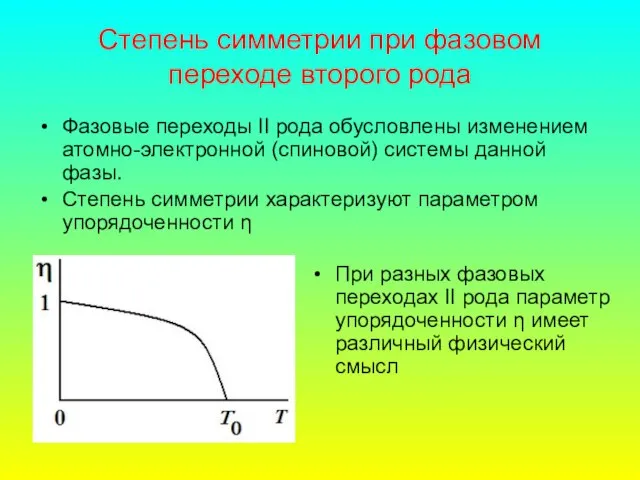
- 53. Степень симметрии при фазовом переходе второго рода Фазовые переходы II рода обусловлены изменением атомно-электронной (спиновой) системы
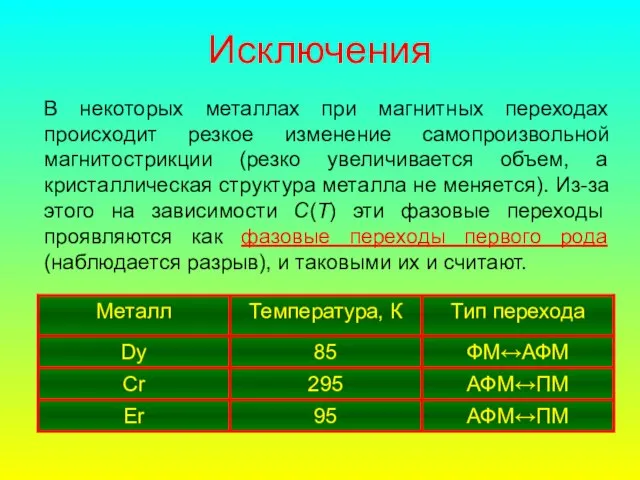
- 54. Примеры влияния ФП на теплоемкость. 1. Плавление металлов (ФП I рода) Для большинства металлов ΔS ≈
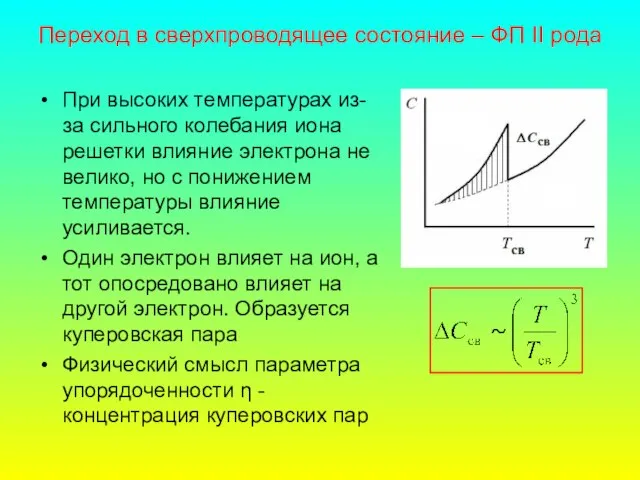
- 55. Магнитные превращения Переходы - ФМ↔ПМ; АФМ ↔ПМ; ФМ ↔АФМ При магнитном превращении происходит изменение степени упорядоченности
- 56. Исключения В некоторых металлах при магнитных переходах происходит резкое изменение самопроизвольной магнитострикции (резко увеличивается объем, а
- 57. Переход в сверхпроводящее состояние – ФП II рода При высоких температурах из-за сильного колебания иона решетки
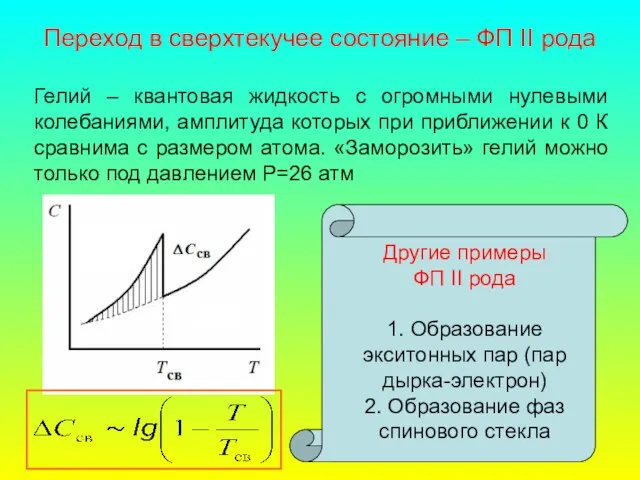
- 58. Переход в сверхтекучее состояние – ФП II рода Гелий – квантовая жидкость с огромными нулевыми колебаниями,
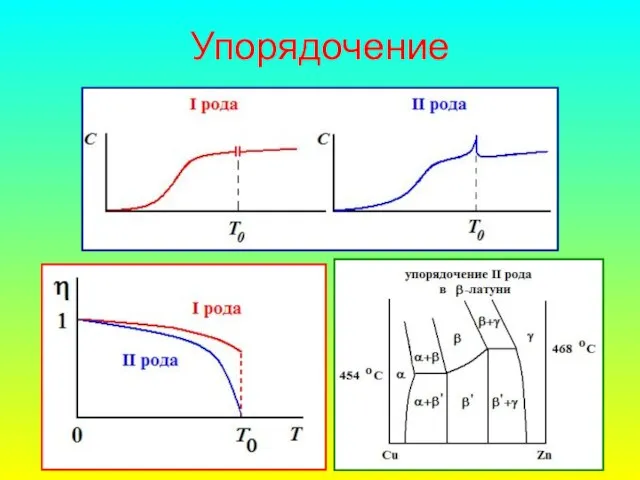
- 59. Упорядочение
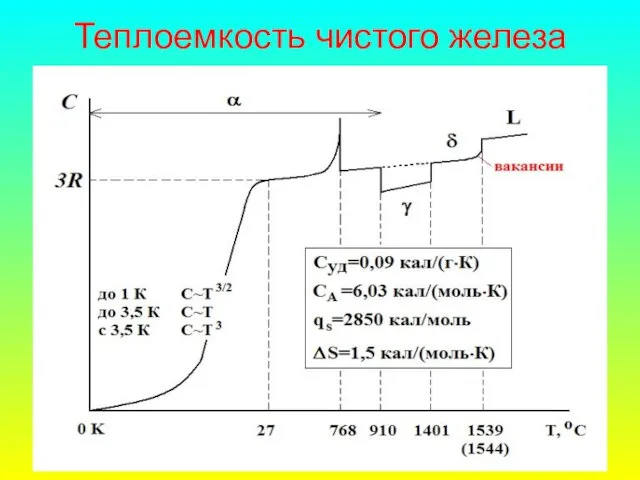
- 60. Теплоемкость чистого железа
- 61. Лекция 4. час 1 Теплоемкость сплавов и соединений
- 62. Теплоемкость сплавов Все изложенные ранее закономерности выполняются и для сплавов. Имеющиеся отличия обусловлены тем, что при
- 63. Расчет теплоемкости соединения Для теплоемкости при Т > θ справедливо правило аддитивности Неймана-Коппа : где x1
- 64. Расчет теплоемкости гетерогенной системы где q1 и q2 – массовые доли. Пример: Латунь Л80 (80%Cu+20%Zn) Cуд(Cu)=0,0909
- 65. Примеры расчета для У8
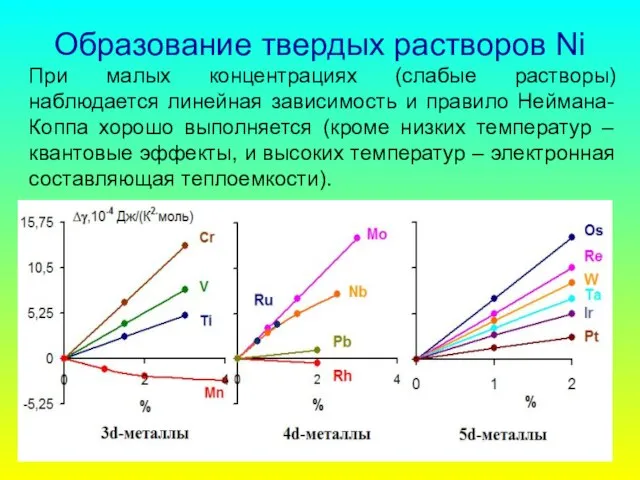
- 66. Образование твердых растворов Ni При малых концентрациях (слабые растворы) наблюдается линейная зависимость и правило Неймана-Коппа хорошо
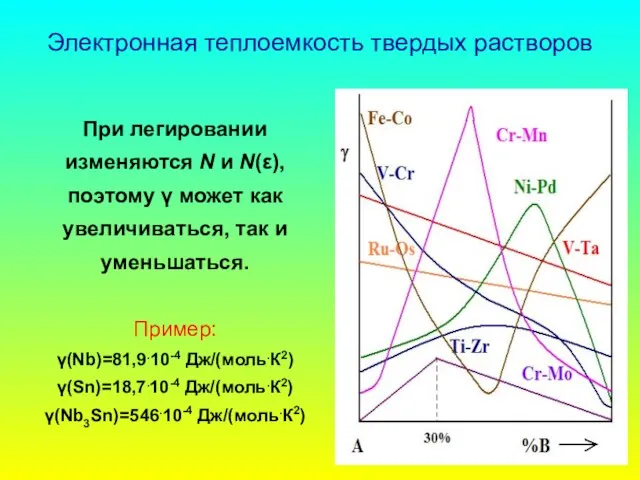
- 67. Электронная теплоемкость твердых растворов При легировании изменяются N и N(ε), поэтому γ может как увеличиваться, так
- 68. Лекция 4. час 2. 2.4. Зависимость теплоемкости от размеров структурных составляющих материалов. Теплоемкость сплавов в кристаллическом,
- 69. Теплоемкость наноматериалов Теплоемкость наноматериалов отличается от теплоемкости массивного материала такого же химического и фазового состава. Причины:
- 70. Влияние размера дисперсных частиц на cпектр колебаний решетки В ультрадисперсных системах могут возникать волны, длина которых
- 71. Зависимость теплоемкости от параметров частиц Теплоемкость крупнокристаллического тела объемом V по Дебаю при T Теплоемкость дисперсных
- 72. Квантовый подход к определению влияния размера частицы В квантовом приближении для сферической частицы радиусом r общее
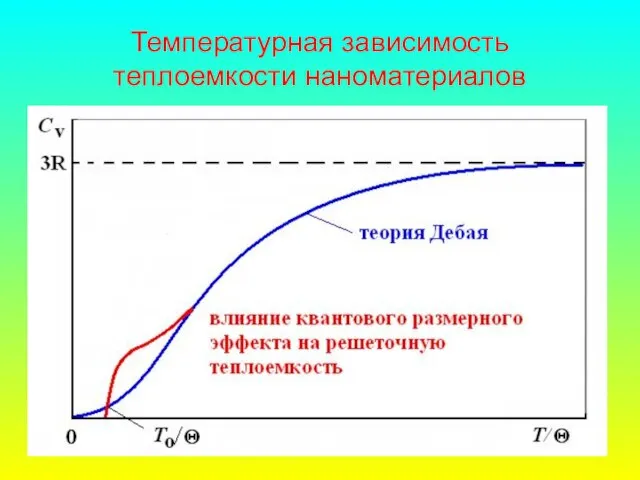
- 73. Температурная зависимость теплоемкости наноматериалов
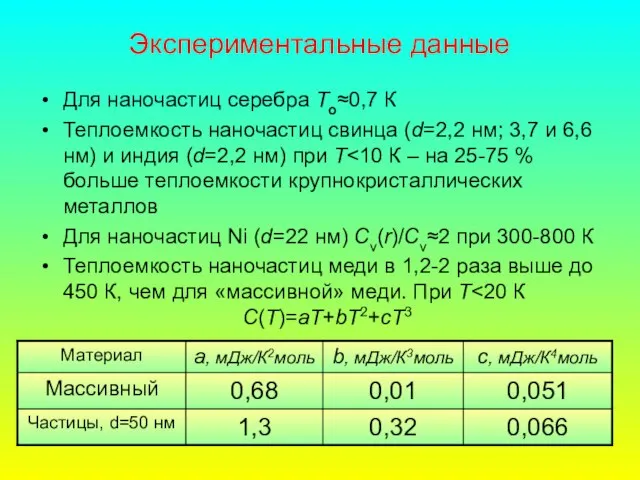
- 74. Экспериментальные данные Для наночастиц серебра То≈0,7 К Теплоемкость наночастиц свинца (d=2,2 нм; 3,7 и 6,6 нм)
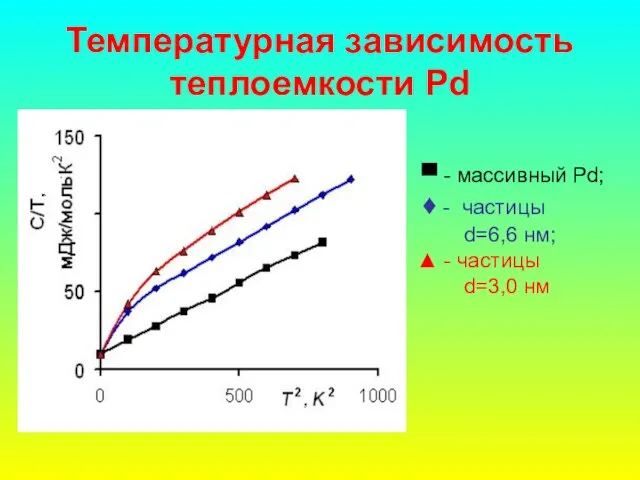
- 75. Температурная зависимость теплоемкости Pd ▀ - массивный Pd; ♦ - частицы d=6,6 нм; ▲ - частицы
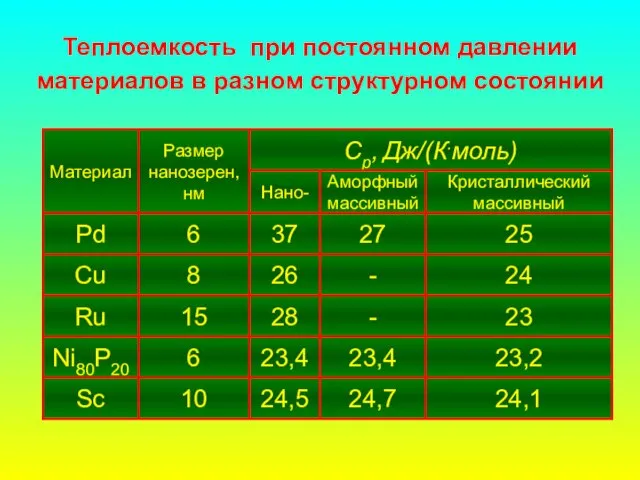
- 76. Теплоемкость при постоянном давлении материалов в разном структурном состоянии
- 77. Влияние дисперсности материала на температуру Дебая Соотношение между температурами Дебая массивного Θ и ультрадисперсного материалов Tд
- 79. Скачать презентацию











![Виды теплоемкости Теплоемкость тела: C = δQ/dT [Дж/К]. Удельная теплоемкость: Суд =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/366147/slide-16.jpg)













![Число фононов Число фононов n = 1/[exp(1/x)-1], где x = ħω/kT. Общее](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/366147/slide-33.jpg)




















 Окрылённые призванием «Секрет учительского счастья» Золотарев Андрей Алексеевич Учитель истории и обществ
Окрылённые призванием «Секрет учительского счастья» Золотарев Андрей Алексеевич Учитель истории и обществ Нефть и газ.
Нефть и газ. Дифференциальный манометр ДСП-80В-РАСКО
Дифференциальный манометр ДСП-80В-РАСКО Личные границы ребенка
Личные границы ребенка Методические рекомендации по организации самостоятельных занятий спортом
Методические рекомендации по организации самостоятельных занятий спортом Презентация на тему ПРОФЕССИЯ Ветеринарный врач
Презентация на тему ПРОФЕССИЯ Ветеринарный врач  ПИСЬМО РОССИЙСКОМУ ДРУГУ
ПИСЬМО РОССИЙСКОМУ ДРУГУ Facebook – начало освоения технологии работы Кто-то сказал: «Facebook можно сравнить с телевизором: в нем есть миллионы каналов, только их не надо переключать - достаточно один раз на нужные подписаться, а потом сидеть перед экраном и просто смотреть»
Facebook – начало освоения технологии работы Кто-то сказал: «Facebook можно сравнить с телевизором: в нем есть миллионы каналов, только их не надо переключать - достаточно один раз на нужные подписаться, а потом сидеть перед экраном и просто смотреть»  Порядок допуска локомотивов принадлежащих ОАО РЖД на пути общего пользования
Порядок допуска локомотивов принадлежащих ОАО РЖД на пути общего пользования «Московский государственный университетимени М. В. Ломоносова» Экономический факультет ПРЕЗЕНТАЦИЯ К ВЫПУСКНОЙ КВАЛИФИКАЦИ
«Московский государственный университетимени М. В. Ломоносова» Экономический факультет ПРЕЗЕНТАЦИЯ К ВЫПУСКНОЙ КВАЛИФИКАЦИ Путешествие в Великобританию
Путешествие в Великобританию КОМПЛЕКС ES TECK СОСТОИТ ИЗ 4-Х МЕТОДИК (HRV, SPo2, BC, EIS)
КОМПЛЕКС ES TECK СОСТОИТ ИЗ 4-Х МЕТОДИК (HRV, SPo2, BC, EIS) Путешествие в страну «Математика»
Путешествие в страну «Математика» ИЗОБРАЗИТЕЛЬНОЕ ИСКУССТВО 7 КЛАСС 8 февраля 2012г. учитель: Евтеева Татьяна Николаевна
ИЗОБРАЗИТЕЛЬНОЕ ИСКУССТВО 7 КЛАСС 8 февраля 2012г. учитель: Евтеева Татьяна Николаевна История германии
История германии Презентация на тему Образ Богородицы в иконографии
Презентация на тему Образ Богородицы в иконографии  Сельское хозяйство
Сельское хозяйство Puteshestvie_po_miru
Puteshestvie_po_miru Спорт – норма жизни! 5-9 классы
Спорт – норма жизни! 5-9 классы Баухаус.Фото
Баухаус.Фото Урок математики в 4 классе
Урок математики в 4 классе Формирование учебно-познавательной мотивации обучающихся на уроках русского языка и литературы через технологию КМ
Формирование учебно-познавательной мотивации обучающихся на уроках русского языка и литературы через технологию КМ Проект Эконаукоград Солнцеград. Фонд Лазурные Города
Проект Эконаукоград Солнцеград. Фонд Лазурные Города Технология возделывание зерновых культур
Технология возделывание зерновых культур Презентация на тему А.А.Фет. Весенний дождь. Бабочка
Презентация на тему А.А.Фет. Весенний дождь. Бабочка  Сбер - больше чем банк
Сбер - больше чем банк Краевой конкурс детского фольклорного творчества «Солнцеворот»
Краевой конкурс детского фольклорного творчества «Солнцеворот» Моделирование юбки
Моделирование юбки