Содержание
- 2. Повторение Перечислите основные положения МКТ. Дайте определение относительной молекулярной массы. Что такое количество вещества? Что такое
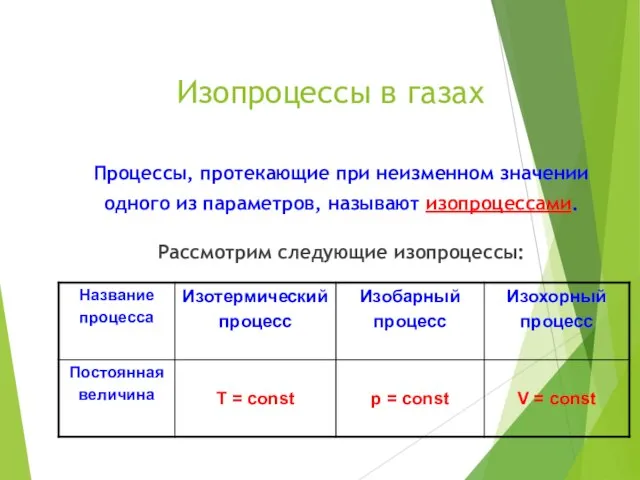
- 3. Изопроцессы в газах Процессы, протекающие при неизменном значении одного из параметров, называют изопроцессами. Рассмотрим следующие изопроцессы:
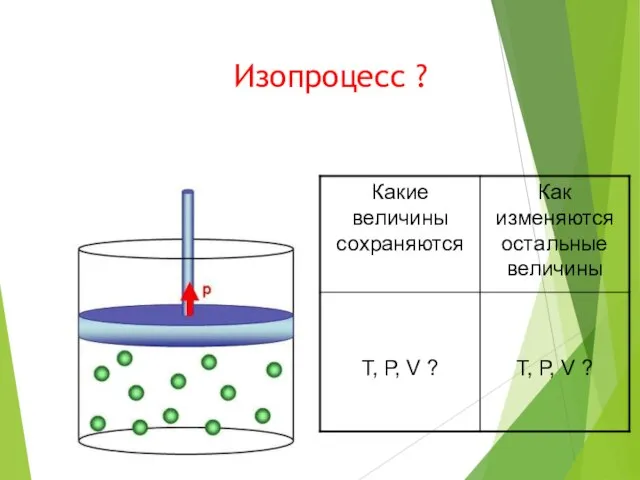
- 4. Изопроцесс ?
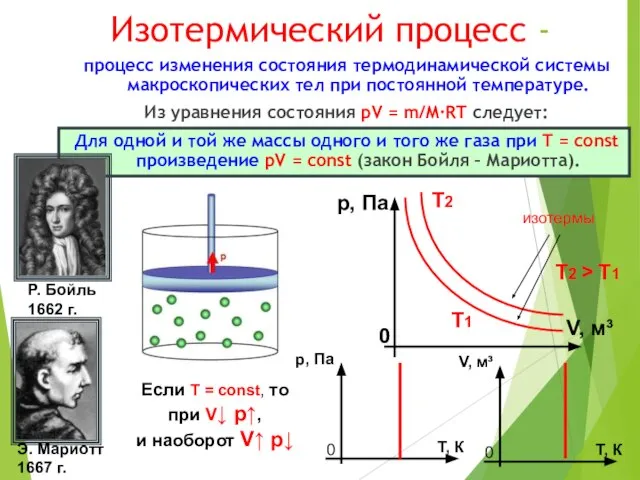
- 5. Изотермический процесс - процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре. Из уравнения состояния
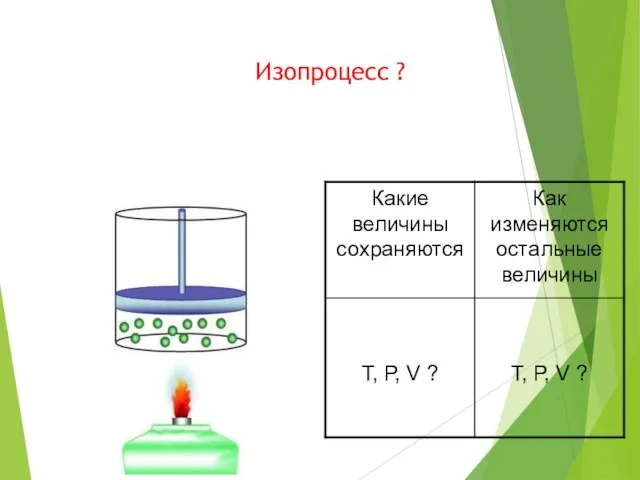
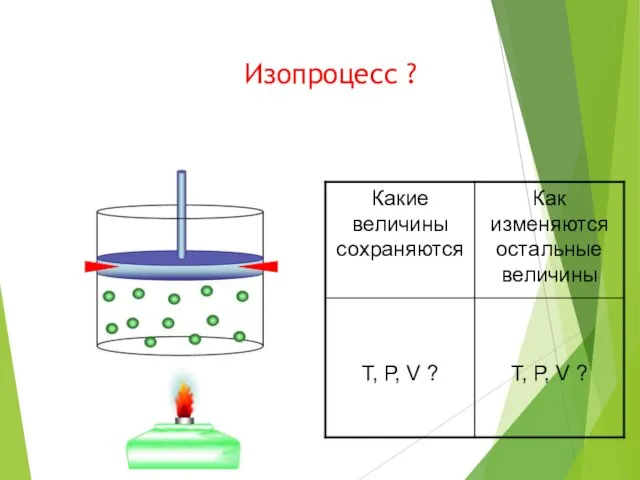
- 6. Изопроцесс ?
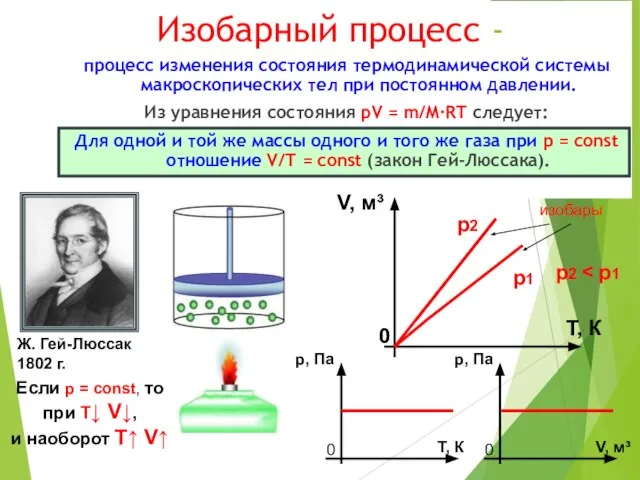
- 7. Изобарный процесс - процесс изменения состояния термодинамической системы макроскопических тел при постоянном давлении. Из уравнения состояния
- 8. Изопроцесс ?
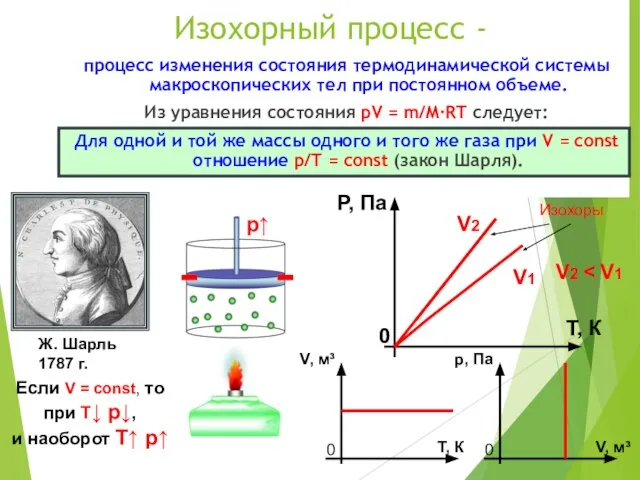
- 9. Изохорный процесс - процесс изменения состояния термодинамической системы макроскопических тел при постоянном объеме. Из уравнения состояния
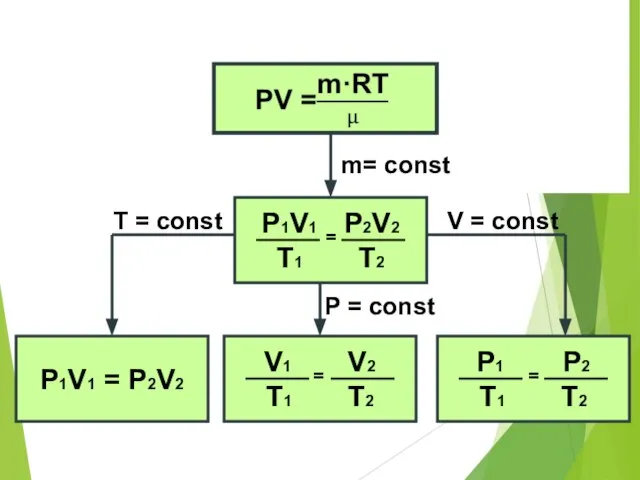
- 10. m= const P1V1 = P2V2 V = const T = const P = const
- 11. Повторение. Пройди тест.
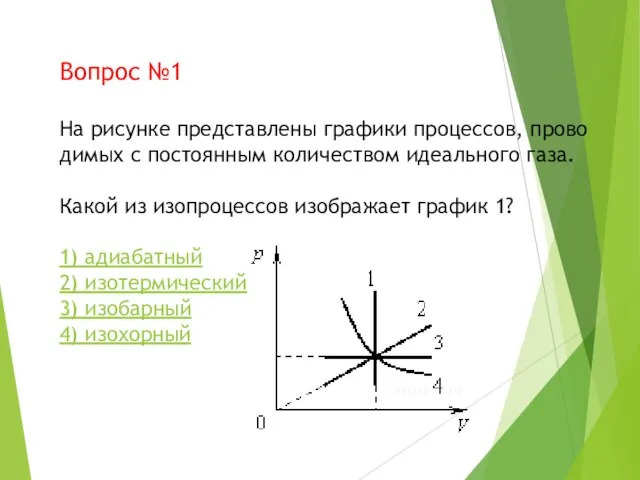
- 12. Вопрос №1 На рисунке представлены графики процессов, проводимых с постоянным количеством идеального газа. Какой из изопроцессов
- 13. Неверно Из рисунка видно, что процесс 1 идет при постоянном объеме. Такой процесс называется изохорным. Правильный
- 14. Верно
- 15. Идеальный газ сначала нагревался при постоянном давлении, потом его давление уменьшалось при постоянном объеме, затем при
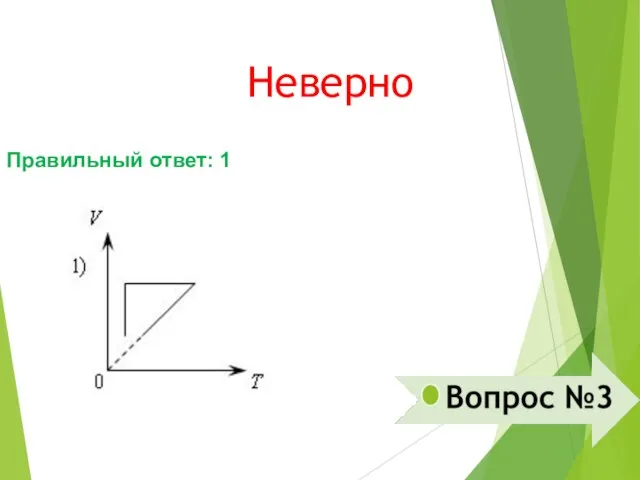
- 16. Неверно Правильный ответ: 1
- 17. Верно
- 18. Вопрос №3 Постоянная масса идеального газа участвует в процессе, показанном на рисунке. Наименьшему давлению газа в
- 19. Неверно Правильный ответ: 3
- 20. Верно
- 21. Вопрос №4 На рисунке изображён процесс перехода идеального газа из состояния А в состояние Б .
- 22. Неверно Правильный ответ: 2
- 23. Верно
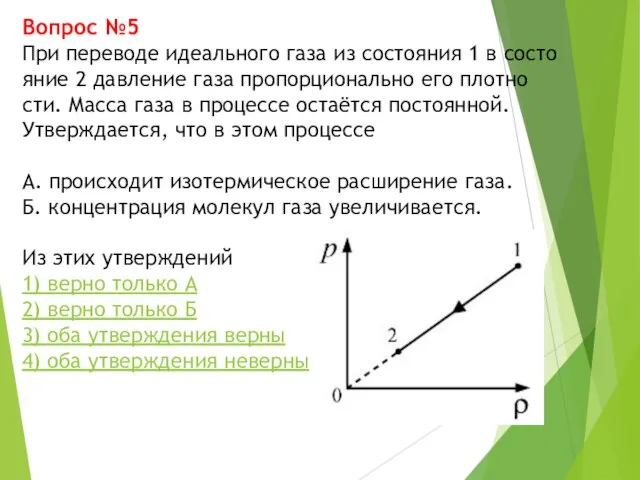
- 24. Вопрос №5 При переводе идеального газа из состояния 1 в состояние 2 давление газа пропорционально его
- 25. Неверно Правильный ответ: 1
- 26. Верно
- 27. Вопрос №6 Разогретую колбу плотно закрыли пробкой и оставили остывать. Какое из приведённых ниже уравнений точнее
- 28. Неверно Правильный ответ: 2
- 29. Верно
- 31. Скачать презентацию

















 Движение тела по окружности под действием силы тяжести
Движение тела по окружности под действием силы тяжести Суперпроводники. История открытия
Суперпроводники. История открытия Газовые законы
Газовые законы Проводники с током в магнитном поле. Лекция 7
Проводники с током в магнитном поле. Лекция 7 Тормозные системы
Тормозные системы Кинематика
Кинематика Электромагнитные волны. Лекция 11
Электромагнитные волны. Лекция 11 Презентация на тему Выталкивающая сила
Презентация на тему Выталкивающая сила  Определение проекции силы на координатную ось
Определение проекции силы на координатную ось Инновационные технологии в машиностроении. Лекция 1, 2. Общая характеристика машиностроительного производства
Инновационные технологии в машиностроении. Лекция 1, 2. Общая характеристика машиностроительного производства Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков
Разработка инструментария для решения задачи вычислительной гидродинамики при моделировании воздушных потоков Радиоактивные превращения атомных ядер
Радиоактивные превращения атомных ядер Общие сведения о системах радиосвязи. Электропитание средств связи
Общие сведения о системах радиосвязи. Электропитание средств связи Общий осмотр автомобиля Toyota Mark II
Общий осмотр автомобиля Toyota Mark II Презентация на тему Интерференция. Дифракция
Презентация на тему Интерференция. Дифракция  Неразъемные соединения
Неразъемные соединения Слесарные инструменты
Слесарные инструменты Урок 12 Електродвигуни. Електровимірювальні прилади
Урок 12 Електродвигуни. Електровимірювальні прилади Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями
Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями Международная система единиц СИ
Международная система единиц СИ Презентация на тему Источники электрического тока
Презентация на тему Источники электрического тока  Фильтры с бесконечной импульсной характеристикой. Синтез БИХ-фильтров методом билинейного Z-преобразования''
Фильтры с бесконечной импульсной характеристикой. Синтез БИХ-фильтров методом билинейного Z-преобразования'' Однородные уравнения. Уравнения, приводящиеся к однородным
Однородные уравнения. Уравнения, приводящиеся к однородным Построение изображений, полученных с помощью линз
Построение изображений, полученных с помощью линз Определение коэффициента поверхностного натяжения синтетических моющих средств
Определение коэффициента поверхностного натяжения синтетических моющих средств Электроэнергия Ксенон (Светодиоды)
Электроэнергия Ксенон (Светодиоды) Графическое представление результатов измерений
Графическое представление результатов измерений Блоки цилиндров и цилиндровые втулки
Блоки цилиндров и цилиндровые втулки