Содержание
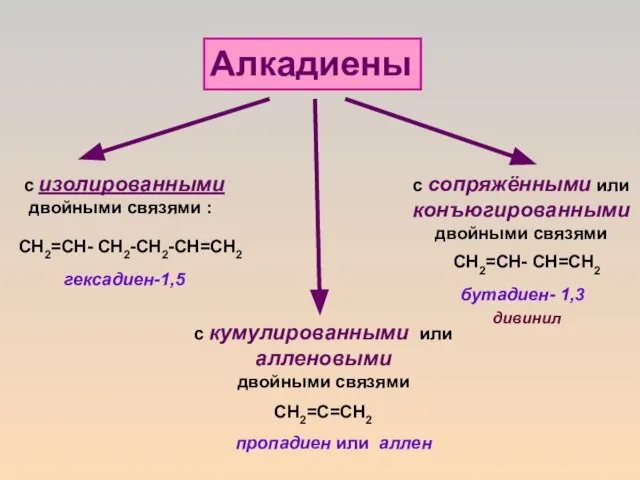
- 2. Алкадиены с изолированными двойными связями : СН2=СН- СН2-СН2-СН=СН2 с кумулированными или алленовыми двойными связями СН2=С=СН2 гексадиен-1,5
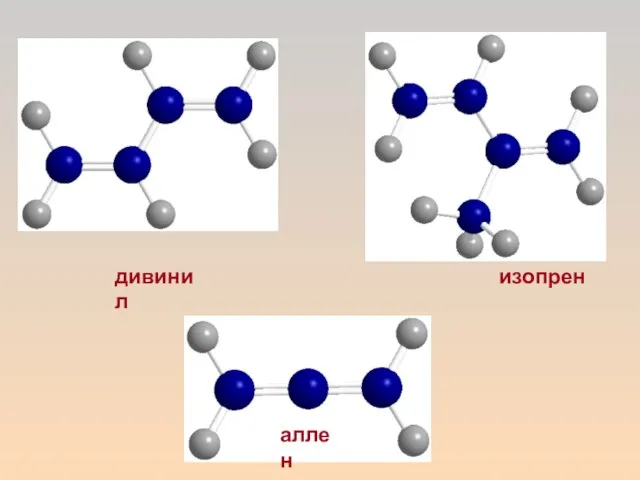
- 3. дивинил изопрен аллен
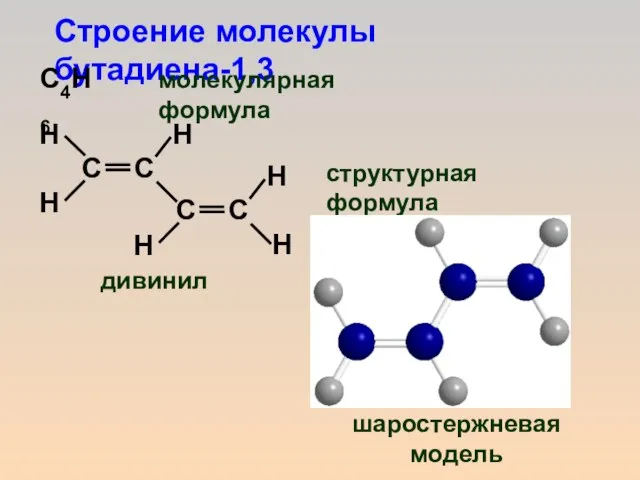
- 4. Строение молекулы бутадиена-1,3 C4H6 молекулярная формула структурная формула шаростержневая модель дивинил
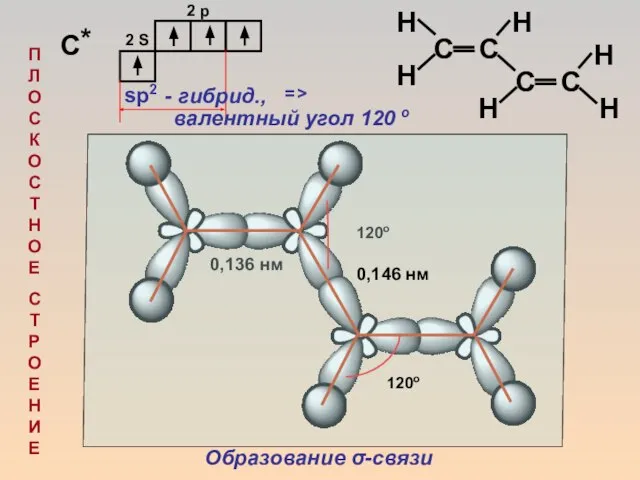
- 5. 120o 0,136 нм 2 S sp2 - гибрид., П Л О С К О С Т
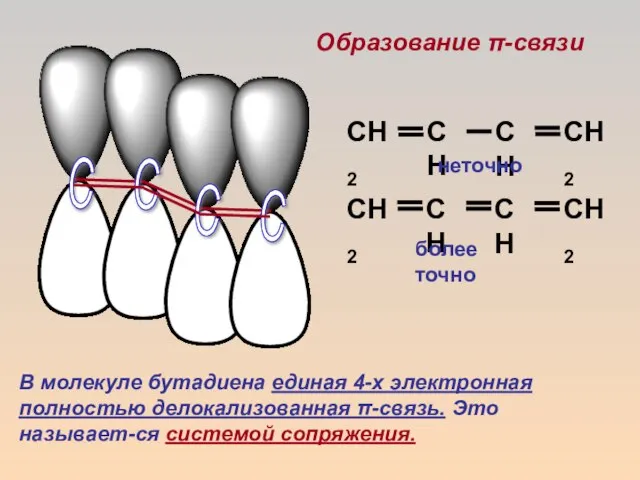
- 6. С С С С неточно более точно
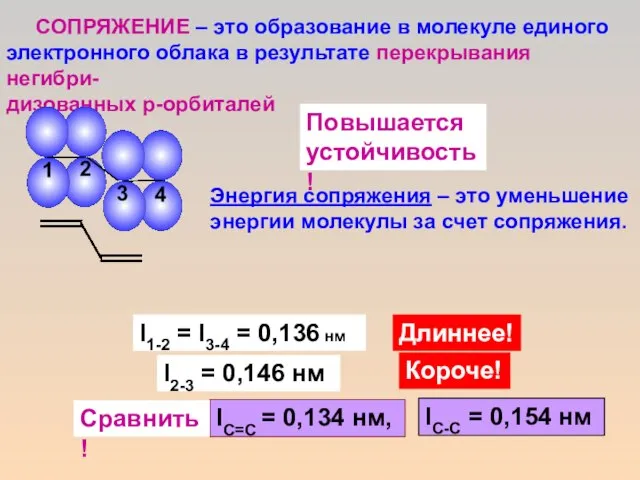
- 7. СОПРЯЖЕНИЕ – это образование в молекуле единого электронного облака в результате перекрывания негибри- дизованных р-орбиталей l2-3
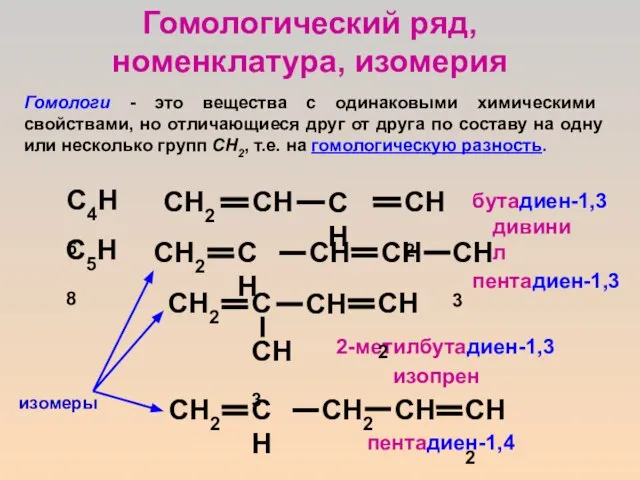
- 8. Гомологи - это вещества с одинаковыми химическими свойствами, но отличающиеся друг от друга по составу на
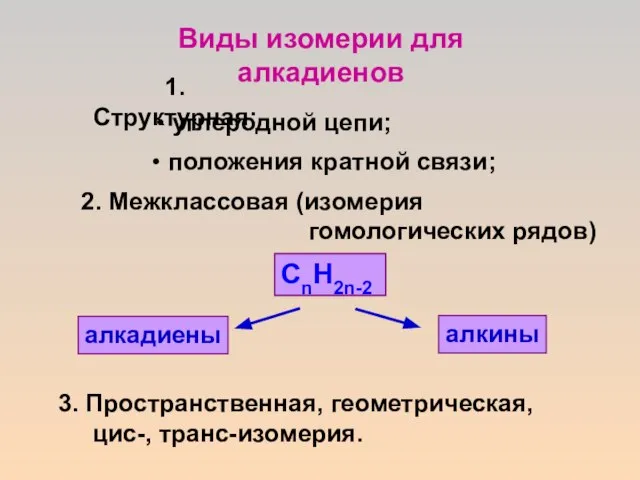
- 9. Виды изомерии для алкадиенов 1. Структурная: углеродной цепи; положения кратной связи; 2. Межклассовая (изомерия гомологических рядов)
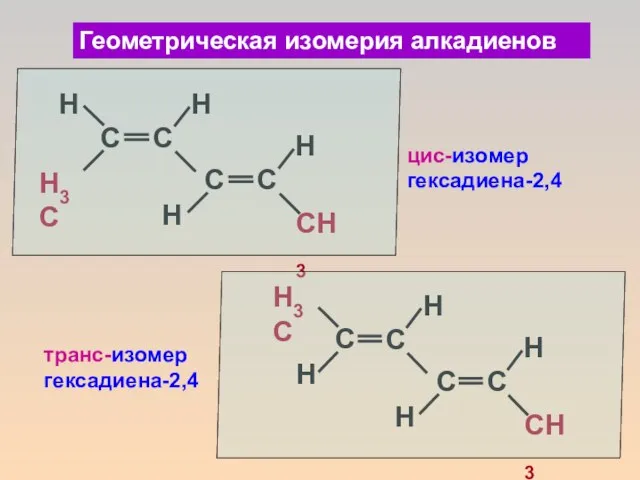
- 10. Геометрическая изомерия алкадиенов цис-изомер гексадиена-2,4 транс-изомер гексадиена-2,4
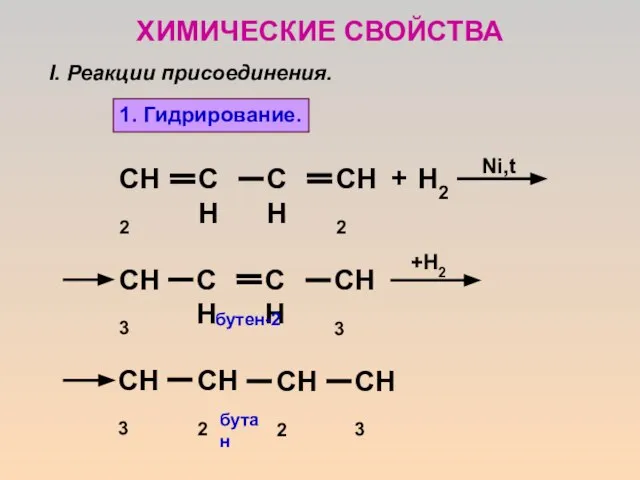
- 11. ХИМИЧЕСКИЕ СВОЙСТВА I. Реакции присоединения. Ni,t +H2 бутен-2 бутан 1. Гидрирование.
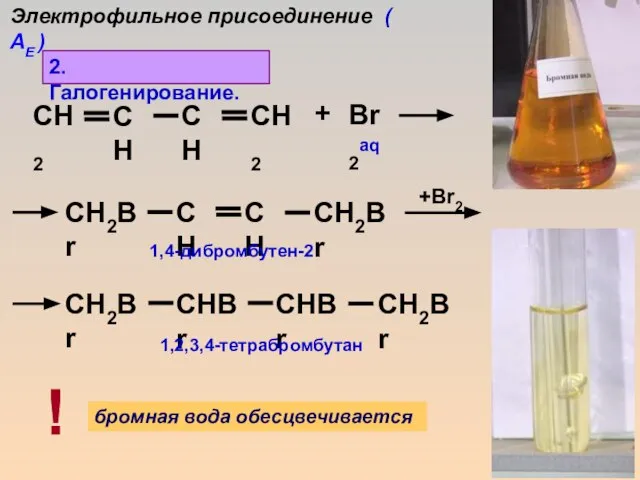
- 12. Br2 +Br2 + 1,4-дибромбутен-2 1,2,3,4-тетрабромбутан aq 2. Галогенирование. бромная вода обесцвечивается ! Электрофильное присоединение ( АЕ
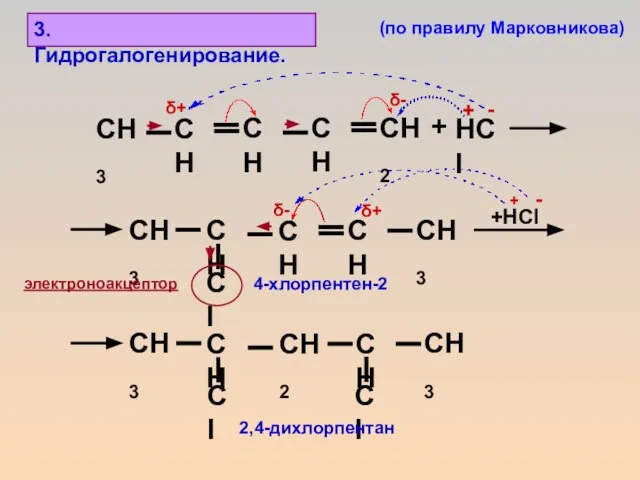
- 13. + HCl +HCl δ- δ+ δ- δ+ 3. Гидрогалогенирование. 4-хлорпентен-2 2,4-дихлорпентан + - + - электроноакцептор
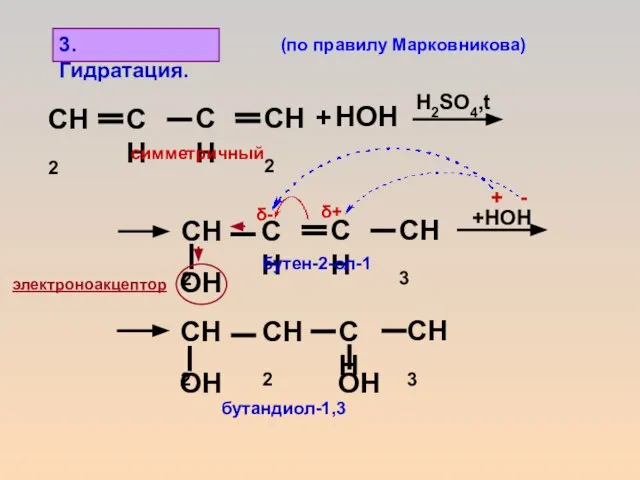
- 14. +HOH δ- δ+ 3. Гидратация. бутен-2-ол-1 бутандиол-1,3 симметричный H2SO4,t + - электроноакцептор (по правилу Марковникова)
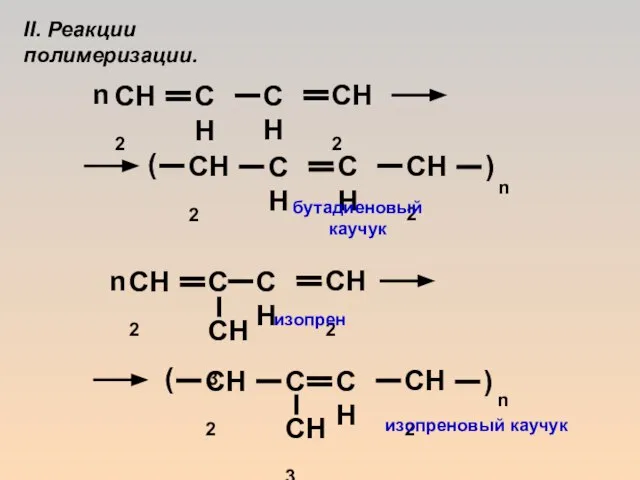
- 15. n ( ) n n ( ) n бутадиеновый каучук изопрен изопреновый каучук II. Реакции полимеризации.
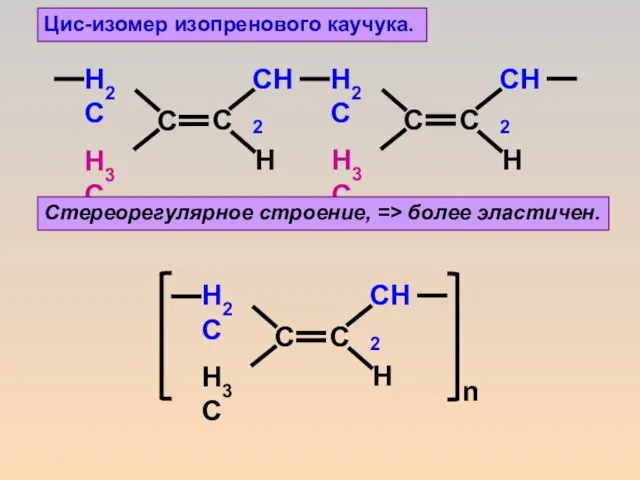
- 16. Цис-изомер изопренового каучука. Стереорегулярное строение, => более эластичен.
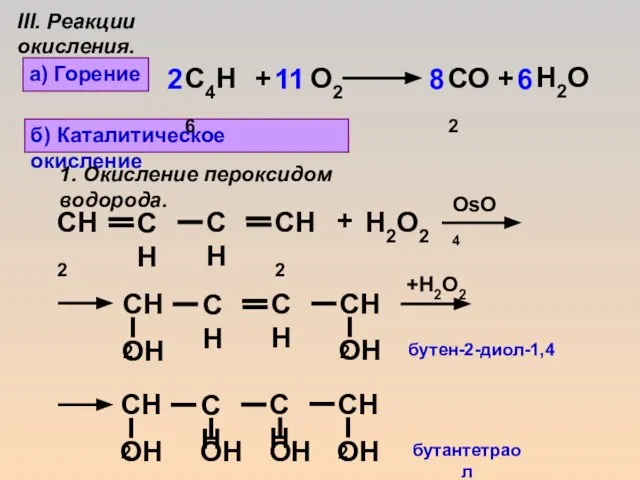
- 17. б) Каталитическое окисление + Н2О2 OsO4 +H2O2 1. Окисление пероксидом водорода. а) Горение С4Н6 + О2
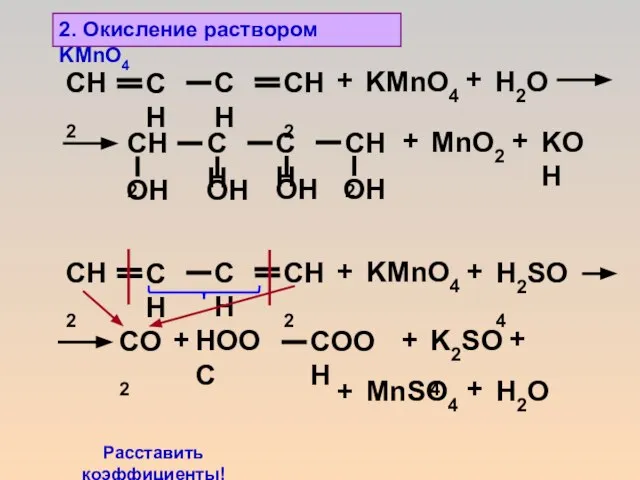
- 18. 2. Окисление раствором KMnO4 + KMnO4 + Н2О + MnO2 + KОН + KMnO4 + Н2SО4
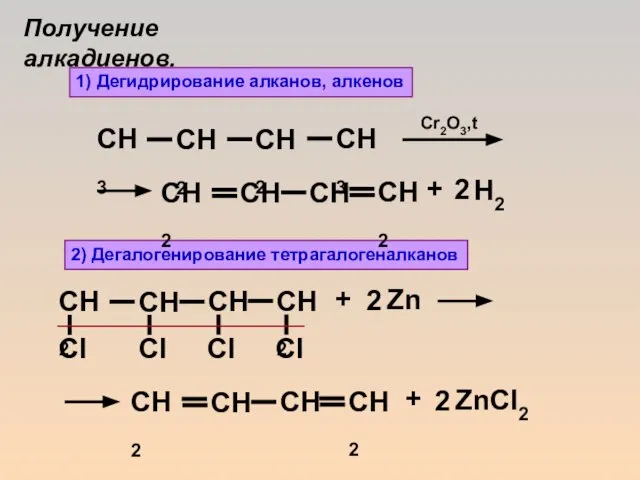
- 19. 1) Дегидрирование алканов, алкенов 2) Дегалогенирование тетрагалогеналканов + + + Cr2O3,t Получение алкадиенов.
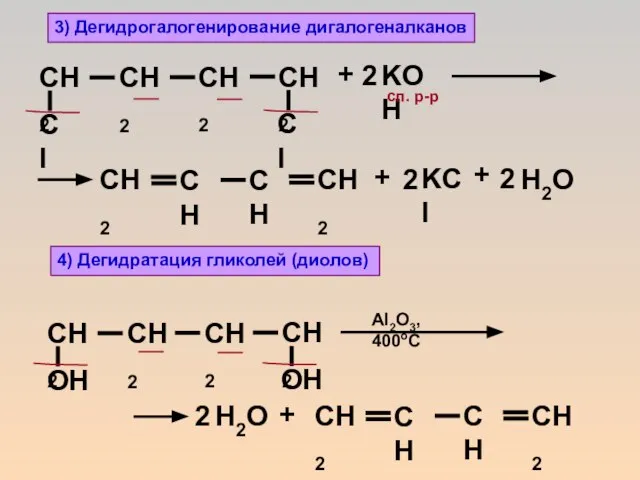
- 20. 3) Дегидрогалогенирование дигалогеналканов + KOH 2 + + сп. р-р + Al2O3, 400oC 4) Дегидратация гликолей
- 22. Скачать презентацию
 Драгоценные камни
Драгоценные камни Калифорний Cf
Калифорний Cf Понятие биотехнологии
Понятие биотехнологии Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Вязкоупругие свойства полимеров
Вязкоупругие свойства полимеров Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Строение и свойства металлов
Строение и свойства металлов Валентность химических элементов
Валентность химических элементов Строение веществ
Строение веществ Щелочноземельные металлы
Щелочноземельные металлы Актиний. Нахождение в природе
Актиний. Нахождение в природе Кремень. Нахождение в природе
Кремень. Нахождение в природе Исследование свойств модельной смеси сополимера Акритана-С с ЛД-70
Исследование свойств модельной смеси сополимера Акритана-С с ЛД-70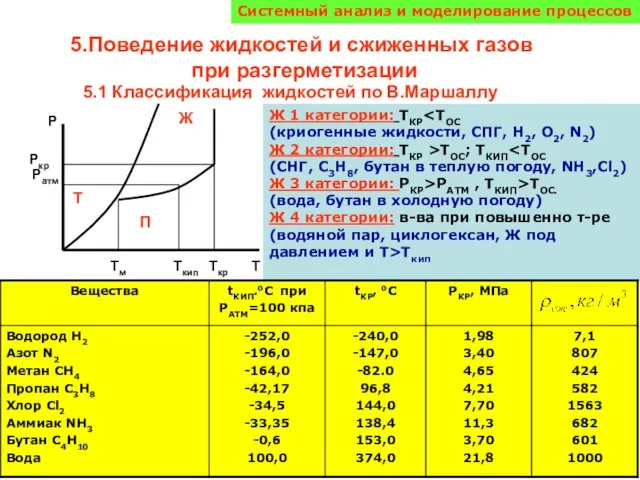 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Типичные экспериментальные кинетические данные
Типичные экспериментальные кинетические данные Задача №2 Спящий Амур. Команда гимназии №1 Берлинская лазурь
Задача №2 Спящий Амур. Команда гимназии №1 Берлинская лазурь Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химические явления. Закон сохранения массы веществ
Химические явления. Закон сохранения массы веществ Химическая связь
Химическая связь Алифатические и ароматические амины
Алифатические и ароматические амины Окислительно-восстановительные реакции. 8 класс
Окислительно-восстановительные реакции. 8 класс Шаблон презентации по химии
Шаблон презентации по химии Выращивание кристаллов соли (домашний эксперимент)
Выращивание кристаллов соли (домашний эксперимент) Научные принципы химического производства
Научные принципы химического производства Материалы космической техники
Материалы космической техники Минералы
Минералы Вещества простые и сложные
Вещества простые и сложные