Содержание
- 2. Бром Бром — химический элемент с атомным номером 35. Химически активный неметалл, относится к группе галогенов.
- 3. Физические свойства брома При обычных условиях бром — красно-бурая летучая жидкость с резким неприятным запахом, ядовит,
- 4. ● В свободном виде существует в виде двухатомных молекул Br₂. Химические свойства брома ● Бром немного,
- 6. Скачать презентацию
Слайд 2Бром
Бром — химический элемент с атомным номером 35. Химически активный неметалл, относится
Бром
Бром — химический элемент с атомным номером 35. Химически активный неметалл, относится

к группе галогенов. Простое вещество бром при нормальных условиях является тяжёлой едкой жидкостью красно-бурого цвета с сильным неприятным «тяжёлым» запахом, отдалённо напоминающим запах одновременно йода и хлора. Летуч, ядовит. Молекула брома двухатомна
(формула Br2)
Слайд 3Физические свойства брома
При обычных условиях бром — красно-бурая летучая жидкость с резким
Физические свойства брома
При обычных условиях бром — красно-бурая летучая жидкость с резким

неприятным запахом, ядовит, при соприкосновении с кожей образуются ожоги. Бром — одно из двух простых веществ (и единственное из неметаллов), наряду со ртутью, которое при комнатной температуре является жидким. Температура кипения составляет +58,6 °C, при кипении бром превращается из жидкости в буро-коричневые пары, при вдыхании раздражающие дыхательные пути.
Слайд 4● В свободном виде существует в виде двухатомных молекул Br₂.
Химические свойства брома
●
● В свободном виде существует в виде двухатомных молекул Br₂.
Химические свойства брома
●

Бром немного, но лучше других галогенов растворим в воде
● По химической активности бром занимает промежуточное положение между хлором и йодом.
● Реакция брома с водородом протекает при нагревании и приводит к образованию бромоводорода HBr.
● С кислородом и азотом бром непосредственно не реагирует.
- Предыдущая
Классы неорганических веществ. ОксидыСледующая -
Louis de Funès Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Алкены. Физические и химические свойства
Алкены. Физические и химические свойства Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химически опасные объекты Аварии, связанные с выбросом АХОВ
Химически опасные объекты Аварии, связанные с выбросом АХОВ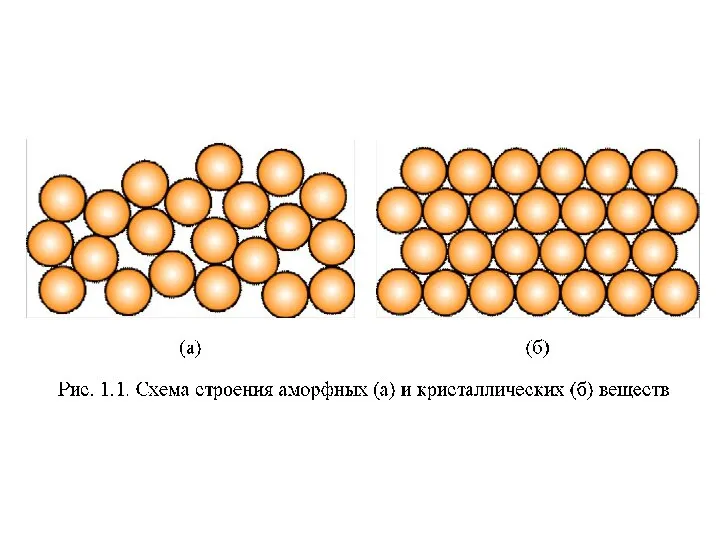 Материаловедение
Материаловедение Синтетические волокна
Синтетические волокна Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Электролиз (катод)
Электролиз (катод) Основные принципы работы химических сенсоров
Основные принципы работы химических сенсоров Химическая картина мира
Химическая картина мира Основания: определение, классификация, химические свойства
Основания: определение, классификация, химические свойства Металлы. Общая характеристика, химические свойства. Получение
Металлы. Общая характеристика, химические свойства. Получение Вебинар. Гидролиз солей
Вебинар. Гидролиз солей Свойства радиоактивных элементов
Свойства радиоактивных элементов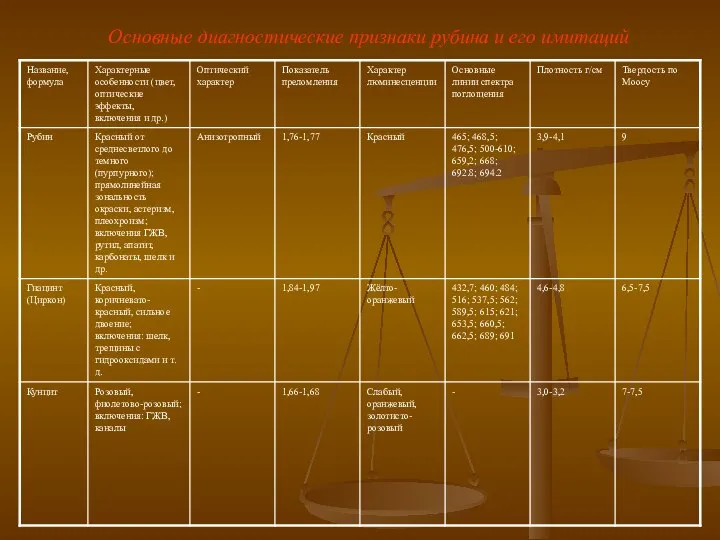 Основные диагностические признаки рубина и его имитаций
Основные диагностические признаки рубина и его имитаций Генетические ряды неорганических соединений
Генетические ряды неорганических соединений Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства
Двойные латуни. Диаграмма состояния. Примеси. Структура и свойства Вуглеводи. Визначення вуглеводів
Вуглеводи. Визначення вуглеводів Галогены. Обобщение знаний
Галогены. Обобщение знаний Подготовка к ГИА по химии
Подготовка к ГИА по химии Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым ОВ. Структура и принцип работы параметры ОВ
ОВ. Структура и принцип работы параметры ОВ Абсолютное первенство по химии - 2012
Абсолютное первенство по химии - 2012 строение атома углерода. Валентные состояния атома углерода
строение атома углерода. Валентные состояния атома углерода Общая характеристика элементов IIА группы
Общая характеристика элементов IIА группы Вода… Химические названия
Вода… Химические названия Водород – первый элемент в периодической таблице
Водород – первый элемент в периодической таблице Кристаллы, выращенные учащимися
Кристаллы, выращенные учащимися