Содержание
- 2. 02.10.2015 Валентность химических элементов
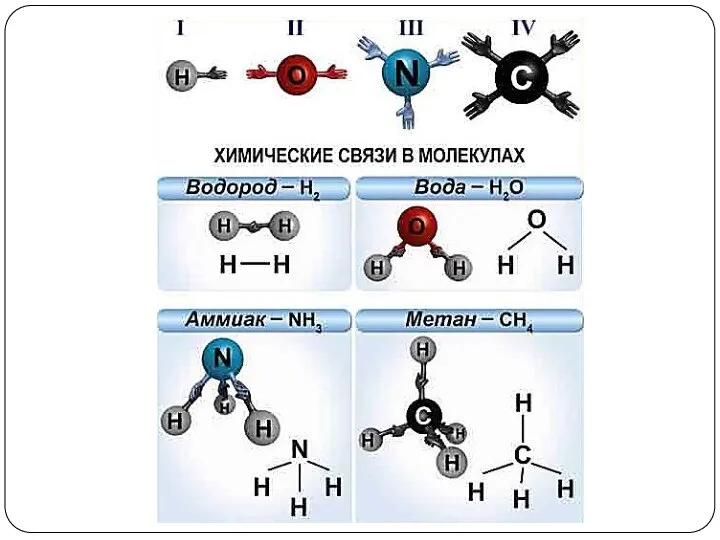
- 3. Валентность – способность атомов присоединять определенное число других атомов. Водород всегда одновалентен, кислород - двухвалентен. Значение
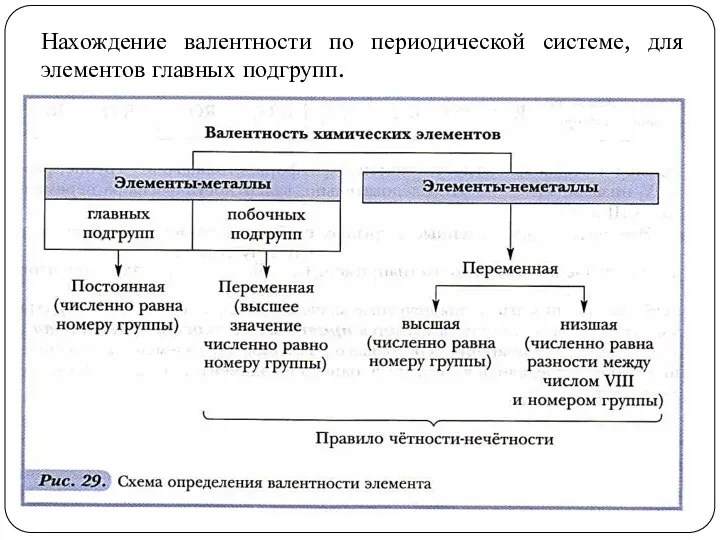
- 5. Нахождение валентности по периодической системе, для элементов главных подгрупп.
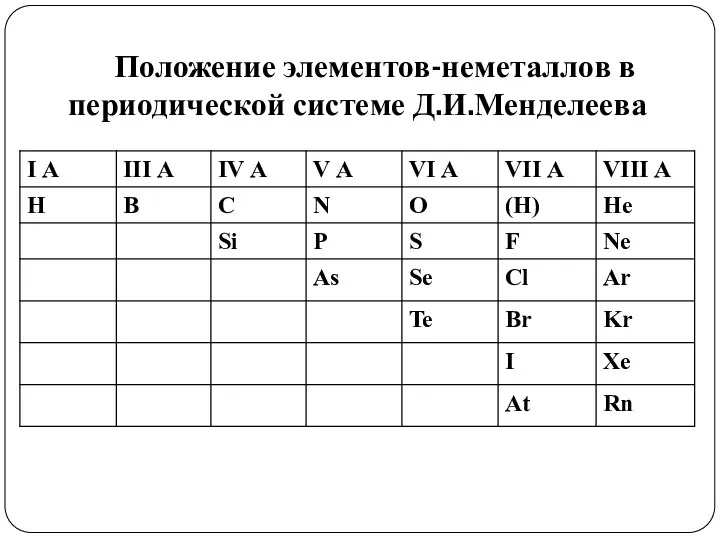
- 6. Положение элементов-неметаллов в периодической системе Д.И.Менделеева
- 7. Для металлов А-подгрупп валентность совпадает с номером группы. Для неметаллов определяют две валентности: высшую – валентность
- 8. Элементы, которые не подчиняются правилу нахождения валентности по номеру группы: Железо Fe (II, III) Медь Cu
- 9. Правило четности-нечетности Элементы расположенные в группах с четными номерами имеют четное значение валентности. Элементы расположенные в
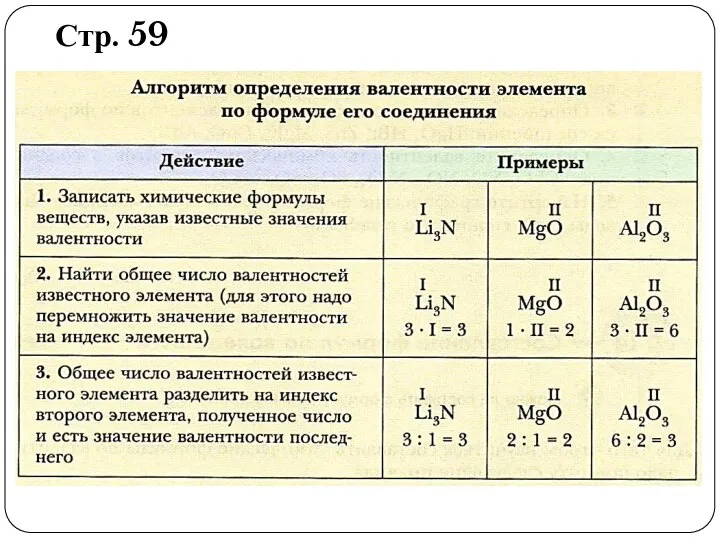
- 10. Стр. 59
- 12. Скачать презентацию




 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества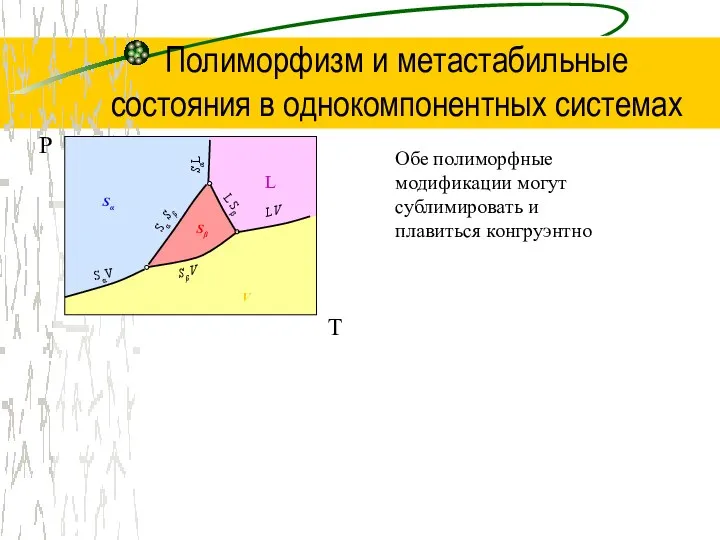 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості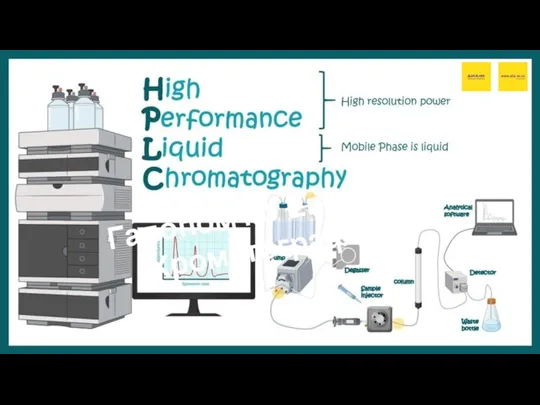 Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі