Содержание
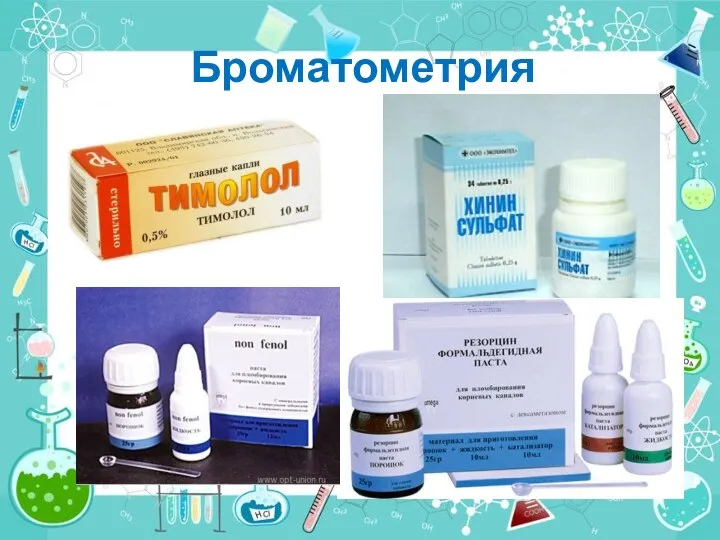
- 2. Броматометрия
- 3. ТИТРАНТ броматометрического титрования Первичный стандартный раствор (раствор с приготовленным титром) 0,1 моль/л KBrO3 Не меняет свой
- 4. Броматометрическое титрование основанное на окислении определяемого вещества броматом в кислой среде ВrОз- + 6Н+ + 6е→
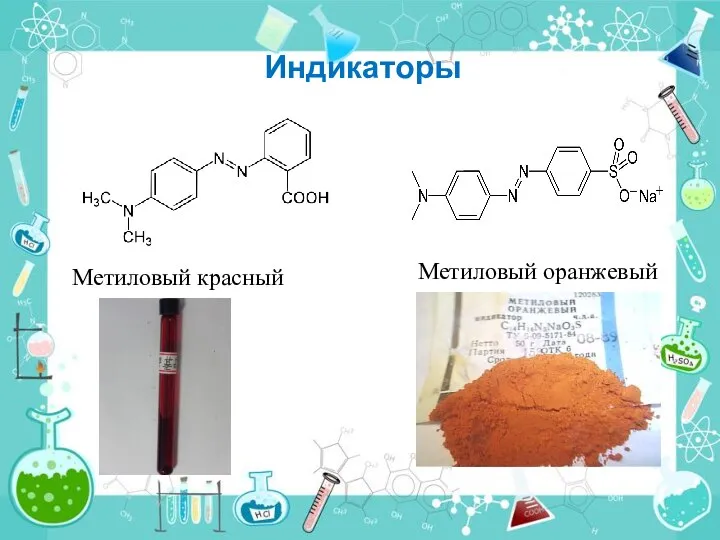
- 5. Индикаторы Метиловый красный Метиловый оранжевый
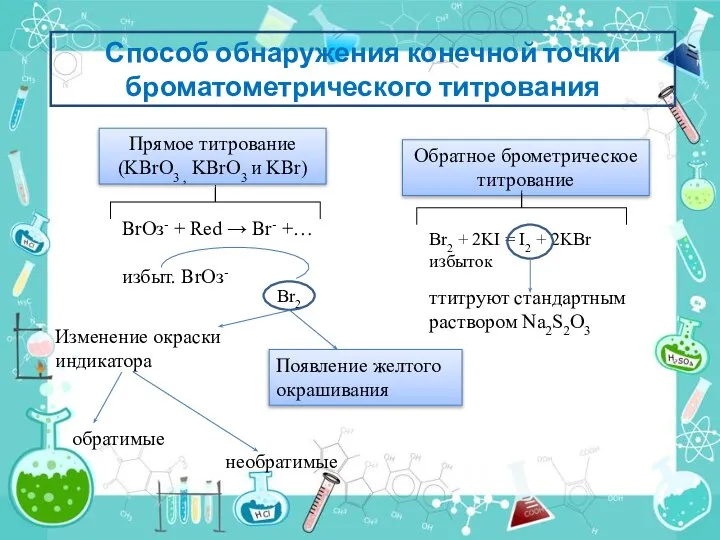
- 6. Способ обнаружения конечной точки броматометрического титрования Прямое титрование (KBrO3 , KBrO3 и KBr) Обратное брометрическое титрование
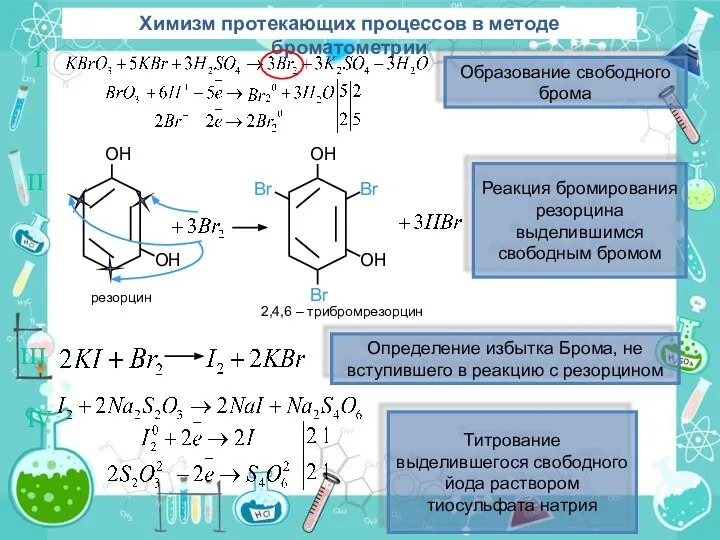
- 7. Химизм протекающих процессов в методе броматометрии I II OH OH Br Br Br резорцин 2,4,6 –
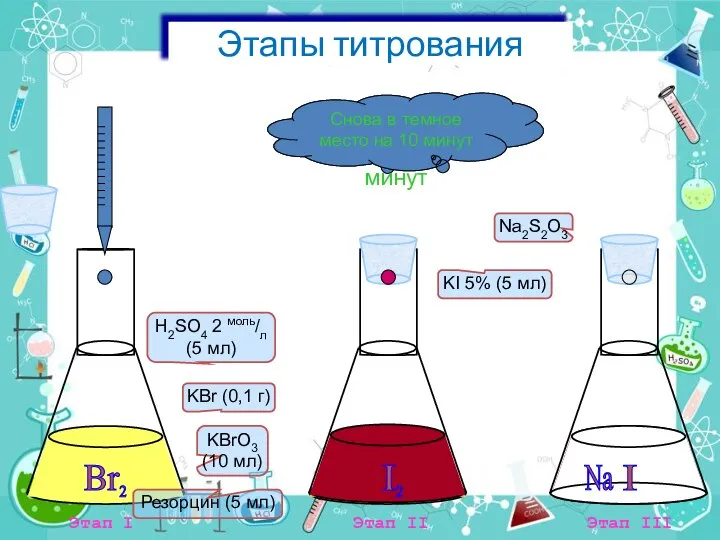
- 8. В темное место на 10 минут Резорцин (5 мл) KBrO3 (10 мл) KBr (0,1 г) H2SO4
- 9. Формула для расчета массовой доли резорцина:
- 10. НИТРИТОМЕТРИЯ
- 11. Применение
- 13. ТИТРАНТ нитритометрического титрования Вторичный стандартный раствор (раствор с установочным титром) 0,1 моль/л NaNO2 Первичные стандартные растворы
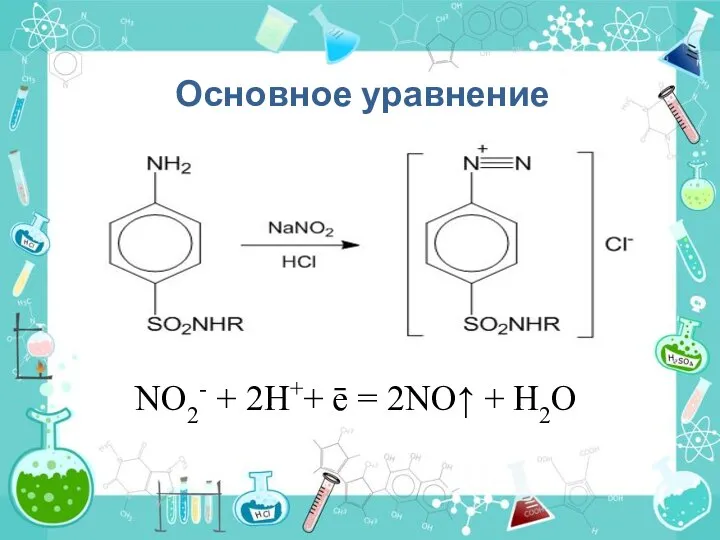
- 14. Основное уравнение NO2- + 2H++ ē = 2NO↑ + H2O
- 15. 1) Стандартизация NaNO2 5NaNO2 + 2КМпО4 + 3H2SO4 → 5NaNO3 + 2MnSO4 + +K2SO4 +3H2О NO2-
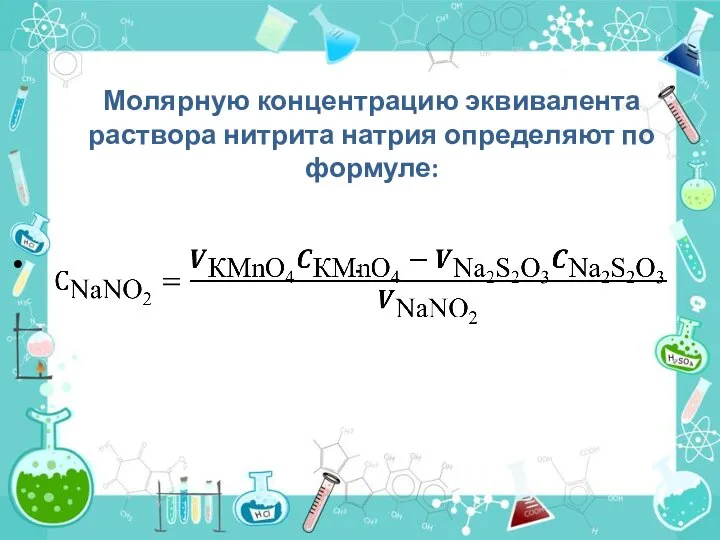
- 16. Молярную концентрацию эквивалента раствора нитрита натрия определяют по формуле:
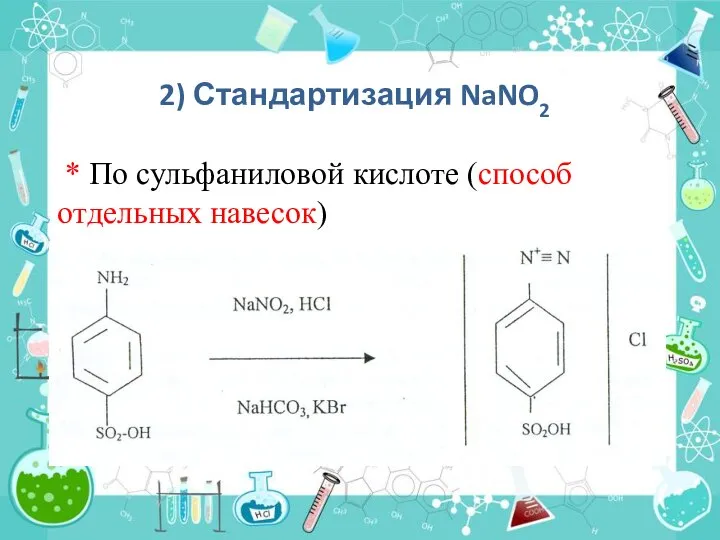
- 17. 2) Стандартизация NaNO2 * По сульфаниловой кислоте (способ отдельных навесок)
- 18. Молярную концентрацию эквивалента раствора нитрита натрия определяют по формуле: М (сульфаниловая кислота) = 173,19 г/моль
- 19. Фиксирование точки эквивалентности внешний индикатор: -йодкрахмальная бумага; - раствор флавокридина гидрохлорида и др. ) внутренний индикатор
- 20. Фиксирование точки эквивалентности Внешний индикатор Титруемый раствор йодокрахмальная бумага I- крахмал Избыток NaNO2 I2
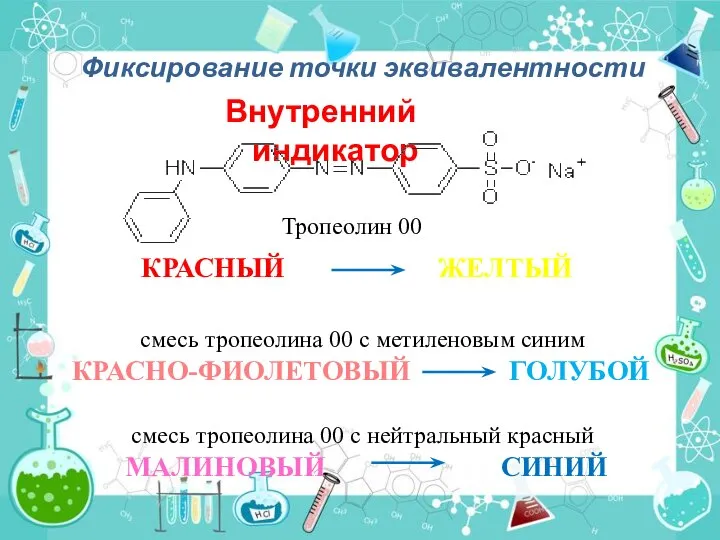
- 21. Фиксирование точки эквивалентности Внутренний индикатор Тропеолин 00 КРАСНЫЙ ЖЕЛТЫЙ смесь тропеолина 00 с метиленовым синим КРАСНО-ФИОЛЕТОВЫЙ
- 22. Условия титрования - температура не более 18-200С; - титрование при рН - введение катализатора - бромида
- 24. Скачать презентацию











 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества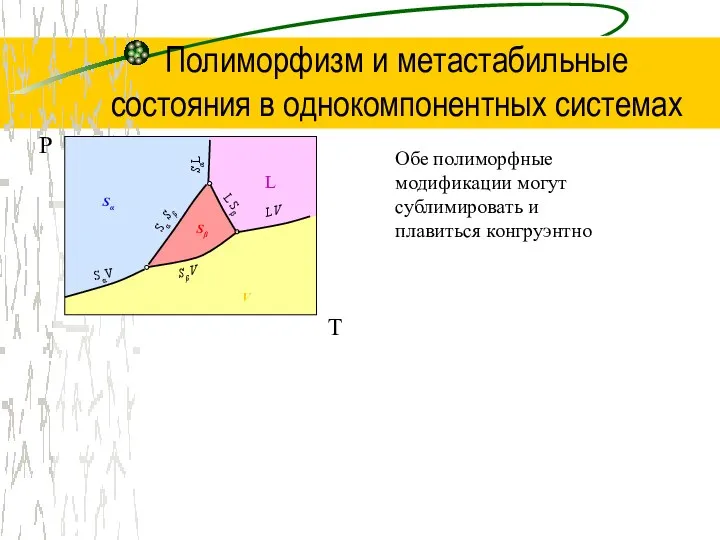 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі