Содержание
- 2. Предельные углеводороды (АЛКАНЫ) – атомы углерода соединены простыми σ связями (-С-С-С-); Непредельные углеводороды – содержат двойные
- 3. В настоящее время наиболее распространена международная (систематическая, ИЮПАК) номенклатура. Разберем ее на примере алканов. Попробуем назвать:
- 6. 3.Называют радикалы: метил, этил и т.д. (от простых к сложным, от менее разветвленным к более разветвленным).
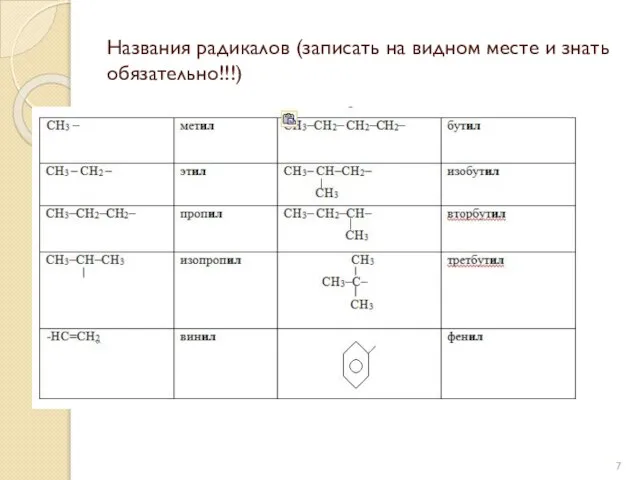
- 7. Названия радикалов (записать на видном месте и знать обязательно!!!)
- 8. 4. Перед названием радикала ставится цифра, означающая, от какого углеродного атома цепи ответвляется радикал. 5. Если
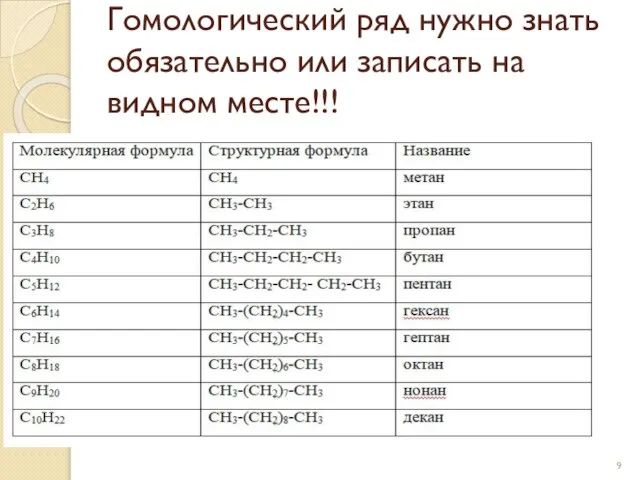
- 9. Гомологический ряд нужно знать обязательно или записать на видном месте!!!
- 10. Таким образом, данное вещество имеет название 2,4-диметилгексан.
- 11. При названии этиленовых углеводородов (алкенов) по номенклатуре ИЮПАК в качестве главной выбирают самую длинную углеродную цепь,
- 12. 3. Обозначают местоположения радикалов цифрой (цифрами), не забывая использовать приставки ди, три, тетра... и перечислять радикалы
- 13. Гомологический ряд алкенов
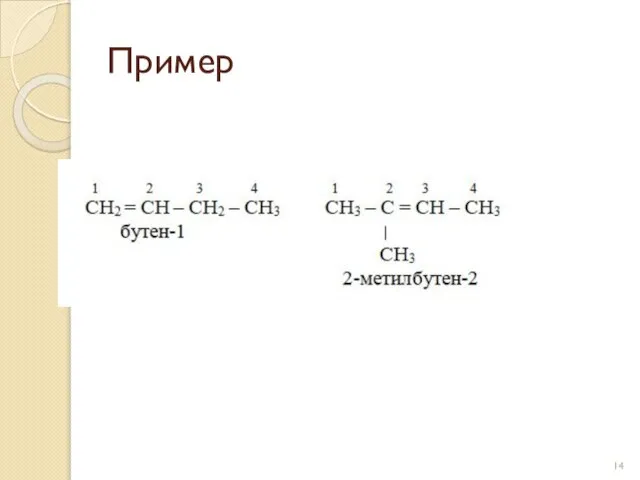
- 14. Пример
- 15. Называют ацетиленовые углеводороды так же, как и этиленовые, но вместо окончания –ен пишут –ин. После окончания
- 16. Систематическое название всех ароматических углеводородов – арены, а бензола – бензен. Гомологи бензола рассматривают, как замещённые
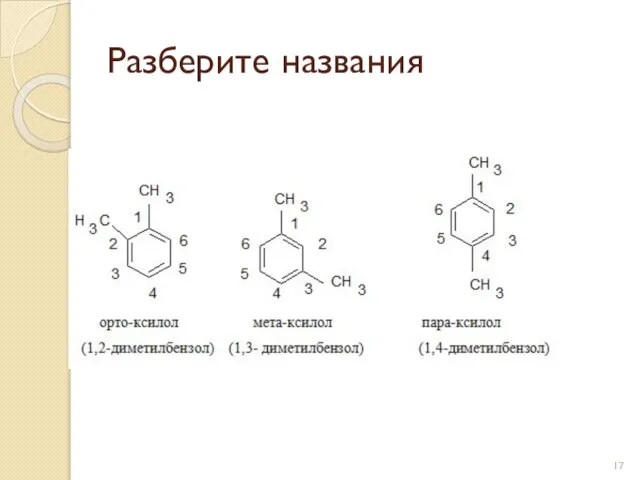
- 17. Разберите названия
- 18. Изомерия явление существования веществ, имеющих одинаковый состав (одинаковую молекулярную формулу), но разное строение (разные структурные формулы)
- 19. Изомерия алканов Для алканов характерна изомерия углеродного скелета. Для примера ниже приведены изомеры для вещества состава
- 20. Задание Попробуйте написать и назвать изомеры для алканов состава С5Н10 и С6Н14.
- 21. Изомерия алкенов Изомерия строения углеродной цепи. Положения двойной связи. Пространственная (цис- и транс- изомерия). Межклассовая изомерия.
- 22. 1. Изомерия углеродного скелета Разберем на примере С4Н8 (соответствует формуле СnH2n – это алкен) Пишем цепочку
- 23. 2.Изомеры положения двойной связи = связь может находится у любого атома углерода.
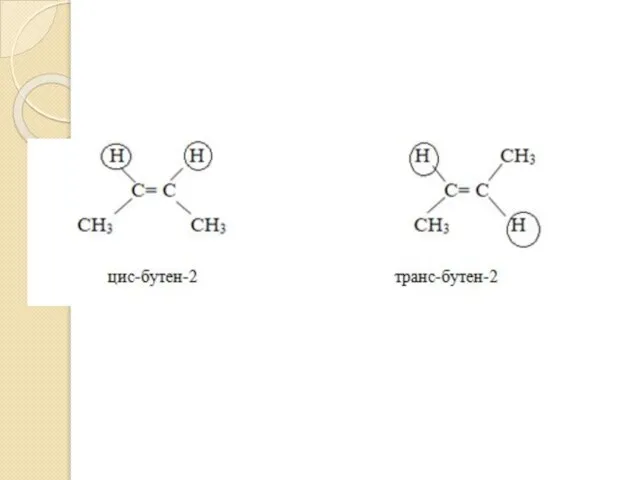
- 24. 3.Пространственные изомеры (цис- и транс- изомеры) Цис-изомер – 2 одинаковых заместителя находятся по одну сторону от
- 26. 4. Межклассовые изомеры (алкены изомерны циклоалканам)
- 27. Задание Напишите 6 изомеров, относящихся к разным видам изомерии для С5Н10 и назовите их.
- 28. Изомерия алкинов Изомерия строения углеродной цепи. Положения тройной связи. Межклассовая изомерия
- 29. 1. Изомерия углеродного скелета Разберем на примере С5Н8 (соответствует формуле СnH2n-2 – это алкин) Пишем цепочку
- 30. 2. Положения тройной связи
- 31. 3. Межклассовая изомерия алкины изомерны циклоалкенам и алкадиенам (2 двойные связи)
- 32. Задание Напишите 5 изомеров для С6Н10 и назовите их.
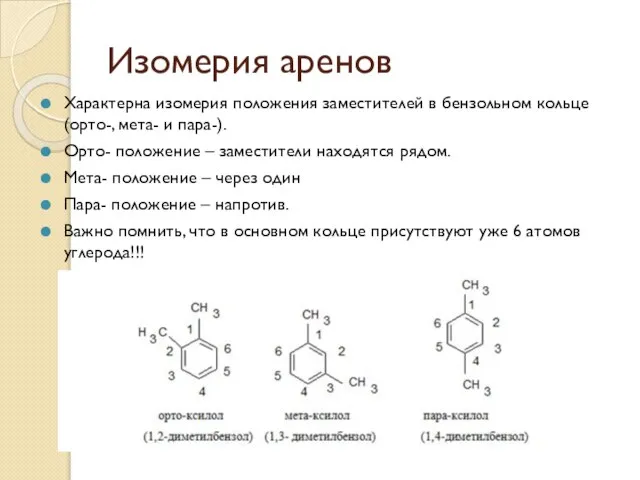
- 33. Изомерия аренов Характерна изомерия положения заместителей в бензольном кольце (орто-, мета- и пара-). Орто- положение –
- 34. Задание Напишите изомеры аренов для С9Н12 и назовите их. Подсказка: С9-С6(в основном кольце), получается, что в
- 35. Химические свойства углеводородов
- 36. Алканы Алканы имеют старинное название парафины, что означает, что они малоинертны. Дело в том, что атомы
- 37. Реакции замещения Более подробно разберем реакции замещения, хотя характерны и реакции горения, пиролиза, изомеризации, отщепления. Предельные
- 38. Правило Реакции замещения протекают по радикальному механизму в соответствии с нижеизложенным правилом. Замещение атомов водорода на
- 39. Реакция нитрования (Коновалова)
- 40. Реакция хлорирования
- 41. Химические свойства алкенов Двойная связь представляет собой сочетание σ- (прочной сигма) и π-(непрочной пи) связей. Поэтому
- 42. Реакции присоединения Присоединение водорода (гидрирования) или галогенов (галогенирования) всегда идёт по месту разрыва двойной связи. Аналогичным
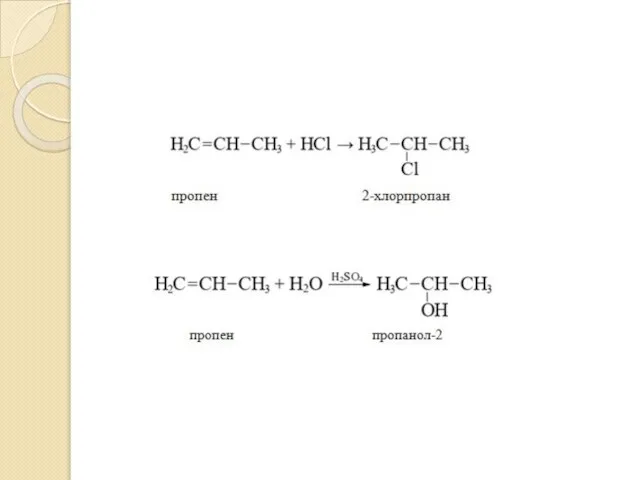
- 43. Реакция гидрогалогенирования и гидратации Несимметричные алкены присоединяют галогеноводороды (НBr,HCl) –гидрогалогенирование или воду (HOH) -гидратация) по правилу
- 45. Реакции полимеризации Под действием температуры, давления и в присутствии катализатора происходит разрыв π-связи и образование длинных
- 46. Реакции окисления Протекают в зависимости от условий. При мягком окислении водным раствором перманганата калия образуется двухатомный
- 47. Реакция окисления При горении (полном окислении) образуются углекислый газ, вода и тепло.
- 48. Химические свойства алкинов Тройная связь между атомами углерода включает одну σ-связь и две π-связи. Наличие π-связи
- 49. Реакции гидрогалогенирования и гидратации Данные реакции идут как с алкенами по правилу Марковникова
- 50. Особенность реакции гидратации Гидратация ацетиленовых углеводородов приводит к образованию карбонильных соединений. Гидратация ацетилена приводит к образованию
- 52. Реакция замещения!!!! (отличает алкены от алкинов) Соединённый с атомом углерода атом водорода может замещаться на металл,
- 53. Реакции окисления
- 54. Химические свойства аренов Арены имеют особый вид связи – ароматическую П-связь, состоящую из 6-Пи-электронов, она равномерно
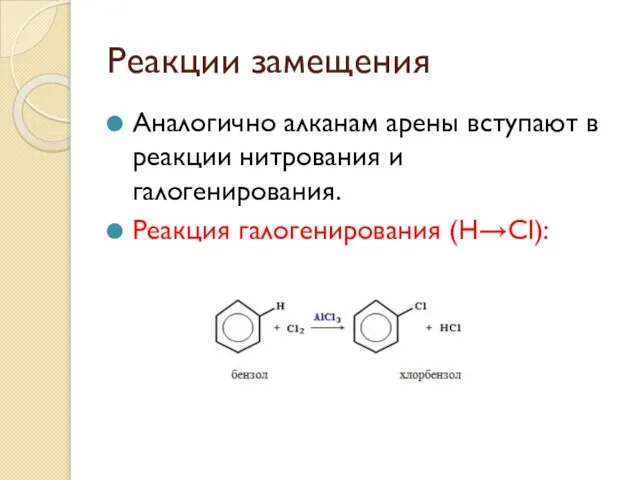
- 55. Реакции замещения Аналогично алканам арены вступают в реакции нитрования и галогенирования. Реакция галогенирования (Н→Сl):
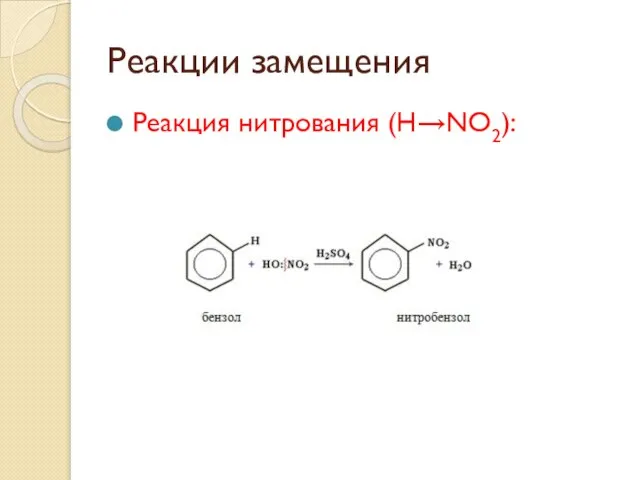
- 56. Реакции замещения Реакция нитрования (H→NO2):
- 57. Реакции замещения Реакции замещения у гомологов и изомеров аренов проходят согласно правилам ориентации в бензольном ядре.
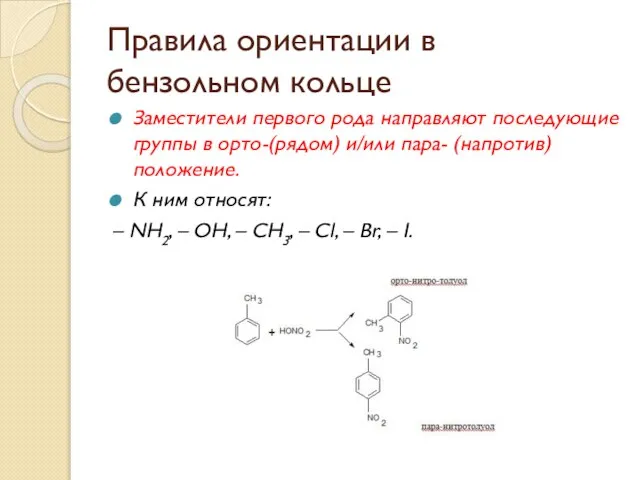
- 58. Правила ориентации в бензольном кольце Заместители первого рода направляют последующие группы в орто-(рядом) и/или пара- (напротив)
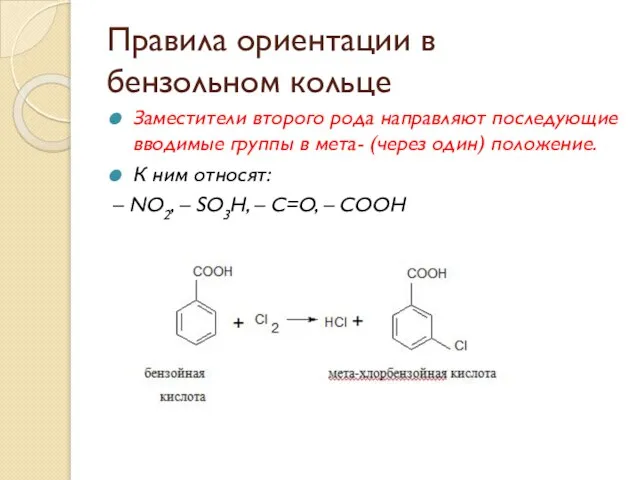
- 59. Правила ориентации в бензольном кольце Заместители второго рода направляют последующие вводимые группы в мета- (через один)
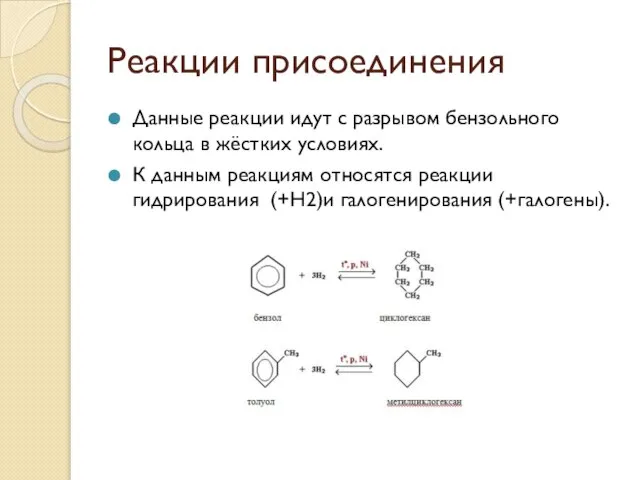
- 60. Реакции присоединения Данные реакции идут с разрывом бензольного кольца в жёстких условиях. К данным реакциям относятся
- 61. Реакции окисления Бензол окисляется с трудом, только под действием сильных окислителей. Гомологи бензолов окисляются легко до
- 63. Скачать презентацию
















































 Неделя химии в МБОУ (викторина)
Неделя химии в МБОУ (викторина) Свойства основных липопротеинов (ЛП) плазмы крови
Свойства основных липопротеинов (ЛП) плазмы крови Углеводы
Углеводы Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9
Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9 Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Органическая химия. Теория строения органических веществ
Органическая химия. Теория строения органических веществ Строение атома
Строение атома Презентация 1
Презентация 1 Теория активированного комплекса
Теория активированного комплекса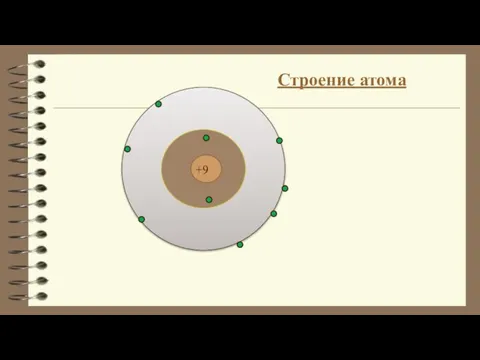 Строение атома
Строение атома Кислоты в химии
Кислоты в химии Природные источники углеводородов
Природные источники углеводородов Природные кислоты и щелочи. Индикаторы
Природные кислоты и щелочи. Индикаторы Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа
Закалка и отпуск стали. Ознакомление со структурами серого и белого чугуна. Распознавание руд железа Химическая технология. Структура ВКР
Химическая технология. Структура ВКР Интеллектуальная игра по химии «Металлы»
Интеллектуальная игра по химии «Металлы» Аминокислоты и их применение
Аминокислоты и их применение Углеволокно (карбон)
Углеволокно (карбон) Спирты (алканолы)
Спирты (алканолы) Дисперсные системы в пищевой промышленности
Дисперсные системы в пищевой промышленности Фосфор
Фосфор Пересчет данных анализа, выраженных в ионной форме
Пересчет данных анализа, выраженных в ионной форме Степень окисления. Составление формул бинарных соединений
Степень окисления. Составление формул бинарных соединений Металлы тоже воевали… 8 класс
Металлы тоже воевали… 8 класс Презентация на тему Серебро
Презентация на тему Серебро  Классификация химических реакций
Классификация химических реакций Sinteticheskie_Materialy_I_Ikh_Rol_1
Sinteticheskie_Materialy_I_Ikh_Rol_1