Содержание
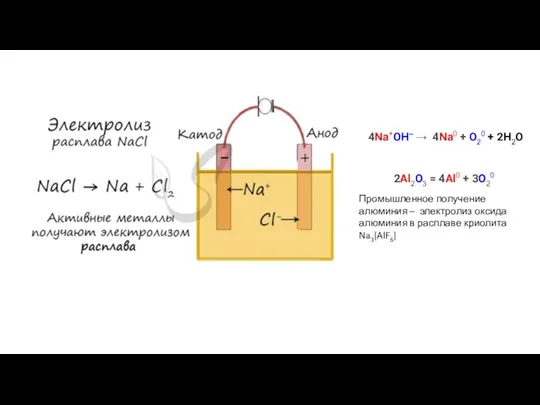
- 2. Электролиз
- 3. Электролиз - химическая реакция, происходящая при прохождении постоянного тока через электролит. Это разложение веществ на их
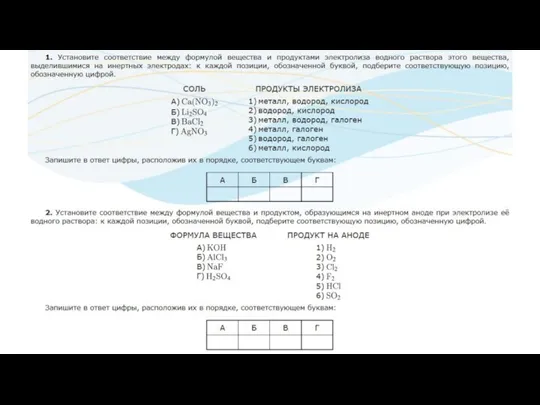
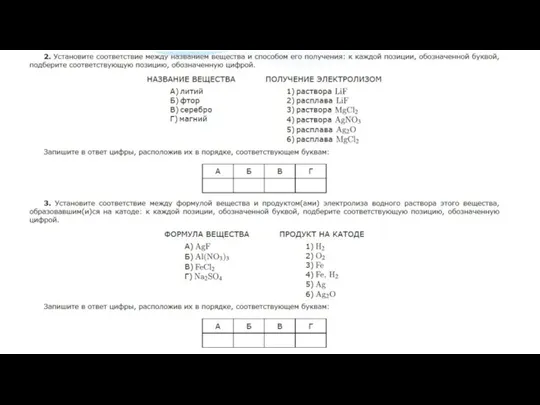
- 4. Процессы на катоде (-) К катоду притягиваются катионы (+ заряженные ионы) В зависимости от положения металла
- 5. Процессы на аноде (+) К аноду притягиваются анионы (- заряженные ионы)
- 6. NaCl, AgNO3, CuCl2, KF, CH3COOK
- 7. 4Na+OH– → 4Na0 + O20 + 2H2O 2Al2О3 = 4Al0 + 3О20 Промышленное получение алюминия –
- 8. Если материал электродов выполнен из того же металла, который присутствует в растворе в виде соли, или
- 12. Гидролиз Гидролиз - процесс расщепления молекул сложных химических веществ за счет реакции с молекулами воды.
- 13. Гидролиз солей может протекать: → обратимо: только небольшая часть частиц исходного вещества гидролизуется. → необратимо: практически
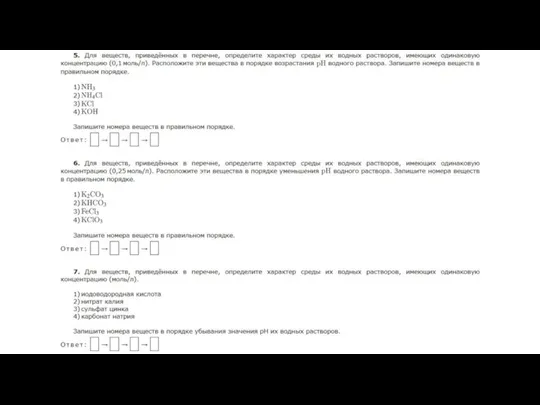
- 14. Обратимый гидролиз солей 1. Соли, образованные сильным основанием и слабой кислотой, гидролизуются ПО АНИОНУ. Примеры таких
- 15. 2. Соли, образованные слабым основанием и сильной кислотой, гидролизуются ПО КАТИОНУ. Пример такой соли: NH4Cl, FeCl3,
- 16. 3. Соли, образованные слабым основанием и слабой кислотой, гидролизуются И ПО КАТИОНУ, И ПО АНИОНУ. Примеры
- 17. Необратимый гидролиз солей выделяется ↓,↑ или вода. Необратимый гидролиз является химической реакцией: 2МеCl2 + 2Na2CO3 +
- 21. Комплексные соединения
- 22. [Cu(NH3)4]SO4 – сульфат тетраамминмеди (II), [Ni(H2O)6]Cl2 – хлорид гексаакваникеля (II). Na2[Zn(OH)4] – тетрагидроксоцинкат (II) натрия; K4[Fe(CN)6]
- 24. Скачать презентацию
















![[Cu(NH3)4]SO4 – сульфат тетраамминмеди (II), [Ni(H2O)6]Cl2 – хлорид гексаакваникеля (II). Na2[Zn(OH)4] –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1176372/slide-21.jpg)
 Эфирные масла
Эфирные масла Адсорбция на границе раствор-газ. ПАВ и ПНАВ
Адсорбция на границе раствор-газ. ПАВ и ПНАВ Общая характеристика оксидов
Общая характеристика оксидов Относительная молекулярная масса вещества
Относительная молекулярная масса вещества romanchuk
romanchuk Комплексные соединения
Комплексные соединения Алкены
Алкены Карбоцепные полимеры
Карбоцепные полимеры Сложные эфиры. Организация внеаудиторной творческой работы учащихся
Сложные эфиры. Организация внеаудиторной творческой работы учащихся Презентация на тему Алканы
Презентация на тему Алканы  Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Характеристика кислорода и серы
Характеристика кислорода и серы Химические понятия. Вещество. Химические явления. Выдающиеся ученые-химики
Химические понятия. Вещество. Химические явления. Выдающиеся ученые-химики Модель Андерсона
Модель Андерсона α-карбин и β-карбин
α-карбин и β-карбин Химическая связь
Химическая связь Химический эквивалент. Лекция 2
Химический эквивалент. Лекция 2 Дисперсные системы
Дисперсные системы Золоторудное поле Дуэт
Золоторудное поле Дуэт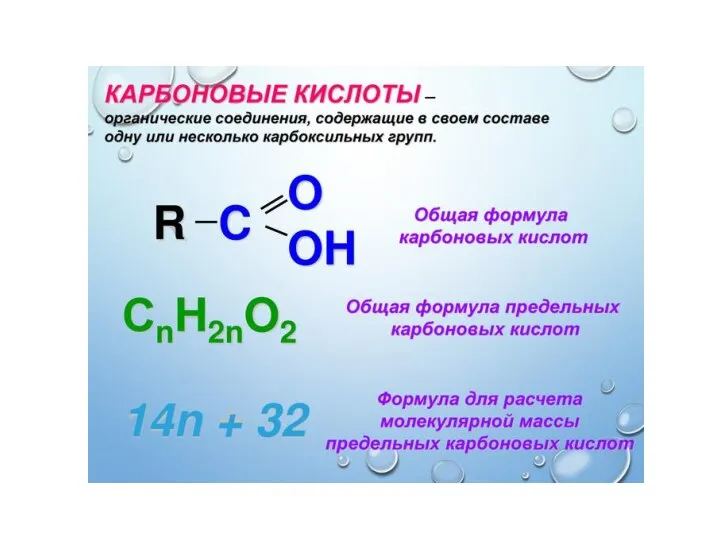 Карбоновые кислоты
Карбоновые кислоты Презентация на тему Общая характеристика металлов главных подгрупп I-III
Презентация на тему Общая характеристика металлов главных подгрупп I-III  Галогены
Галогены Фосфор в организме человека
Фосфор в организме человека Физика твердого тела. Введение в кристаллографию. Построение стереографических проекций
Физика твердого тела. Введение в кристаллографию. Построение стереографических проекций Типы химической реакции
Типы химической реакции Взаимодействие карбонатов с разбавленными кислотами. Качественные реакции на карбонаты
Взаимодействие карбонатов с разбавленными кислотами. Качественные реакции на карбонаты Структура неорганических ионных соединений. Лекция 12
Структура неорганических ионных соединений. Лекция 12 Полезные ископаемые
Полезные ископаемые