Слайд 2Загадки
Если в паре элементов
Кислород вторым стоит,
Ты же знаешь, эта пара
Называется …
Если формулы

начало
Представляется с металла,
ОН-красуется затем,
Вещества знакомы всем.
Не надо придумывать им название
Ведь эти вещества …
Слайд 3Задание
Распределите формулы вещества по классам в таблицу;
Подчеркните формулы кислотных оксидов.
HCl, SO3, HNO3,

H2SO4, Ca(OH)2, K2O, Na2O, CO2, N2O5, Al2O3, Zn(OH)2, AL(OH)3
Слайд 4Можно ли объединить оставшиеся формулы веществ в одну группу?
HCl, HNO3, H2SO4

Слайд 5КИСЛОТЫ
Из своего жизненного опыта вы знаете, что многие продукты питания обладают кислым

вкусом.
Кислый вкус этим продуктам придают кислоты.
Кислый вкус лимону придает лимонная кислота,
Яблоку – яблочная кислота.
Скисшему молоку – молочная кислота.
Щавель имеет кислый вкус благодаря наличию в его листьях щавельной кислоты.
Слайд 6Целеполагание
Сформировать комплекс знаний о кислотах как классе неорганических веществ

Слайд 7
Состав кислот и названий кислот.
Классификация кислот.
Распознавание кислот.
Определение степени окисления элементов, входящих

в состав кислот и зарядов ионов.
История открытия кислот.
Применение кислот.
Слайд 9Названия кислот состоят из прилагательного и существительного «кислота».
Прилагательные бескислородных кислот состоят из

двух корней обозначающих химические элементы, составляющие эти кислоты.
(Пример: H2S- сероводородная; HF- фтороводородная; HBr- бромоводородная и др.)
Прилагательные кислородосодержащих кислот состоят из корня-названия химического элемента-неметалла, образующего данное соединение плюс суффикс –н, если данный элемент находится в высшей степени окисления;
(Пример: H2SO4- серная; HNO3- азотистая.)
Или суффикс –ист, если этот элемент имеет промежуточную степень окисления (H2SO3-сернистая; HNO2-азотистая.)










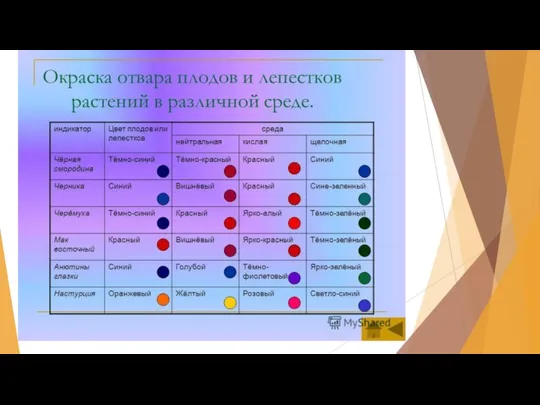
 Электроотрицательность
Электроотрицательность Электронная конфигурация атома
Электронная конфигурация атома Сера. Характеристика химического элемента и простого вещества
Сера. Характеристика химического элемента и простого вещества Белки
Белки Кислоты. 8 клас
Кислоты. 8 клас Основы химической термодинамики
Основы химической термодинамики Оксиды в свете ТЭД
Оксиды в свете ТЭД Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Марганец. Химия элементов. Кислородосодержащие соединения
Марганец. Химия элементов. Кислородосодержащие соединения Лекция1Тов
Лекция1Тов Малотоннажные термопласты
Малотоннажные термопласты Классификация органических веществ
Классификация органических веществ Техника безопасности на уроках химии
Техника безопасности на уроках химии Презентация на тему Стекло. История открытия, получение, применение
Презентация на тему Стекло. История открытия, получение, применение  Изменение агрегатных состояний вещества
Изменение агрегатных состояний вещества 5кл 20.10практична робота
5кл 20.10практична робота Спирты. Методы получения
Спирты. Методы получения Электролиз
Электролиз Способы очистки питьевой воды
Способы очистки питьевой воды Цезий сверхактивный 1860 г
Цезий сверхактивный 1860 г Аминокислоты. Белки. Лекция 2
Аминокислоты. Белки. Лекция 2 Химия природная или синтетическая. За и против
Химия природная или синтетическая. За и против Алканы. Этан
Алканы. Этан Химия в загадках
Химия в загадках 12_BROMATOMETRIYa_NITRITOMETRIYa
12_BROMATOMETRIYa_NITRITOMETRIYa Презентация на тему Многообразие карбоновых кислот
Презентация на тему Многообразие карбоновых кислот  Химическая связь. Строение вещества
Химическая связь. Строение вещества Кислотно-основные равновесия в растворах
Кислотно-основные равновесия в растворах